據外媒報道,太平洋西北國家實驗室(PNNL)的科學家們發現,電池中的分子也會玩一種“搶座位”的游戲,進而損害電池性能。研究人員證明,氧原子的激發能夠提升鋰離子電池性能,同時也會造成損傷。這一發現為制造壽命更長、容量更大的可充電鋰離子電池提供科學依據。
氧的缺點
控制分子的結合和流動方式,對電池儲存和釋放能量至關重要。在鋰離子電池中,充電時,鋰離子從正極通過電解質流向負極;放電時,相同的離子會返回正極,精確地回到所屬晶格中,晶格里還有其他原子,比如氧、鎳、鈷和鎂。這種循環往復使電池能夠儲存和釋放能量。
為了促進這一過程,科學家們利用氧作為電子的供體,增加從正極中流出的鋰。但是,“被激發”的氧原子能對精心構造的正極造成破壞。PNNL研究小組發現,這些氧分子是制造混亂的罪魁禍首,它們的流動性很強,很可能從表面逃逸,導致電池容量減少,最終導致電池故障,它們可以輕松地交換分子位置,從而影響電池結構。
領導這項研究的PNNL科學家Chongmin Wang表示:“利用氧原子提供電子,可以增加容量。然而,這是要付出代價的,人們還沒有意識到這一點。我們知道氧可以提高電池的性能,但還沒有完全理解其中的原理。”
正極大戰
Wang的團隊精確追蹤正極中氧發生的變化,揭示了分子之間進行的“搶座位”游戲,其中包括被激發的氧“霸王”,它們趁機從整體結構中離開,造成巨大的缺口,鋰離子阻礙了它們原路返回。
研究小組發現,氧原子貢獻電子后,過度激發的氧原子很容易從正極表面逃逸,在精心構造的電池晶格中留下空位。表面的氧原子離開后,在整體結構中,其他氧原子就會擠進這些空位里。越來越多的氧分子也跟著發生連鎖反應,進入空隙并逸出表面。隨著這一過程的繼續,缺陷從正極表面一點點滲透至更深的材料中,形成大洞。這種位置交換會破壞電池之前有序的原子結構。氧原子離開后留下的空位會形成空隙,造成巨大的屏障,阻止鋰離子回到原有位置。其他原子,如鎳、鎂、鈷和氧,開始四處移動,像惡霸一樣橫行霸道,在鋰進行必要的化學反應時,很可能偷走原本屬于鋰的位置。
如果越來越多的鋰原子不能精確地回到自己在正極中的位置,那么,能夠在正負極之間往來的鋰原子就會減少,電池儲存的能量將越來越少。大量的空位或空隙會破壞晶格的穩定性,導致容量減少,最終導致電池失效。
為任性的氧做保鏢
”一旦失去足夠的氧原子,電池容量就會損失,整個結構隨之崩潰。“Wang說。在此項研究中,他所在的PNNL團隊與來自中國北京理工大學、勞倫斯伯克利國家實驗室和阿貢國家實驗室的科學家展開合作。
該團隊正在探索阻止此類缺陷的方法。有一種想法是穩定表面的氧,將氧原子更緊密地鎖在應有位置,阻止它們逃逸。研究人員正在嘗試利用氧化鋯分子施加化學影響,并充當保鏢,使氧原子保持在適當位置,從而減少氧損失。這有助于保持整體結構,讓鋰離子更從容地移動。
-
電子
+關注
關注
32文章
1879瀏覽量
89362 -
電池
+關注
關注
84文章
10564瀏覽量
129491
發布評論請先 登錄
相關推薦
基于BQ76952的電池包短路保護DSG FET損壞原因及優化方法

BQ76952在電池均衡時電壓采樣不準確的原因分析及優化方法

了解鋰電池熱失控:原因及預防
蓄電池測試儀的常見故障及原因分析
鋰電池內阻變大的原因及影響
蓄電池充電電流升不上去的原因?怎么解決?
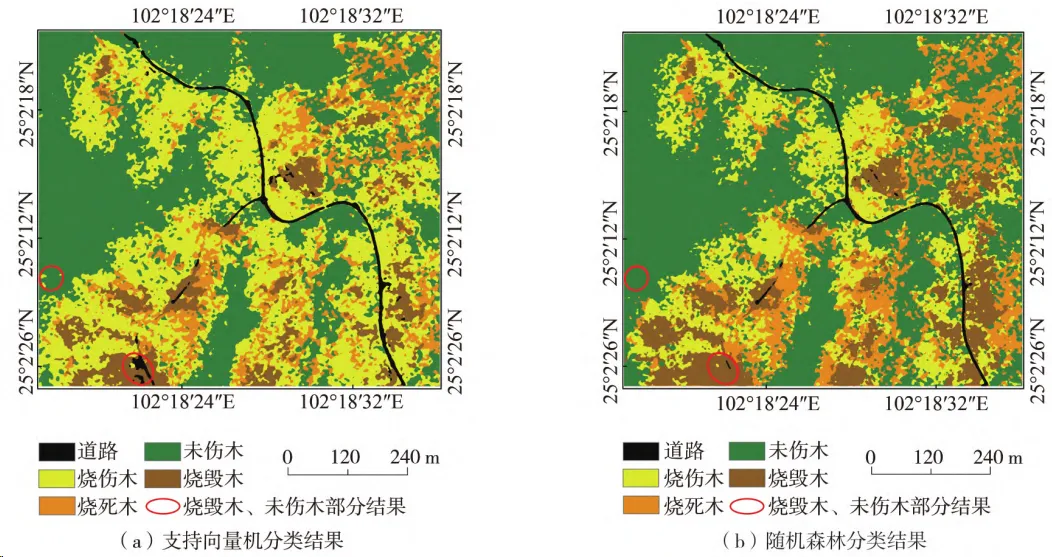
多光譜無人機的林木火災受損信息提取研究2.0
新能源汽車電池包故障是什么原因?
電池點焊機選擇電阻焊與激光焊的原因:優勢分析與應用探討





 電池受損的原因
電池受損的原因










評論