據(jù)外媒New Atlas報(bào)道,癌癥有許多賴以生存和發(fā)展的工具,因此,在阻止癌癥發(fā)展方面存在諸多可能性。一種這樣的途徑集中于被稱為溶酶體的細(xì)胞“垃圾處理單元”,與健康細(xì)胞相比,其在癌細(xì)胞中特別容易受到傷害。韓國(guó)科學(xué)家近日發(fā)現(xiàn),通過(guò)精心混合帶電納米粒子,它們可以給癌細(xì)胞帶來(lái)致命的打擊。
溶酶體是充滿酶和酸的微小囊,它們會(huì)降解細(xì)胞中不需要的部分,然后再將其回收或傾倒到細(xì)胞壁之外,就像將垃圾帶到路邊一樣。最近的研究表明,溶酶體可能在阿爾茨海默病中發(fā)揮作用,其中功能失調(diào)的處置系統(tǒng)可能導(dǎo)致大腦中有毒蛋白質(zhì)的積累。
韓國(guó)基礎(chǔ)科學(xué)研究所的科學(xué)家正在努力研究功能失調(diào)的溶酶體,原因是受損的溶酶體在細(xì)胞內(nèi)釋放垃圾會(huì)導(dǎo)致該細(xì)胞死亡,當(dāng)涉及癌細(xì)胞時(shí)這顯然是一件好事。有利于團(tuán)隊(duì)的一件事是,癌細(xì)胞的溶酶體比健康細(xì)胞更容易受到損害。麻煩在于提出僅針對(duì)前者的療法,而使后者完好無(wú)損。
研究人員認(rèn)為,他們已經(jīng)找到了實(shí)現(xiàn)這一目標(biāo)的方法,它涉及帶負(fù)電和帶正電的納米粒子的精細(xì)混合。這些在癌細(xì)胞表面上選擇性地成簇形成,然后在溶酶體內(nèi)部轉(zhuǎn)化為納米顆粒晶體,使它們?nèi)苊洠饾u變質(zhì)并最終死亡。
該研究的共同主要作者Bartosz A. Grzybowski說(shuō):“在這項(xiàng)工作中,我們利用了放松管制的癌細(xì)胞廢物管理系統(tǒng),充當(dāng)了‘納米級(jí)裝配線’,用于構(gòu)建高質(zhì)量的納米顆粒晶體,這些晶體可以摧毀非常溶酶體的‘反應(yīng)器’,從而使它們首先生長(zhǎng)。”
該團(tuán)隊(duì)對(duì)這種新型療法進(jìn)行了不同配方的實(shí)驗(yàn),發(fā)現(xiàn)具有80%帶正電和20%帶負(fù)電的配體的納米顆粒對(duì)于癌細(xì)胞的選擇性是最佳的。該團(tuán)隊(duì)還認(rèn)為,對(duì)部分帶負(fù)電荷的配體的pH敏感度是癌細(xì)胞選擇性的關(guān)鍵。這是通過(guò)對(duì)多種癌細(xì)胞類型進(jìn)行的實(shí)驗(yàn)確定的,該團(tuán)隊(duì)的納米顆粒被證明對(duì)所有癌細(xì)胞均有效。
研究的第一作者M(jìn)agdalena Borkowska補(bǔ)充說(shuō):“我們的結(jié)論是基于對(duì)13種不同肉瘤、黑素瘤、乳腺癌和肺癌細(xì)胞系與四種非癌細(xì)胞類型的比較。” 納米粒子對(duì)所有13種癌癥細(xì)胞都有效,而不會(huì)傷害非癌細(xì)胞。”研究小組計(jì)劃在未來(lái)研究這種混合電荷策略是否可以有效對(duì)抗動(dòng)物模型中的腫瘤。
該研究發(fā)表在《自然納米技術(shù)》雜志上。
-
納米
+關(guān)注
關(guān)注
2文章
696瀏覽量
36980
發(fā)布評(píng)論請(qǐng)先 登錄
相關(guān)推薦
北海道大學(xué):基于ZnO納米粒子激光誘導(dǎo)石墨烯的超靈敏可拉伸應(yīng)變傳感器
磁調(diào)制式電流傳感器在粒子加速器中的應(yīng)用
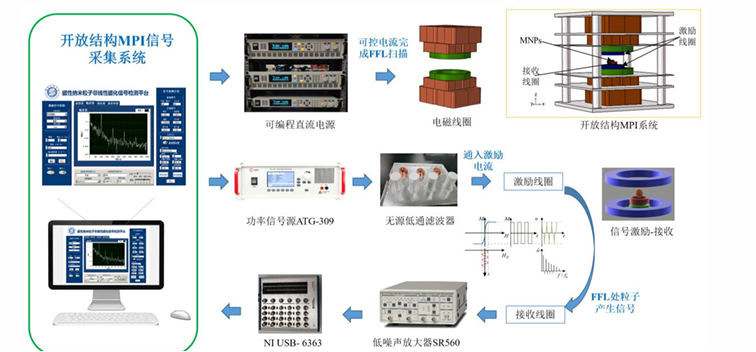
安泰功率放大器在磁性納米粒子血管精細(xì)成像方法中的應(yīng)用
活細(xì)胞的“聚光燈”——前沿活細(xì)胞成像的案例分享

ATG-2000系列功率信號(hào)源在介電電泳細(xì)胞分選測(cè)試中的應(yīng)用

P60.X200系列高精度一維壓電納米定位臺(tái)應(yīng)用于光學(xué)測(cè)量

安森美宣布收購(gòu)CQD傳感器技術(shù)公司
液滴微流控技術(shù)在癌癥研究中的應(yīng)用:從單細(xì)胞分析到3D細(xì)胞培養(yǎng)
用光子連接懸浮在真空中的納米粒子,并控制它們之間的相互作用
Zeta電位納米粒度儀的原理介紹
更快、更高效的納米粒子成像系統(tǒng)
PPTC熱敏電阻原理及應(yīng)用領(lǐng)域
回旋加速器中粒子的最大動(dòng)能與什么有關(guān)
自供電氣體傳感器未來(lái)發(fā)展機(jī)遇與挑戰(zhàn)




 帶電納米粒子能給癌細(xì)胞帶來(lái)致命打擊
帶電納米粒子能給癌細(xì)胞帶來(lái)致命打擊











評(píng)論