眾所周知,新藥研發普遍面臨著研發周期長、投入資金大、臨床試驗失敗率高的問題。其中一大部分原因在于新藥臨床前試驗數據不夠準確,不能及時篩選出新藥的潛在問題。
據了解,目前業界臨床前試驗大多使用2D細胞模型和動物模型,以觀察新藥實際效果或可能出現的副作用。但問題是,2D細胞模型生理功能不完整,無法反映組織間的相互作用和生理狀態下的藥物發生機理;動物則與人類之間則存在種屬差異,無法準確地模擬人體系統,這些都會致使試驗結果并不準確。
新藥研發亟需一種精準性更高、更能反映生理機制的藥物篩選技術,器官芯片便是其一,它通過逆向工程還原人體器官關鍵的部位和功能,可在極大程度上還原人體器官模型。
36氪近期接觸到的大橡科技,即是自主研發和生產人體器官芯片的一家科技企業,它專注于推動器官芯片在新藥研發、個體化醫療等領域的廣泛應用,為行業提供更精準、更高效、更經濟的藥物研發和精準用藥解決方案。它曾在2019年11月獲得由藥明康德領投,久友資本、復容投資跟投的千萬元天使輪融資。
據大橡科技CEO周宇介紹,目前,這家公司已取得突破性進展,正式推出了三款可商用的“器官芯片”產品,具體包括針對藥物肝毒性測試的肝臟模型、針對抗腫瘤藥物研發的腫瘤模型、和針對腦部疾病藥物研發的血腦屏障模型。他表示,這也是國內首批商用器官芯片產品。
關于器官芯片技術,它主要是利用微流控技術控制流體流動,結合細胞與細胞相互作用、基質特性以及生物化學和生物力學特性,在芯片上構建三維的人體器官生理微系統。據悉,微流控芯片系統能夠將微組織器官的直徑控制在毫米甚至微米級別,并且增強其營養交換,防止微組織器官的核心細胞的死亡。
大橡科技通過將生物組織工程學和微流控技術結合,在芯片上構建了三維的人體器官生理微系統,包含活體細胞、組織界面、生物流體、機械力等器官“微環境”關鍵要素,可在體外重現人類器官結構和功能特征。
周宇表示,基于這種仿生的器官芯片模型,新藥臨床前試驗能得到準確數據,同時縮短試驗時間,降低新藥研發失敗的風險。
值得一提的是,大橡科技器官芯片產品現已實現了細胞從2D維度向3D維度(在核心受試細胞周圍構建三維人體器官生理微系統)的跨越,即它通過微加工技術將芯片通道控制在微米級,既使微器官及其微環境更接近人體真實環境,也使試驗耗材得以大幅節省。
周宇介紹到,耗材用量的減少也意味著,大橡科技可以將昂貴但對藥物更敏感的人原代細胞應用到模型中,并使其整體保持較低的成本。
以此次大橡科技推出的肝臟模型為例,即采用了人原代肝細胞,也就是從人類肝組織分離的細胞。該模型在肝細胞培養1天后即可加藥測試,且在培養長達28天后仍可保持極好的活性,既能用于肝臟急毒性測試,也能用于慢毒性測試,這一效果是傳統的細胞模型無法實現的。
目前,中國正處于創新藥的黃金發展期,作為能反映人體器官微生理系統的關鍵生理學特征,能準確、穩定獲得臨床前試驗數據的技術,“器官芯片”無疑會具有廣闊的發展前景。
資料顯示,截至目前,全球范圍內已發表的人體不同的器官芯片有:腸道芯片、肺部芯片、心臟芯片、肝臟芯片、血管芯片、腫瘤芯片、胎盤芯片以及集合多種器官芯片組成的人體芯片(human-on-a-chip)。
從技術發展進程來看,2004年全球第一篇關于器官芯片的研究文章發表,“器官芯片”的概念被首次提出;隨后,美國政府投入了大量資源進行研究,并在2010年后開始有組織、系統性地支持器官芯片研究及后續的產業化。
反觀中國,雖然相關科研機構在2010年前后也開始投入更多精力研究器官芯片技術,科技部也在2013年推出國家支持的器官芯片重大專項,但器官芯片行業在國內整體仍缺乏資金和政府系統性組織的支持,更多還停留在科研層面。
像中國科學院大學溫州研究院的一支團隊就在進行類似研究,試圖設計高通量的藥物篩選平臺構建體外肺泡的概念,縮短整個藥物研發的流程,但產業界應用較少。
周宇表示,相關產品的研發仍需要克服較高的門檻,國內有不少研究院所正從事器官芯片領域的研究,但其研究但時間內還難以實現產業化落地。
團隊方面,大橡科技聚集了一批通識微流控、醫學組織工程、細胞生物學、藥理學、病理學等學科的“專才”,核心人員在“器官芯片”領域10年以上的研究經驗,公司90%都是研發人員。以公司CTO肖榮榮為例,其研究內容就橫跨了包括生物技術、微流控芯片、生物組織工程、分子生物學在內的多個專業領域。
-
3D
+關注
關注
9文章
2875瀏覽量
107486 -
仿生
+關注
關注
1文章
33瀏覽量
8268 -
器官芯片
+關注
關注
1文章
37瀏覽量
14672
原文標題:加速新藥研發,大橡科技推出三款商用“器官芯片”產品
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
三款低功耗MCU,實現應用產品的耐久續航力
揚杰科技11款產品入選《2024長三角汽車芯片產品手冊》
芯片上集成功能性血管化類器官的微流控平臺
最近推出了JFE150,這是一款面向低噪聲應用的分立式 N 溝道 JFET
恩智浦半導體獲得商用密碼安全芯片產品認證證書
Microchip推出三款電動汽車充電器參考設計
華擎科技正式推出兩款無風扇設計顯卡
國芯新材料研發并推出全球首款可商用的鉀離子電池產品
國芯科技近日成功推出了新一代指紋芯片CCM4101
微軟推出Surface Laptop 6商用版和Surface Pro 10商用版
意法半導體新推出了兩款近距離無線點對點收發器芯片
芯來科技正式發布首款專用處理器產品線Nuclei Intelligence系列
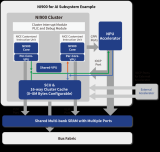
ATA-3090B功率放大器在醫療行業器官芯片中的應用
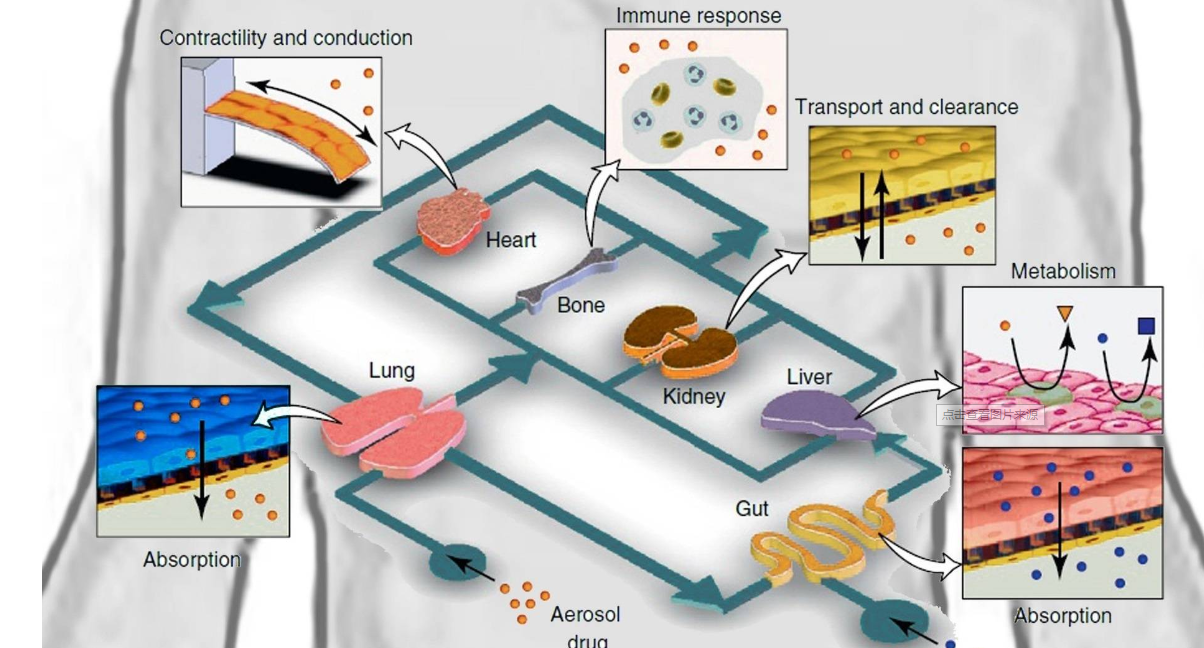




 大橡科技正式推出了三款可商用的“器官芯片”產品
大橡科技正式推出了三款可商用的“器官芯片”產品










評論