近日,武漢科技大學(xué)醫(yī)學(xué)院公共衛(wèi)生學(xué)院李誠予副教授在CRISPR/Cas12a生物傳感器的構(gòu)建方面取得階段性進(jìn)展,研究成果“A boosting upconversion luminescent resonance energy transfer and biomimetic periodic chip integrated CRISPR/Cas12a biosensor for functional DNA regulated transduction of non-nucleic acid target”發(fā)表于SCI一區(qū)期刊《Biosensors and Bioelectronics》上。
近年來,基于Clustered regularly interspaced short palindromic repeats (CRISPR) 的基因編輯技術(shù)受到了科學(xué)界的廣泛關(guān)注。這項革命性技術(shù)的靈感是來源于細(xì)菌和病毒在生命進(jìn)化歷史上進(jìn)行斗爭所產(chǎn)生的免疫應(yīng)答模式。簡單來說,就是病毒能把自己的基因整合到細(xì)菌內(nèi),利用細(xì)菌的細(xì)胞工具為自己的基因復(fù)制服務(wù),而細(xì)菌為了將病毒的外來入侵基因清除,進(jìn)化出CRISPR系統(tǒng)。利用這個系統(tǒng),細(xì)菌可以不動聲色地把病毒基因從自己的基因組上切除。
由于CRISPR系統(tǒng)需要核酸酶(Cas蛋白)結(jié)合一段引導(dǎo)RNA(CrRNA)來實(shí)現(xiàn)目標(biāo)核酸的特異性識別,因此該技術(shù)在實(shí)際操作過程中具有很高的精準(zhǔn)度。相比于早期發(fā)現(xiàn)的CRISPR/Cas9系統(tǒng),近年來新發(fā)現(xiàn)的CRISPR/Cas12a系統(tǒng)不僅具備CRISPR/Cas9的cis cleavage功能,還可實(shí)現(xiàn)一種特殊的trans cleavage效應(yīng),即額外對任意“非目標(biāo)”核酸序列進(jìn)行切割。
近期,借助CRISPR/Cas12a優(yōu)異的目標(biāo)物識別精準(zhǔn)度以及trans cleavage能力,研究人員基于電化學(xué)、比色、熒光等分析平臺構(gòu)建了一系列的生物傳感器,其中熒光分析受到更為廣泛的關(guān)注。但是,由于缺少有效的目標(biāo)物轉(zhuǎn)導(dǎo)模式,目前所報道的CRISPR/Cas12a傳感器都只能用于單純核酸的檢測。為進(jìn)一步擴(kuò)大分析物的范圍,李誠予副教授在本工作中將“功能化DNA”這一概念引入CRISPR/Cas12a系統(tǒng)以實(shí)現(xiàn)對非核酸目標(biāo)物的轉(zhuǎn)導(dǎo)。通過將適配體和DNAzyme作為功能化DNA,上述CRISPR/Cas12a傳感器可有效對模型目標(biāo)物ATP和Na+分別進(jìn)行信號轉(zhuǎn)導(dǎo)。
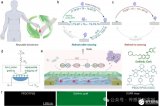
由于目前所構(gòu)建的CRISPR/Cas12a熒光生物傳感器都是基于傳統(tǒng)的斯托克斯熒光發(fā)射模式(可見光激發(fā)),因此它們在復(fù)雜生物樣本(如細(xì)胞提取液,人體體液)中仍存在挑戰(zhàn)。為解決這一問題,李誠予副教授將“基于上轉(zhuǎn)換發(fā)光的發(fā)光共振能量轉(zhuǎn)移(LRET)”這一檢測模式進(jìn)一步引入到CRISPR/Cas12a系統(tǒng)中。由于上轉(zhuǎn)換納米顆粒(UCNP)的尺寸較大(一般> 20 nm), 將UCNP作為能量供體的LRET體系存在能量轉(zhuǎn)移效率很低(一般< 50%)這一瓶頸。李誠予副教授在本工作中構(gòu)建了一種“能量集中”型UCNP,即通過構(gòu)建一種“三明治”結(jié)構(gòu)的UCNP,將上轉(zhuǎn)換發(fā)光區(qū)域極大地局限于一個很窄的內(nèi)殼層內(nèi)(~ 2.5 nm)。基于以上設(shè)計理念,上述改進(jìn)的UCNP對其表面所偶聯(lián)的報道DNA(修飾有BHQ-1分子)的能量轉(zhuǎn)移效率可被顯著提升至92.9%。
“能量集中”型UCNP與仿生周期芯片相結(jié)合的針對非核酸目標(biāo)物的CRISPR/Cas12a生物傳感器原理圖
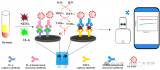
為進(jìn)一步提升分析靈敏度并同時實(shí)現(xiàn)“即使檢測”,李誠予隨后將上述傳感體系負(fù)載于一種特殊的“仿生”周期芯片當(dāng)中。通過選用光子晶體作為信號放大器與芯片界面,上述上轉(zhuǎn)換發(fā)光強(qiáng)度可被大幅提升35倍。同時,該傳感器可在便攜式手持980 nm激光器的照射下,通過手機(jī)拍照這一簡單的方式來進(jìn)行定量檢測,對ATP和Na+的檢出限可分別低至18 nM和0.37 μM,并具有很好的特異性。此外,該方法不僅可有效對單細(xì)胞水平內(nèi)的ATP含量變化進(jìn)行動態(tài)監(jiān)測,還可準(zhǔn)確分析低血鈉患者中的血漿鈉含量。
上述論文武漢科技大學(xué)為第一完成單位,李誠予副教授為第一作者兼通訊作者,武漢大學(xué)唐宏武教授為共同通訊作者,武漢大學(xué)鄭貝博士為共同第一作者。該工作得到國家自然科學(xué)基金(21904102, 81772256和21827808)的支持。
原文標(biāo)題:武漢科技大學(xué)構(gòu)建新型CRISPR/Cas12a生物傳感器,幫助實(shí)現(xiàn)非核酸目標(biāo)物的轉(zhuǎn)導(dǎo)
文章出處:【微信公眾號:微流控】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
責(zé)任編輯:haq
-
傳感器
+關(guān)注
關(guān)注
2550文章
51039瀏覽量
753092 -
芯片
+關(guān)注
關(guān)注
455文章
50721瀏覽量
423170 -
生物傳感器
+關(guān)注
關(guān)注
12文章
368瀏覽量
37367
原文標(biāo)題:武漢科技大學(xué)構(gòu)建新型CRISPR/Cas12a生物傳感器,幫助實(shí)現(xiàn)非核酸目標(biāo)物的轉(zhuǎn)導(dǎo)
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
生物傳感器:科技前沿的生物監(jiān)測利器
中國科學(xué)院大學(xué):實(shí)現(xiàn)可再生高靈敏度生物傳感器新進(jìn)展
上海大學(xué):研發(fā)電化學(xué)生物傳感器檢測神經(jīng)系統(tǒng)疾病生物標(biāo)志物
Aigtek功率放大器如何幫助納米電子生物傳感器更好的研發(fā)和生產(chǎn)
電化學(xué)生物傳感器在生物檢測領(lǐng)域的顯著優(yōu)勢
三郡科技:電化學(xué)生物傳感器電極與生物芯片的異同
便攜快速檢測的電化學(xué)生物傳感器:顛覆性變革生物檢測方式
中國科學(xué)院在薄膜熒光傳感器研究方面取得進(jìn)展,美國為F-22升級新傳感器

綜述:基于間質(zhì)液的可穿戴生物傳感器研究和應(yīng)用進(jìn)展
安泰ATA-2161高壓放大器在生物傳感器研究中的應(yīng)用
?科普|生物傳感器
天府錦城實(shí)驗室在生物傳感與蛋白質(zhì)測序領(lǐng)域取得重要進(jìn)展

利用太赫茲超構(gòu)表面開發(fā)一款革命性的生物傳感器
武漢大學(xué)1052頁P(yáng)PT帶你全面了解傳感器技術(shù)(史上最全!)






 武漢大學(xué)在生物傳感器構(gòu)建方面取得進(jìn)展
武漢大學(xué)在生物傳感器構(gòu)建方面取得進(jìn)展










評論