近年來各方對 AI 制藥領域的關注度明顯上升,資本持續注入,藥企研發力度逐步增強,AI 制藥相關技術的迭代速度也明顯加快。可以預見人工智能技術正逐步從多方面滲透到生物制藥領域,并有機會為行業帶來重大變革。針對這些趨勢,CB Insights 中國對 AI 制藥領域進行了全面梳理。
資本市場熱度不減
AI 制藥行業受到廣泛關注,資本市場保持火熱。
2020 年, AI 制藥領域在資本市場獲得了很高的關注度,對于 AI 技術在藥物研發中的真正作用也引發了一系列討論。從供給端看,隨著基因檢測技術的進步,各種藥物研發數據的不斷積累以及計算機硬件設備與人工智能算法的改良使得 AI 技術在生物制藥領域的發展獲得了良好的條件。而在需求端,傳統生物制藥企業在進行新藥研發時長期存在的研發周期長、失敗率高、成本高等痛點也給 AI 制藥行業帶來了巨大的增量。這些來自供需兩端的驅動力也真正助推了這場資本熱潮。
圖 | 融資金額及數量
在生命大健康領域,與 AI 技術相關的應用融資逐步上升。
據 CB Insights 數據統計,2015 年到 2020 年期間,AI 技術在生命大健康領域的應用融資逐步攀升。自 2020 年 3 月以來,受益于投資機構對于人工智能技術應用于藥物研發賽道的關注,共有 11 家 AI 制藥公司完成了 1 億美元以上的融資。
圖 | 融資地區分布
美國是 AI 制藥領域融資交易的主要地區,中國緊隨其后。
從地區分布上看,美國仍然占據了融資交易的主要份額,近 5 年來在 AI 制藥領域有 50.6% 的融資交易發生在美國。中國以 9.4% 的比例緊隨其后,成為了除美國外最大的新興市場,超越了英國、韓國、以色列等傳統科技強國。這也展現了中國市場在新興科技領域發展的巨大的潛力。在 AI 制藥這類新興賽道上越來越多中國企業的身影涌現。
圖 | 融資輪次統計
在融資輪次上,AI 在醫療領域各階段的融資輪次比例正在發生改變,種子輪企業占比逐年降低。
CB Insights 統計在 2015 年融資輪次為種子輪的企業占比為 51% 而 2020 年這一比例下降到了 30%。目前這一領域的絕大多數公司仍然處于早期階段,但仍有少數頭部公司已經初露鋒芒。
根據美國 FDA 的統計數據,目前經過 FDA 審批通過的 AI 產品共計 41 款。中國也有 6 款 AI 產品獲得國家醫療器械三類證。同樣在 AI 制藥這一細分領域也不乏 Schrodinger、 Insilico Medicine 、BenevolentAI、晶泰科技等明星公司的身影。 技術確定性探討
AI 制藥行業是人工智能技術和生物制藥領域的深度交叉。
由于需要信息技術人才與生物制藥人才的協同創新,這無疑增加了 AI 制藥領域的創新門檻。在人才儲備上,AI 制藥企業一方面會儲備計算所需要的計算生物學、計算化學、AI 算法設計等背景的人才,另一方面也會廣泛引入藥劑學、藥物臨床試驗和臨床醫學等方面的人才。同時,擁有算法和藥物研發復合背景的人才更是成為市場上的稀缺資源。 在技術層面,如何理解 AI 制藥結果的確定性正成為判斷 AI 制藥公司成長潛力的關鍵部分。
人工智能技術本身更像一個”黑箱“,許多技術細節難以解釋,這與生物制藥這一具有高嚴謹性高確定性要求的領域產生了矛盾。對于 AI 制藥技術來說,要判斷其確定性,除了要追蹤其前期模型結果產出環節的歷史精準度,后期對于決策證據的可靠性論證以及對結果的確定性驗證是更為關鍵的部分。目前人工智能的各種細分技術例如監督學習、無監督學習、增強學習等已經深入到藥物研發的各個環節。針對不同方向的各類模型準確性判定方式也略有差異。
圖 | AI 制藥技術分類
一般而言,用于 AI 制藥的深度神經網絡通常含有輸入層、隱含層和輸出層三層結構。
生物數據首先需要轉換為輸入值數組,然后這些值被輸入隱藏層運算。深度神經網絡的其中一個挑戰便是定義網絡的深度和寬度即隱藏層和每層節點的數量。一層中的每個節點從前一層的所有節點獲取輸入信息,然后對輸入信息進行數學變換,之后再進行正向反饋。最終在輸出層輸出輸入數據的最終演算結果。
其中所涉及的非線性轉換的數量越多,對最高級別層的解釋也就變的越困難。此類網絡目前主要是通過不斷迭代輸入值數組,根據輸入和輸出結果之間的關系來評估模型特征和權重。通過歸因分數、相關性系數或權重共享系數等方法給出特征重要性評分。
圖 | 兩類深度學習網絡結構
另外一種深度神經網絡模型則選擇用可見層取代隱藏層。
這類算法主要基于統計學和生物信息學的知識圖譜,利用生物學底層邏輯將運算串聯起來,使得每一層的數據產生機理得到解釋。這一類型的可見層中往往采用基因本體論(Gene Ontology)等生物信息學相關網絡結構來定義輸入層和輸出層的連接方式,因此輸出層的計算可以通過網絡回溯。
2020 年 Kuenzi 等人便使用從基因本體論衍生的層次結構的深度神經網絡對腫瘤對藥物的敏感性進行了建模,取得了重大突破。 這兩種類別的深度神經網絡模型在確定性判斷上是有差異的。
對于許多基礎的生物問題,第一類深度神經網絡通常可以實現很高的預測精度,但很難將預測的方式和原因結合起來,而第二類模型則可以有效改善這一問題。
同樣,受限于現階段理論研究的邊界,第二類模型往往在模型深度上受限,或者需要極高的算力支撐。在確定性上,第二類模型理論上可以通過數理邏輯自證,而對于第一類深度神經網絡模型,由于隱藏層的內部運算是相對未知的所以很難進行數據溯源,模型輸出結果的確定性通常采用后期實驗驗證的方式來證明。
整體來說目前 AI 制藥驗證的鏈條相對較長,因此在未來建立高通量高效的實驗評價體系對 AI 制藥企業來說尤為重要。 數據、算力和算法是目前 AI 制藥企業的三大技術核心。
數據方面,原始數據通常來自三個方面,公開數據集例如 PubChem、ChEMBL 等、與藥企合作獲得的研發數據集、企業自身研發積累的數據集。原始數據會經過多輪數據清洗最終獲得可以用來建模的數據。
算力方面,GPU 云計算資源等為 AI 制藥企業提供了重要的計算支撐。數據和算力是 AI 制藥企業的基石,基于此 AI 制藥企業可以搭建出自己的底層知識圖譜,并形成其行業壁壘之一。
目前藥物研發新基建還處于早期搭建的階段,但隨著各大數據庫的開源以及云計算平臺的普及,數據和算力已經逐漸不再成為制約其發展的決定性因素。 對于 AI 制藥企業來說更為核心的壁壘是算法,其核心創新點在于建模的精度和產生新信息的能力。
深度學習的迭代算法可以有效地整合模板建模和自由建模,進而開發出動態可迭代的特異性約束條件,從而提高建模精度。另一類由自監督學習等方法產生的共進化模型,則能夠從無到有地產生出新的生物學信息,拓寬人類的知識邊界。這些創新優勢是其它傳統制藥手段難以達到的。
透過 AI 精確的建模和新的生物學相關信息的產生可以加深我們對人體復雜生理生化模型的理解,進而在藥物發現階段即可與臨床試驗相結合,找到合適的分子。通過前期低成本的高效的AI 賦能來降低后期臨床試驗的成本和失敗概率,從根本上改變臨床試驗階段投入大成功率低的現象。
AI 技術賦能生物醫藥
從制藥的流程看,AI 技術已經在多個環節找到了適合自己的應用場景,并發揮出巨大潛力。
從臨床前藥物發現階段到藥物研發后期臨床試驗階段,AI 技術已經滲透到藥物研發諸多環節。例如基準化合物設計、預測疾病靶點、預測信號通路、預測成藥靶點、確認新靶點、硅化合物庫設計、預測藥物結構與活性的關系、預測 ADMET 性質、優化藥物反應試驗、選擇受試人群、藥物警戒和轉錄組數據查詢等。
現階段 AI 在藥物研發需要大數據分析和高通量測試的階段優勢最為明顯。例如在根據海量文獻篩選靶點、專利追蹤、批量性質預測等方面,藥企便可以通過使用人工智能相關技術降低大量制藥成本。
圖 | 藥物研發各環節中 AI 的作用(來源:Drug Discovery Today,CB Insights 中國整理) 不斷取得的突破性進展也給 AI 制藥的未來帶來了空前的想象力。
人工智能技術與生物制藥領域的結合不僅將藥物發現、臨床前研究的時間縮短接近 40% 還可以節約臨床試驗階段約 50%-60% 的時間。每年近 260 億美金的化合物篩選成本和約 280 億美金的臨床實驗費用也可以通過 AI 制藥技術節省出來。面對創新藥研發領域日趨激烈的同質化競爭,AI 技術在藥物研發過程中帶來的諸多底層創新無疑也展現出了巨大的價值。
生物制藥企業與 AI 企業的合作
基于AI 技術的特有優勢,許多大型藥企開始在這一領域積極布局。
部分國際藥企早早的便開始和人工智能企業展開了合作。其中默沙東和葛蘭素史克與 AI 平臺的合作最早也最為頻繁,其次是拜耳(Bayer),武田制藥(Takeda Pharmaceutical),阿斯利康(AstraZeneca),賽諾菲(Sanofi)和羅氏(Roche)。
2012 年,默沙東首次與 Numerate 公司合作開展心血管疾病的研究。葛蘭素史克自 2012 年以來已經與 Insilico Medicine、Exscientia、Deep Intelligent Pharma 和 Cloud Pharmaceutical 四家 AI 平臺企業建立了合作。 在所披露的合作當中,神經退行性疾病和癌癥方向是目前合作的兩大熱門領域,心血管以及胃腸道疾病領域也有所涉獵。
楊森制藥與 Benevolent AI 合作,在帕金森氏癥領域展開小分子化合物研究。公司主要利用 AI 系統 JACS 從論文、臨床試驗中提取數據,提出新假設從而加速新藥研發。
GNS Healthcare 與 Gene tech 合作利用 GNS 分析平臺在腫瘤學方向展開研究。他們將大數據、機器學習和仿真技術結合起來判斷疾病預后效果,從而輔助醫療供應商進行市場決策。
圖 | 藥企與 AI 企業的合作
隨著大型藥企與 AI 公司合作的展開,人工智能技術在醫療服務領域的嵌入也越來越深。
在 CB Insights 整理的 100 家生命大健康領域相關的 AI 初創公司當中,AI 制藥公司占據了相當大的比重,初創公司漸漸涌現。
圖 | 100 家 AI 在生命大健康領域的初創公司
2020 年科技巨頭谷歌旗下的 Deepmind 在 AI 藥物研發領域取得重大進展,更是進一步點燃了 AI 制藥領域的研發熱情,各路資本紛涌而至。
CB Insights 中國整理了 AI 制藥領域 50 大核心投資方,這其中不僅有許多耳熟能詳的明星基金也可以發現大型藥企的身影。
核心 VC/PE 基金重點分布在美國(舊金山、馬薩諸塞州、紐約)、中國(上海、北京)、加拿大、英國、比利時、瑞士等國家和地區。這也從側面展現出這些地區雄厚的資本基礎和巨大的創新活力,為 AI 制藥初創公司的落地提供了新選擇。
圖 | AI 制藥領域50大核心投資方
在技術和資本的雙重推力下,近年來在藥物研發各細分環節中誕生了許多各具特色的 AI 制藥初創公司。
在信息搜集與整合、靶點篩選、藥物設計合成、藥物有效性預測以及臨床試驗數據優化等細分環節中,AI 制藥初創公司正發揮著越來越重要的作用。
蓬勃發展的初創企業正在為 AI 制藥行業帶來全新的視角和分析工具。例如中國的基于真實世界數據解決方案研究的領星醫學,基于多組學數據挖掘的普瑞基準等新興公司,都在嘗試利用人工智能技術解答那些醫學中最本質的問題,從而賦能到新藥的研發。
圖 | AI 制藥初創企業分類
除卻全球市場的火熱,AI 制藥在中國也迎來了發展良機,有望成為改變生物制藥產業的新機遇。
中國互聯網巨頭們紛紛開始向 AI 制藥領域進軍。
騰訊早在 2015 年和 2018 年便參與了目前中國 AI 制藥頭部企業之一晶泰科技的 A 輪及 B 輪融資。2020 年更是重點打造了“云深智藥”,將 AI 藥物研發正式列入企業版圖。
華為在醫療領域布局了華為云 EIHealth,計劃今年進一步在 AI 藥物研發領域展開布局。
阿里巴巴旗下的阿里云與全球健康藥物研發中心合作,開發 AI 藥物研發和大數據平臺,并針對 SARS/MERS 等冠狀病毒的藥物研發進行數據挖掘。
百度 2020 年 9 月成立百圖生科進軍 AI 制藥領域。其 LinearFold 算法可將新冠病毒的全基因組二級結構預測從 55 分鐘縮短至 27 秒,提速 120 倍。
字節跳動成立了專門負責大健康業務的極光部門, AI Lab 位于北京、上海、美國三地的團隊也正式開始招攬 AI 制藥領域人才。
圖 | 中國互聯網巨頭在 AI 制藥領域的布局
中國本土資本也逐步在 AI 制藥領域展開布局。
除傳統 VC/PE 外,大型藥企和互聯網企業也紛紛加入此次賽道投資。中國資本啟明創投、百度風投、創新工場、騰訊、藥明康德、恒瑞醫藥等近年來在 AI 制藥行業積極布局,投資額度逐年增加,掀起了一陣投資熱潮。
這場熱潮背后的原因在于 AI 技術的突破有機會解決生物制藥領域很多內生問題,甚至可以從底層改變整個新藥發現的方法論,前景是不可限量的。由于 AI 技術從某種程度上帶有技術顛覆性基因,所以只要找到了適合其發展的應用場景,往往就能釋放出巨大的能量。資本方也正是看到了這一點。 從技術發展角度看去,近年來 AI 技術的突破與生命科學大數據的發展相輔相成。
深度學習算法的進步讓端到端的結構預測在硅基中實現;云計算和超算技術帶來的算力提升也解決了計算蛋白質結構之間相互作用的難題;基因測序技術產生的大量數據積累成為了 AI 算法很好的數據源;小分子藥相對結構化的化學結構很適用于數據建模,也進一步促進了 AI 在藥物結構預測領域的發展。 從商業角度探究,AI 制藥技術有機會引起一場顛覆式的制藥革命。
在完成一定量的技術積累之后,理論上用 AI 賦能的新藥發現平臺可以持續性地開發新藥,這將徹底打破傳統的新藥研發模式,解決藥物研發時間長,成功率低的問題。
AI 技術有助于重塑人們對生命科學的理解,引導幫助生物學家跳出人類固有思維框架的限制,促進做出真正的 First-in-Class 的藥物,AI 制藥企業也因此具備很高的商業前景和社會價值。 在政策上,創新是時代的主旋律,對創新的政策扶持給 AI 制藥企業帶來了機會。
近年來中國出臺的一系列政策例如帶量采購、一致性評價等不斷給仿制藥企業施壓,這也反過來促進了本土藥企關注創新。
大量中國本土的仿制藥企業需要進行創新轉型,天然具備賦能基因的 AI 制藥企業是他們極佳的合作對象。藥企在藥物制劑、藥物遞送、處方設計和研發臨床差異化的改良性新藥等方面都有著迫切的創新需要。可以說市場的大環境對新技術的需求是明確的,這些需求無疑給 AI 制藥領域帶來了無限機會。
AI 制藥初創企業的商業化探索
在創新環境之下,AI 制藥企業正逐步探索自己的商業化之路。
AI 制藥技術的難點在于底層知識圖譜的構建、模型的訓練、以及高性能計算設施提供的算力支撐。這就使得 AI 制藥企業在前期需要進行大量的技術積累,在早期商業化進程方面稍顯吃力。
為解決這一問題,AI 制藥企業往往會先選擇從藥物研發的某一個細分階段切入再逐漸擴大布局。目前大多數公司選擇的是從藥物發現階段進行切入,在未來逐漸布局到臨床階段也有少部分公司選擇從臨床階段切入,之后結合臨床實際布局到臨床前階段。 在盈利模式方面,部分 AI 制藥公司已經探索出自己的發展方向。
和大型藥企合作,基于業績付費是目前 AI 制藥公司主要的盈利模式。一部分生物信息學背景的 AI 制藥公司從靶點選擇開始便與藥企進行深度綁定,在后續的臨床試驗過程中持續保持合作。藥企通過 AI 制藥公司節約了靶點篩選的時間,降低了晶體合成成本,挺高了新藥的臨床響應率,增加了藥物研發成功率。AI 制藥企業也同樣獲得了穩定的現金流和強力的產業背書,這也有助于其進一步增強研發,形成正向循環。
目前商業化步伐最快的公司是美國上市企業 Schrodinger。
它于 2020 年 2 月在納斯達克上市,目前市值約 60 億美元。Schrodinger 的商業模式包含軟件業務和藥物研發業務兩部分。 其中軟件業務采用 license 模式,2019 年營收占比為 28%。
2019 年 Schrodinger 的軟件客戶包含全球前 20 大藥企及超 1350 家科研機構。業務遍及美國、歐洲、日本、印度、中國、韓國等。2019 年年合同額 ACV (annual contract value)超 10 萬美元客戶約 131 家,超 100 萬美元的客戶約 10 家。 Schrodinger 的藥物研發業務包含與外部的合作研發和自主研發兩種類型。
目前有兩款 Schrodinger 參與合作研發的新藥已經獲得 FDA 批準。Schrodinger 與外部合作采用公司與合作方共同成立企業,Schrodinger 占股權的形式。其中 Morphic 和 Relay 兩家公司已經 IPO 上市。這種模式的收入來源包括研究費用、未來的商業化里程碑費用、商業許可費等。在自主研發方面,Schrodinger 已經披露靶點的項目有 5 個。在靶點的選擇上,公司會對 1000 個靶點進行優先級篩選,從腫瘤領域入手,尋找可實現結構模擬,生物學原理可行,治療市場大的靶點進行重點開發。 Schrodinger 上市以來受到資本市場的熱捧,與其商業化進程走在各類 AI 制藥公司前列密不可分。其行業發展經驗同樣受到各類 AI 制藥初創企業的關注。
目前 AI 制藥賽道是一片廣闊藍海,機會與挑戰并存,利益和風險同擔。對于各類初創企業來說,除了要加強創新,確立好自己的核心技術壁壘,盡早的進行商業化布局,利用好先發優勢也是尤為重要的一環。
AI制藥行業重點公司介紹
Schrodinger
總部位于紐約的 Schrodinger 公司于 2020 年 2 月在納斯達克上市,目前市值約 60 億美元。公司從創立至今已經發布了 7 項關鍵技術平臺。包含可對化合物進行高通量篩選的 Glide 、Prime 全集成蛋白結構預測程序、WaterMap 首個計算蛋白結合水位置和能量的方法、FEP+ 首個精確預測具有共同核心的不同分子的不同親和力的方法 、LiveDesign 協同蛋白設計的平臺以及與冷凍電鏡研發相關的 Cyro-EM Initiative。 Schrodinger 還和多家機構或藥企達成合作,深度參與藥物研發。與風投機構 Atlas Venture 共同創立 Nimbus Therapeutics,與生物科技公司 Agios 合作且兩款新藥獲 FDA 批準,與賽諾菲 、武田制藥等大藥企合作加速新藥研發過程,與 SPARC 合作加速神經退行性疾病新藥研發,與藥明康德合作成立 Faxian Therapeutics 藥物研發公司。
圖 | Schrodinger 發展歷程
Insilico Medicine
Insilico Medicine 的核心技術是開發一系列生成對抗網絡(GANs)和增強學習方法(Reinforcement Learning)來識別蛋白質靶點,從而生成具有特定屬性的分子結構。該公司在 2019 年 9 月完成了 3700 萬美元的 B 輪融資,其中由啟明創投領投,斯道資本、F-Prime Capital、禮來亞洲基金、創新工場、百度風投等其他投資方跟投。
2020 年 1 月,輝瑞也與 Insilico Medicine 達成合作,旨在利用 Insilico Medicine 的機器學習技術和專有的 Pandomics 平臺,為多種疾病尋找潛在的治療靶點。 2021 年 Insilico Medicine 利用 AI 技術成功發現一種全新的用于治療特發性肺纖維化(IPF) 的臨床候選藥物,并成功通過動物模型實驗驗證,預計年底進入臨床。整個過程僅僅耗時 18 個月花費 260 萬美元,展現了其 AI 技術的巨大潛力。
圖 | Insilico Medicine 服務流程
BenevolentAI
BenevolentAI 是 2017 年 CB Insights 評選的全球人工智能百強公司。公司核心技術是 JACS 人工智能系統,JACS 可以在運算中從論文、臨床試驗中提取大量的數據,提取推動藥物研發的知識,提出新的可被驗證的假設,加速新藥研發。
近年來與諸多藥企達成了合作例如與楊森制藥合作利用人工智能技術來評估小分子化合物在臨床的潛力,特別是在帕金森氏癥領域、與阿斯利康合作尋找治療慢性腎病和特發性肺纖維化的新藥,與諾華合作開發癌癥相關的藥物。 2019年 8 月 Benevolent AI 與 Neuropore Therapies 合作研究通過人工智能鑒定的與進行性退行性疾病有關的分子靶點。Benevolent AI 自身也在開發有關于肌萎縮側索硬化(ALS)的相關藥物。
圖 | BenevolentAI 程序
Atomwise
Atomwise 是藥物研發與人工智能結合領域的代表性公司,是由 Y Combinator和 Khosla Ventures 投資的舊金山創業公司,目前已與禮來、默沙東、拜耳、輝瑞和艾伯維等多家大型醫藥公司合作。
Atomwise 的核心技術是使用神經網絡構造出分子化合物的 3D 模型并模擬生化反應,預測化合物與靶蛋白之間的特異性結合。
Atomwise 與禮來簽訂了高達 5.6 億美元的 AI 驅動藥物研發項目合作協議,旨在幫助禮來對特定疾病快速尋找到新的藥物分子。2019 年 9 月,Atomwise 進軍亞洲市場,與豪森藥業達成合作,雙方在多個治療領域針對 11 個未公開靶標設計和發現潛在的候選藥物。
圖 | Atomwise 研發領域分布占比
Exscientia
英國 AI 藥物發現公司 Exscientia 成立于 2012 年,目前已與葛蘭素史克和羅氏建立了常規研究合作項目。2019 年 4 月,Excientia 向葛蘭素史克交付了第一個通過人工智能發現的候選藥物,這是一個治療慢性阻塞性肺病(COPD)的潛在療法。
除此之外,Exscientia 還與賽諾菲合作開發了有關代謝性疾病的療法;與新基公司合作開發了針對癌癥和自身免疫性疾病的療法。2020 年 1 月,拜耳宣布與 Exscientia 在心血管疾病和腫瘤藥物研發方向展開合作,項目金額達 2.4 億歐元。
在融資方面,Exscientia 在 2019 年 1 月完成了 2500 萬美元的B輪投資,該輪融資由新基公司、GT Healthcare Capital 以及 Evotec 共同參與完成。
圖 | Exscientia 服務流程
OWKIN
總部位于紐約的 OWKIN 成立于 2016 年。OWKIN 主要利用 Federated learning ( 一種在保護隱私的同時使用敏感用戶數據訓練 AI 的新興方法) 為制藥公司提供藥物研發服務,該技術最早是由谷歌在 2016 年提出的。
公司的核心機器學習平臺 Owkin Socrates 能夠整合生物醫學圖像、基因組學和臨床數據,通過機器學習和深度學習算法,將臨床數據轉化為預測模型,為的是讓醫學專家們零門檻地使用人工智能技術,完成前沿的醫學研究、藥品研發和臨床診治。 谷歌旗下風投基金 GV 參與了對 OWKIN 的 A 輪融資。目前,OWKIN 已與羅氏、益普生、安進等知名藥企達成合作,未來 OWKIN 將深度布局從患者數據中找到與疾病相關的生物標志物這一細分領域。
圖 | OWKIN 業務布局
晶泰科技
晶泰科技致力于生物醫藥的新基建建設,旨在從數字化和智能化兩方面進行技術研發。晶泰科技主要的業務是在臨床前藥物研發階段,對藥物晶型和固相進行預測,從疾病靶點的結構出發進行先導化合物設計等。
晶泰科技核心技術是將計算化學和深度學習相融合,以第一性原理為基礎不斷提高模型精度,以數據為驅動力搜索更多的藥物化學空間。另外晶泰科技的算力資源深厚,其多云架構,可以調度超過百萬的 CPU 核心和 GPU 資源。 2020 年 9 月晶泰科技宣布完成 3.188 億美元的 C 輪融資,創 AI 制藥領域融資紀錄。本輪投資由軟銀愿景基金、人保資本、晨興資本領投, 展現出了資本市場對中國 AI 制藥企業的巨大熱情。
圖 | 晶泰科技
云深智藥
云深智藥是騰訊旗下的 AI 制藥平臺,該平臺覆蓋了臨床前藥物發現的全過程,致力于深度服務藥物研發人員。
其平臺的虛擬篩選模塊首次將元學習和深度神經網絡算法用于基于配體的藥物設計(ligand-based drug design,LBDD)任務。目前該算法的預測精度已經突破業界標準,將預測活性與實驗測量活性的相關性中位數提升到 0.42。另外云深智藥平臺的藥物小分子 ADMET 屬性預測結果準確度比學術界最優模型提高 3%~11%,自研算法精度超過現有商業軟件近 37%。受益于騰訊的資源支撐,云深智藥近年來已經逐步在 AI 制藥初創企業中確立了自己的優勢。
圖 | 云深智藥平臺架構
星藥科技
星藥科技成立于 2019 年,是中國新興的 AI 制藥公司之一,其專注于從苗頭化合物設計到臨床前候選藥物篩選階段的藥物研發。創始人李成濤獲麻省理工學院計算機博士學位,團隊成員擁有成功主導新藥項目經 FDA 批準上市的經驗,從創立初期便致力于打造綜合型的人才體系。
豐厚的人才儲備也為星藥科技帶來了多項技術突破。目前星藥科技已經完成了若干客戶方案交付,其自主研發的算法模型在諸多環節表現優異,權威機構驗證顯示,星藥自有藥物活性評測模塊的篩選命中率較傳統方式可提高十余倍。
鑒于其在產品化方面優異的表現,星藥科技在一年多的時間內獲得四輪融資,資金高達數千萬美元。投資方包含高榕資本、五源資本、DCM 中國、源碼資本、BAI 資本、紅點中國等知名機構。未來星藥科技將重點提高研發團隊規模和建設相關生化檢測實驗室,最終打造藥物生成、篩選、評價和檢測的自動化閉環,加速市場落地。
圖 | 星藥科技平臺架構
普瑞基準
不同于多數 AI 制藥企業致力于藥物發現,普瑞基準基于自身的組學數據挖掘系統,重點關注“通過深挖生物學機制,幫助藥企研究并設計新藥管線的開發策略”,通過提供 AI 支持的新型生物信息和轉化醫學服務,成為腫瘤新藥研發企業的戰略伙伴。
過去 10 年,全球新藥研發領域的回報率快速下降,其中一個重要原因就是對疾病的生物學機制理解不足,許多新藥研發項目遭遇了后期失敗。與此同時,由于對機制理解不足,大批中國創新藥研發企業被迫在有限的已驗證靶點上展開激烈的同質化競爭。普瑞基準通過 AI 算法,深化對疾病及治療相關生物機制的理解,為創新藥研發提供關鍵決策支持,從而提升新藥研發的成功率,或幫助形成差異化優勢。 普瑞基準自主研發了 AI 驅動的面向癌癥藥物研發的大數據系統(AIBERT),專注于“創新藥研發的深水區”,解決四大核心問題,即:潛力靶點的評估,適應癥的選擇,生物標志物的發現,耐藥機制的研究(以及相關的藥物聯用方案)。目前AIBERT 平臺整合了 PB 級別的多組學數據資源,包括大量中國患者數據,特別強調數據的完整性(組學數據與臨床數據的匹配)、規范性和豐富性(高維數據)。AIBERT 的算法設計強調“可解釋性”,結果指向性高,在新藥研發決策、藥物差異化定位等方面達到國際領先水平。尤其在創新的生物標志物研究方面,AIBERT幫助多個藥物提升應答率、擴大適用人群,贏得藥企的廣泛認可。 普瑞基準立足多組學與數據挖掘,目前已和國內外多家知名藥企在轉化醫學和臨床開發領域形成深度合作,包括恒瑞醫藥、阿斯利康、石藥集團、再鼎醫藥等。2020 年公司完成了知名投資機構(創新工場、麥星投資、百度風投)領投的兩輪融資,已成為中國 AI 制藥領域的新星。
圖 | 普瑞基準 AIBERT 平臺
編輯:lyn
-
AI
+關注
關注
87文章
31155瀏覽量
269493 -
人工智能
+關注
關注
1792文章
47442瀏覽量
239008
原文標題:AI 制藥行業專題報告——打開 AI 制藥黑匣子,CB Insights 深度剖析 AI 制藥領域商業機會
文章出處:【微信號:deeptechchina,微信公眾號:deeptechchina】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
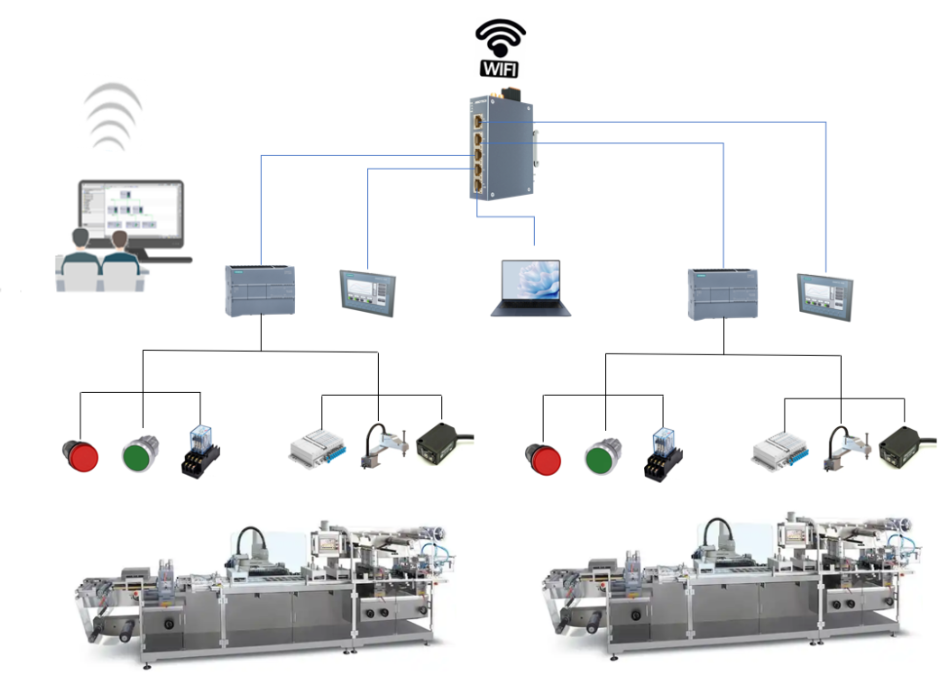
安全、便捷、效率高,明達邊緣計算網關助力制藥裝備企業遠程調機
RISC-V在AI領域的發展前景怎么樣?
AI大模型與深度學習的關系
AI for Science:人工智能驅動科學創新》第4章-AI與生命科學讀后感
《AI for Science:人工智能驅動科學創新》第二章AI for Science的技術支撐學習心得
點成生物攜手寫真化學共赴青島全國制藥機械博覽會

賽諾菲攜手Formation Bio與OpenAI,共促AI藥物開發
高通攜手微軟進軍AI PC,Wintel聯盟有變?

risc-v多核芯片在AI方面的應用
微軟21億美元投資法國AI公司Mistral AI
制藥裝備企業如何實現制粒機遠程監控和運維管理

PLC遠程監控在制藥行業的應用





 基于AI制藥CBInsights深度剖析AI制藥領域的商業機會與其重點公司介紹
基于AI制藥CBInsights深度剖析AI制藥領域的商業機會與其重點公司介紹










評論