獨立研究是驗證 Qorvo Omina 抗原檢測應用質量的重要步驟
中國 北京,2021年8月4日——移動應用、基礎設施與航空航天、國防應用中 RF 解決方案的領先供應商 Qorvo?, Inc.(納斯達克代碼:QRVO)宣布,其 Omnia? SARS-CoV-2 抗原檢測平臺已圓滿完成 NIH 快速診斷提速 (RADxSM) 計劃的一個重要里程碑。亞特蘭大微系統工程現場護理技術中心 (ACME-POCT) 完成了兩項獨立研究:一項成人研究和一項兒童研究,驗證了 Qorvo Omnia 抗原檢測的 SARS-CoV-2 低檢測限 (LOD) 和高特異性/靈敏度。
成人和兒童研究分別將該平臺的性能與 Roche cobas 6800(1800 NDU/ml,使用 FDA 參考反射板)和 Hologic Panther (600 NDU/ml) RT-PCR 系統進行了比較。 這兩項研究表明,對成人的靈敏度/特異性為 100%,對兒童的靈敏度和特異性為 83% 和 100%。 在 Qorvo Omnia 抗原檢測平臺中檢測為陰性的三個兒童樣本在 Hologic 系統中的循環閾值 (Ct) 檢測值大于 38,表明樣本中的病毒載量非常低。該研究的靈敏度和特異性完全低于這些水平。 總的來說,研究人員發現 Qorvo Omnia 平臺設計直觀且簡單易用,與高靈敏度的分子檢測系統相比,可快速獲得檢測結果,在樣本收集后 20 分鐘內即可得到結果。
Qorvo Biotechnologies 總裁 James Klein 表示:“獨立的外部研究是向市場宣傳 Omnia 抗原檢測能力的關鍵步驟,也是 Qorvo Omnia 診斷平臺發展過程中的重要里程碑。我們對這些研究的結果和研究員反饋感到滿意。
此項目由 NIH“快速診斷提速”(RADxSM) 計劃提供部分資助,并由美國國立衛生研究院的美國國家生物醫學影像與生物工程研究所提供聯邦基金。當前合同 (75N92021C00008) 由美國生物醫學高級研究和發展局從公共衛生和社會服務應急基金中撥款出資。該管理局隸屬于美國衛生和公眾服務部應急準備與反應助理部長 HHS 辦公室。
2021 年 4 月,美國食品和藥物管理局 (FDA) 為 Qorvo Omnia 抗原檢測頒布了緊急使用授權 (EUA)。該檢測被授權用于:在癥狀發作前 6 天內,由醫療健康提供商進行定性檢測,確定疑似 COVID-19 患者鼻拭子標本中是否存在 SARS-CoV-2 病毒的核衣殼病毒抗原。
Qorvo Omnia 平臺通過使用高頻體聲波 (BAW) 傳感器實現 SARS-CoV-2 (COVID-19) 抗原快速檢測,體現出診斷測試能力的重大轉變。BAW 傳感器技術可達到近似于分子檢測能力的低 LOD 水平。
Qorvo Omnia SARS-CoV-2 抗原檢測尚未獲得 FDA 許可或批準。經 FDA 根據“緊急使用授權”條例授權,只能通過《1988年臨床實驗室改進修正案》(CLIA),42 U.S.C. §263a 認證的實驗室執行中等或高度復雜的測試。該項檢測僅被授權用于檢測來自 SARS-CoV-2 的蛋白質,不適用于任何其他病毒或病原體。獲得 EUA 授權的測試僅授權用于聲明的期間,即根據“緊急使用授權”法案第 564(b)(1) 節,21 U.S.C. § 360bbb-3(b)(1),有理由授權緊急使用體外診斷測試來檢測和/或診斷 COVID-19 的情況,除非該授權提前終止或撤銷。
-
傳感器
+關注
關注
2550文章
51046瀏覽量
753133 -
Qorvo
+關注
關注
17文章
641瀏覽量
77426
發布評論請先 登錄
相關推薦
華為云云原生中間件 DCS?&?DMS?通過中國信通院與全球 IPv6 測試中心雙重能力檢測

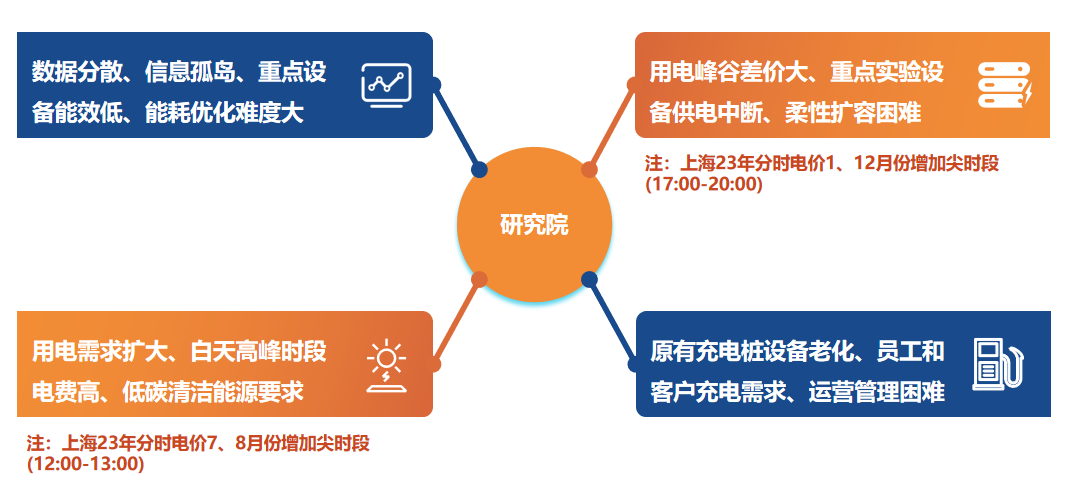
上海某研究院園區改造微電網智慧能源管理平臺
天馬與武進南大未來技術創新研究院達成戰略合作
藍思科技將新增昆山創新研究院,重點服務蘋果
仁懋電子&amp;深圳先進材料研究院孫院長就芯片封裝行業友好交流

羅克韋爾自動化受邀出席聯合國訓練研究所繁榮聯盟上海氣候周研究院項目啟動儀式

華索科技入選深圳比亞迪研究院碳化硅襯底加工項目設備供應鏈
長沙北斗研究院總部基地正式奠基
達實智能正式簽約威高(上海)國際研究院項目!
上海浦東軟件園榮獲SAP中國研究院“Bamboo Award”2023獎項

九聯科技與中國信息通信研究院攜手簽署合作框架協議!
浙江圖靈算力研究院向知存科技頒發“年度最具影響力企業獎”
思看智能三維數字化掃描檢測企業研究院被認定為省級企業研究院!





 Qorvo Biotechnologies Omnia? SARS-CoV-2抗原檢測平臺通過了美國國立衛生研究院(NIH)資助研究項目的驗證
Qorvo Biotechnologies Omnia? SARS-CoV-2抗原檢測平臺通過了美國國立衛生研究院(NIH)資助研究項目的驗證












評論