01
研究背景
五元雜環化合物,如二氫吡唑及其不飽和對應吡唑,廣泛存在于藥理活性分子、農用化學品、天然產物和合成配體中。通過光催化分子內加成氮中心自由基來合成氮雜環具有大量優點。盡管如此,由于大多數N-H鍵的高鍵解離自由能 (BDFE),直接從N-H鍵產生以氮為中心的自由基具有挑戰。通過自然光合作用過程中的質子耦合電子轉移 (PCET) 過程開發了一種結合堿和光催化劑的氧化去質子化電子轉移策略。吖啶鹽及基于釕和銥的過渡金屬配合物已被證明是制備二氫吡唑骨架的良好光催化劑。但是均相催化劑領域在成本、催化劑回收率、穩定性等方面仍存在許多問題。因此,開發用于無金屬多相光催化雜環合成的有效和選擇性策略仍然是非常重要的。調整半導體光催化劑與基底之間的界面相互作用被認為是重要方法。非均相催化劑的表面性質是至關重要的,因為它們影響基底-催化劑相互作用和電荷載流子的遷移率。在非均相催化劑中調控表面性質也為通過調節反應動力學促進選擇性有機反應提供了相當大的機會。
得益于高熱穩定性和化學穩定性、優異的光伏特性以及獨特的電子結構,聚合氮化碳 (CN) 材料已被證明是用于各種催化反應的有效光催化劑。CN材料具有獨特的表面性質,這可以賦予系統以原始材料中不存在的催化活性。然而,目前大多數用于選擇性有機合成的CN光催化劑都集中在熱力學過程上。通過調整催化劑和底物之間的界面相互作用來提高內在活性仍然具有挑戰性。
02
成果簡介
福州大學王心晨、成佳佳教授開發了具有豐富的-NH2的尿素衍生的氮化碳,催化劑帶正電荷的表面可以有效地與去質子化的陰離子中間體絡合,以改善有機反應物在催化劑表面的吸附。所制備的催化劑可用于氮中心自由基的光催化環化,可以合成具有高活性和可重復使用的多種藥物相關化合物(33 個實例)。該工作以“Photocatalytic cyclization of nitrogen-centeredradicals with carbon nitridethrough promoting substrate/catalystinteraction”為題發表在《Nature Communications》上。
03
研究亮點
1.降低的氧化電位和最高占據分子軌道位置的上移使得催化劑的電子奪取動力學在能量上更有利;
2. 設計了具有連續流動和光催化劑循環利用的克級反應裝置。
04
圖文導讀
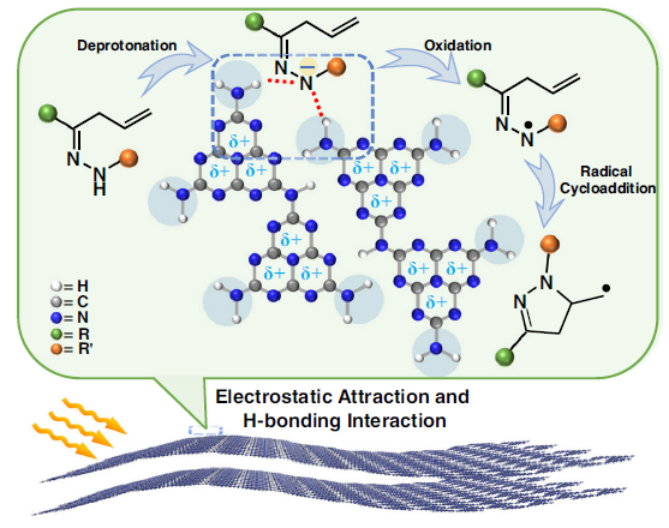
圖 1 氮中心自由基在氮化碳上的界面輔助催化環化。
如圖1所示,提出了在CN上合成功能化二氫吡唑的多相光催化策略。制備了三種具有不同表面性質的CN樣品(g-CN-U、g-CN-DCDA和K-PHI)。觀察到具有豐富的-NH2的尿素衍生氮化碳(g-CN-U)和相對正表面可以有效地與原位生成的陰離子中間體絡合,提高催化劑表面關鍵物質的吸附和活化。
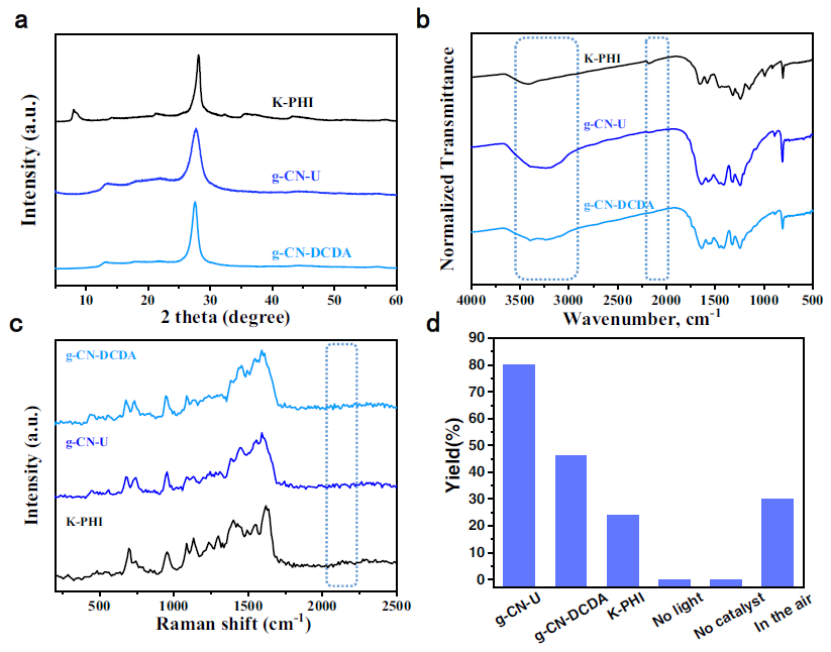
圖2a g-CN-U、g-CN-DCDA、K-PHI的XR;b g-CN-U、g-CN-DCDA、K-PHI的FT-IR光譜;c g-CN-U、g-CN-DCDA、K-PHI的拉曼光譜;d不同光催化劑的光催化活性。
XRD分析證實了光催化劑的晶體結構和分層堆疊模式(圖2a)。在FT-IR中,可以觀察到與庚嗪單元相關的特征峰,表明樣品的框架相同。g-CN-U位于3250 cm-1附近的峰強度比g-CN-DCDA和K-PHI強,表明g-CN-U表面存在豐富的NH2基團。K-PHI在1000 cm-1的峰對應于NK鍵(圖2b)。K-PHI在2180 cm-1處的峰與氰胺官能團振動頻率相關(圖2c)。g-CN-U具有最高的光催化性能(圖2d)。
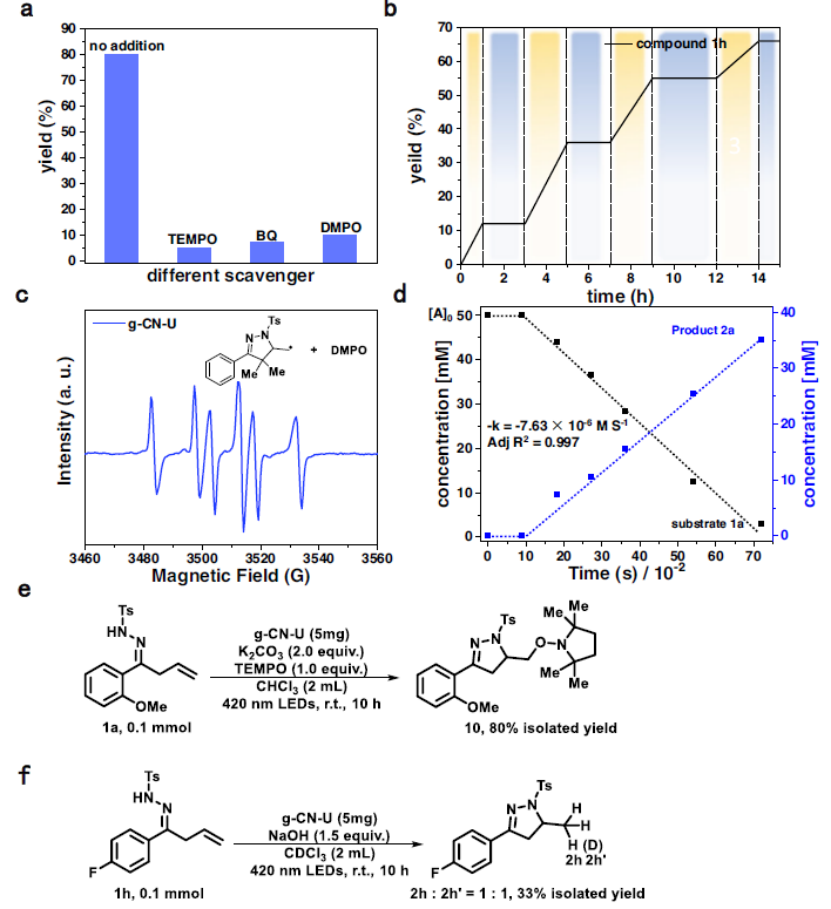
圖3a自由基清除實驗;b開關燈實驗;cESR自旋捕獲實驗;d不飽和β,γ-腙在g-CN-U上的光催化加氫反應時間曲線;e加入TEMPO的反應產物;f在氘代溶劑中進行反應。
自由基清除劑(TEMPO、BQ 或 DMPO)的加入顯著抑制了產物的形成(圖3a)。光開關實驗排除了鏈式過程(圖3b)。ES光譜揭示了一種以碳為中心的自由基物種(圖3c)。TEMPO捕獲產物證實了這一假設(圖3e)。然后在 CDCl3中進行反應(圖3f),2h和2h'的比例為1:1,總產率為33%,證實了產物來自CHCl3的部分氫源。零級動力學曲線表明,決速驟是由于活性物質在g-CN-U 表面的吸附而發生的(圖3d)。
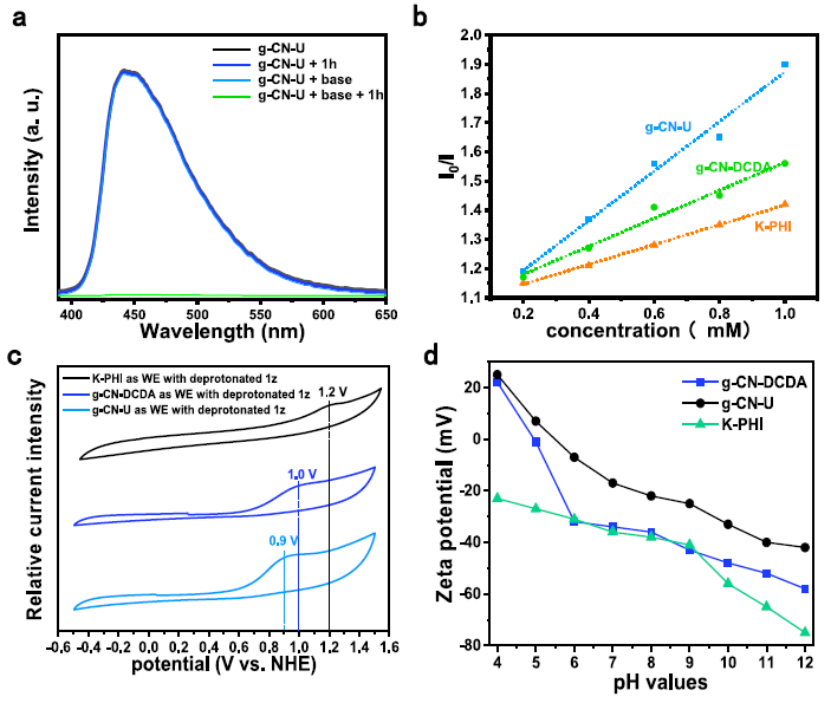
圖4a g-CN-U、g-CN-U/底物、g-CN-U/堿和 g-CN-U/底物/堿在 CHCl3中的穩態光致發光光譜;b 在450 nm (λexc= 390 nm) 處的穩態發射強度和不同的底物濃度的Stern-Volmer分析;cCV;d不同pH下樣品的Zeta電位。
如圖4a所示,當存在堿或腙時,混合物顯示出不變的發射強度。當同時加入腙和堿時,發射信號顯著減弱。Stern-Volmer研究也可以支持g-CN-U和去質子化腙之間加強的相互作用。如圖4b所示,去質子化腙和g-CN-U之間的電子轉移速率比其他催化劑發生得更快。如圖4c所示,在所有的催化劑中,g-CN-U顯示出最低的氧化過電位,這由于g-CN-U與陰離子中間體之間更強的相互作用。Zeta電位測量表明在大多數 pH 范圍內,K-PHI和g-CN-DCDA表現出比g-CN-U更大的負電位(圖4d)。
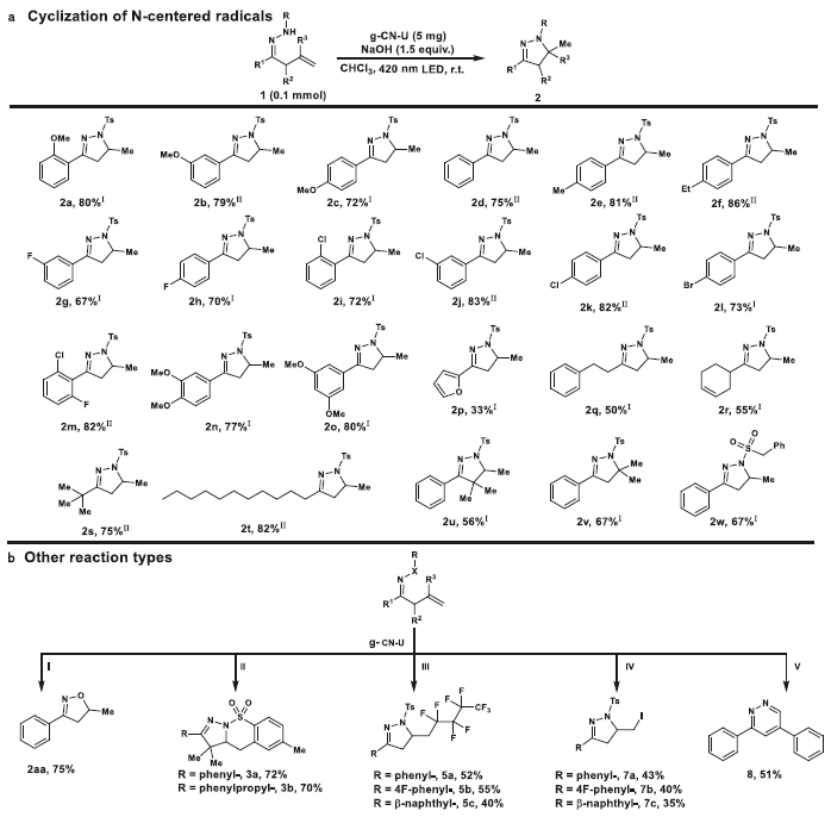
圖5aβ,γ-不飽和腙環化的底物范圍;b其他反應類型。
如圖5a所示,反應在苯基衍生的底物上順利進行,在不同的位置產量高 (2a-l)。雙取代的 β,γ-不飽和腙衍生物作為有效的環化底物 (2m–o)。含有雜環部分的腙具有良好的耐受性,具有33%的產率。烷基取代的腙,包括伯、仲和叔脂肪族基團,可以順利進行 (2q–t)。范圍可以擴大到包括在α位或末端烯烴部分具有烷基的腙(2u,v)。光催化生產2a在420 nm處的表觀量子效率 (AQE) 為7.47%。如圖5b所示,g-CN-U催化劑可以促進β,γ-不飽和肟(2aa)的光催化環化。g-CN-U 也被證明是與 [Co]助催化劑結合使用的合適光催化劑,以70-72%的分離產率提供稠合三環產物 (3a,b)。除此之外,g-CN-U對自由基烯烴全氟烷基化表現出令人滿意的活性,并伴隨有β-官能化 (5a–c)。這一結果表明,在g-CN-U上有效生成了一種反應性全氟烷基自由基物質,它可以直接與碳中心自由基中間體偶聯或攻擊底物的富電子CC雙鍵。以碘代環己烷為偶聯底物(7a-c)切換轉化的選擇性,得到鹵環化產物。
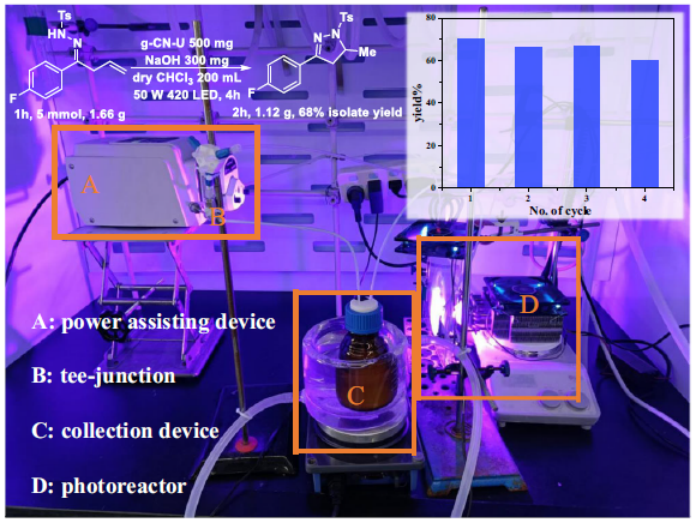
圖6具有連續流動和光催化劑循環利用的克級反應裝置。
使用g-CN-U的光催化過程在反應體積、反應物起始濃度和穩定性方面表現出良好的放大潛力(圖6)。使用連續流動裝置,二氫吡唑衍生物的收率可以達到 68%,反應時間可以進一步縮短到一半。此外,g-CN-U還具有良好的穩定性。
05
總結與展望
作者證明了聚合物半導體g-CN-U是一種高效且穩定的無金屬催化劑,可用于光催化生產各種藥物相關雜環,產率高且底物范圍廣,揭示了催化劑與底物之間的界面耦合是促進反應的關鍵。g-CN-U與表面配合物體系可以通過堿和可見光的協同組合促進NH鍵的高選擇性氧化為以氮為中心的自由基。化學吸附底物-g-CN-U表面復合物的形成歸因于豐富的NH2基團和g-CN-U上相對帶正電荷的表面,通過靜電引力和氫鍵作用與去質子化的陰離子腙有效偶聯。導致腙的氧化電位發生變化,從而更容易去除電子并產生以氮為中心的自由基。這項工作為從動力學的界面相互作用的角度有效改性氮化碳或其他無金屬光催化劑提供了有用的參考。
06
文獻鏈接
Photocatalytic cyclization of nitrogen-centered radicals with carbon nitride through promoting substrate/catalyst interaction (Nat. Commun.2022, DOI:10.1038/s41467-022-32623-3)
文獻鏈接:
https://www.nature.com/articles/s41467-022-32623-3
審核編輯 :李倩
-
電荷
+關注
關注
1文章
643瀏覽量
36336 -
催化劑
+關注
關注
0文章
93瀏覽量
10342
原文標題:王心晨Nature子刊:底物/催化劑相互作用助力氮中心自由基與氮化碳的光催化環化反應
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
Adv. Mater.:界面水調控促進超低過電位下硝酸根還原產氨

離子束與材料的相互作用
異質結類型的介紹



理濤-催化劑磨損指數測定儀 催化劑磨耗測試儀-視頻解說 #催化劑磨損指數測定儀 #催化劑磨耗測試儀 #理濤
實時原位監測光電催化過程中反應物濃度與熱效應的微光纖傳感器技術
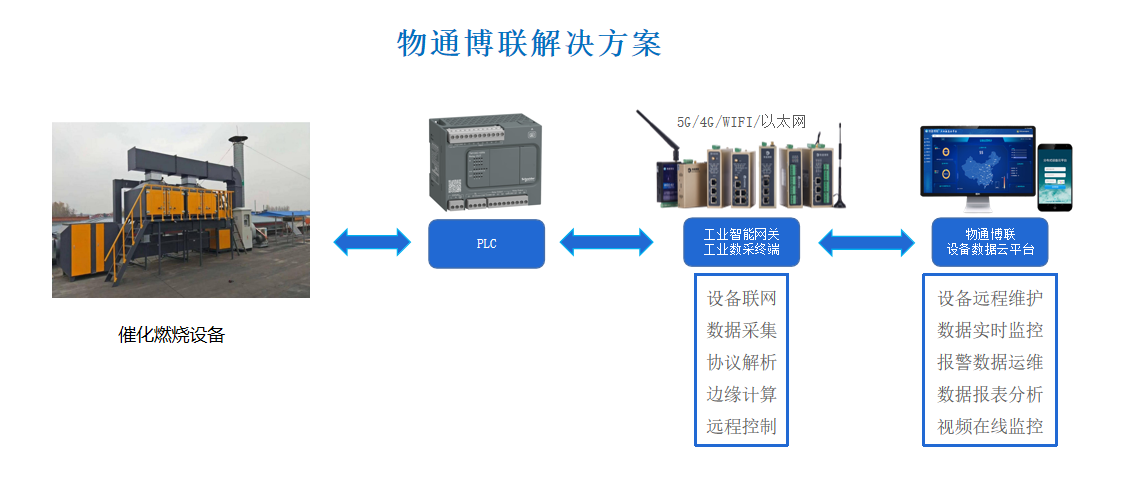
催化燃燒設備數據采集遠程監控系統解決方案
網關助力催化劑產業升級,解決痛點問題!

浪潮通信信息榮獲2024 TM Forum催化劑項目大獎
EthernetiP轉modbusTCP網關在加氫催化中的應用

EthernetiP轉modbusTCP網關在加氫催化中的應用

弦采集儀巖石樁基施工相互作用監測中的幾個方面





 通過促進基質/催化劑相互作用實現氮中心自由基與氮化碳的光催化環化
通過促進基質/催化劑相互作用實現氮中心自由基與氮化碳的光催化環化










評論