人類中樞神經(jīng)系統(tǒng)(CNS)內(nèi)的神經(jīng)回路由具有不同生物物理和功能特征的興奮性/抑制性神經(jīng)元細胞形成。鑒于神經(jīng)回路的復雜性,繪制大腦的解剖和功能特征對于神經(jīng)生物學家來說仍然是一項具有挑戰(zhàn)性的任務。微流控技術(shù)和微制造技術(shù)已被廣泛用于開發(fā)具有集成神經(jīng)細胞大小的微通道的復雜裝置。
此外,許多微流控裝置也與光學和電生理學技術(shù)兼容,使得單個神經(jīng)元能夠被監(jiān)測和操縱。近日,來自德國波恩大學的Volker Busskamp團隊回顧了利用微流控技術(shù)進行不同類型神經(jīng)元細胞分選以及神經(jīng)回路構(gòu)建和分析的研究進展。
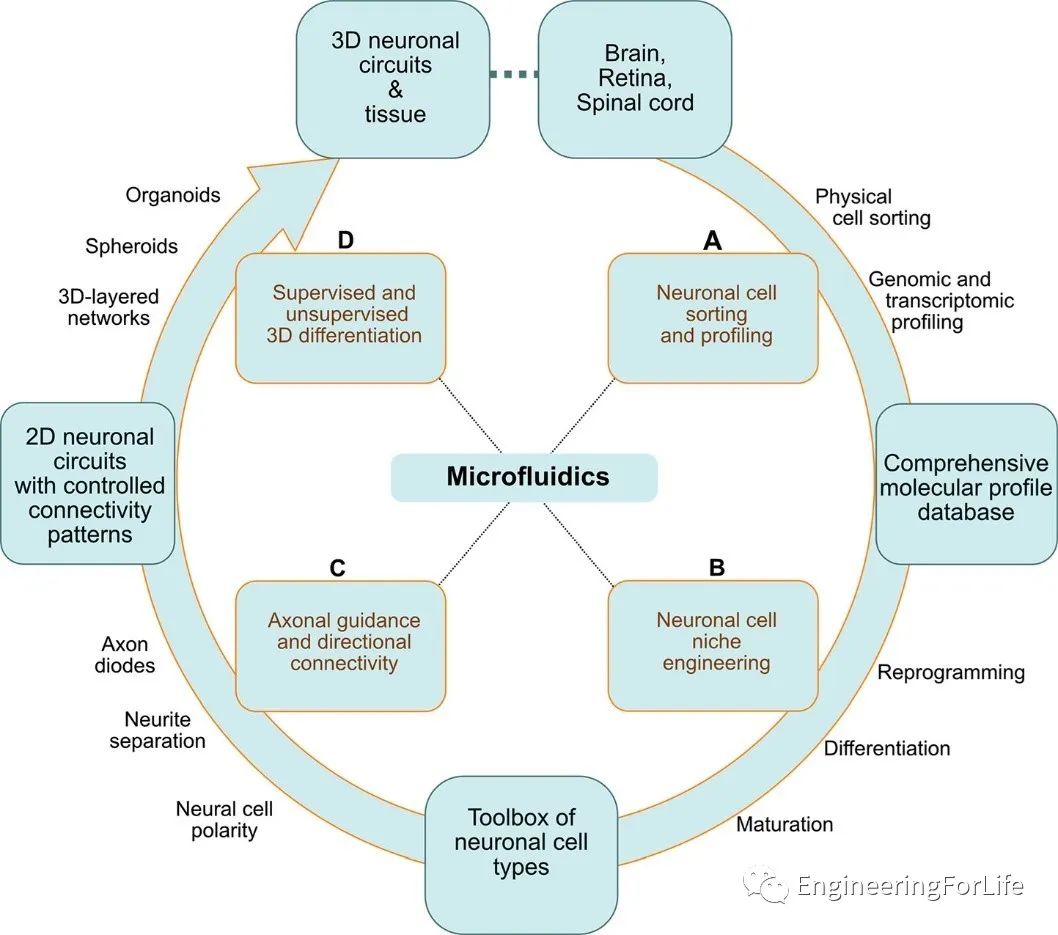
圖1 微流控平臺的多種應用:從中樞神經(jīng)系統(tǒng)細胞的表征到體外神經(jīng)元細胞分選和神經(jīng)回路設(shè)計
首先,研究人員介紹了各種基于微流控技術(shù)的細胞分選策略。例如,通過使用粘彈性調(diào)諧和調(diào)節(jié)微通道中的液體流速,已經(jīng)分離出來自大鼠脊髓的神經(jīng)元和神經(jīng)膠質(zhì)細胞(圖2a)。利用慣性微流控平臺在蛇形通道中分離初級神經(jīng)元和神經(jīng)膠質(zhì)細胞(圖2b)。具有螺旋形通道的慣性微流控裝置也已用于從大細胞群中分離神經(jīng)元細胞(圖2c)。
除了利用流體流動來分離細胞之外,電泳和聲學電泳方法也可以與微流控平臺集成用于細胞分選(圖2d-e)。 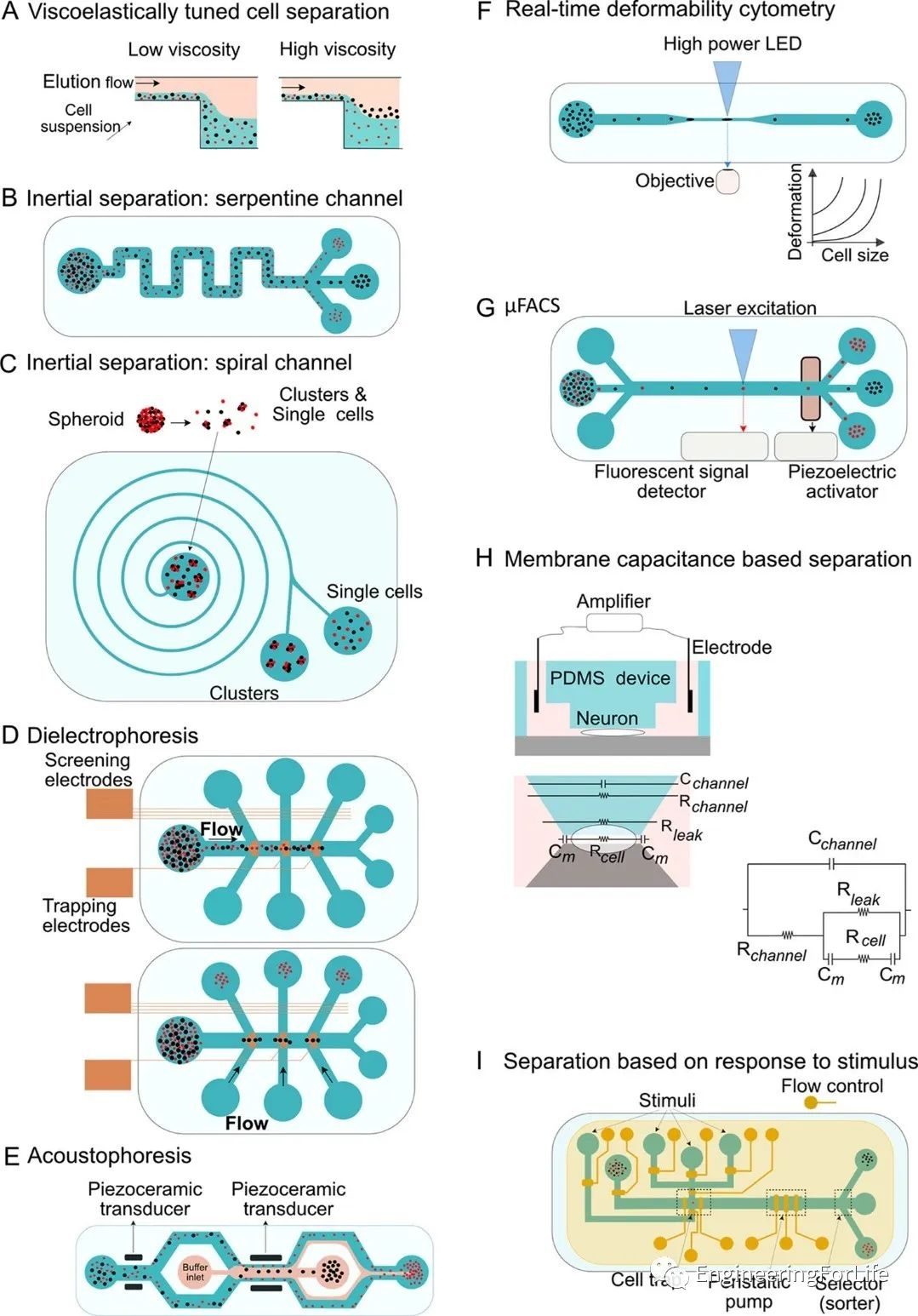
圖2 基于微流控技術(shù)的不同細胞分選策略
其次,研究人員總結(jié)了微流控技術(shù)對scRNA測序技術(shù)發(fā)展的貢獻。對于單細胞轉(zhuǎn)錄組分析,第一步是在微升或納升反應體積中分離單個細胞。
后者主要通過使用流式細胞熒光分選技術(shù)(FACS)、基于集成閥門或液滴的微流控系統(tǒng)或基于微流控技術(shù)的高密度微孔板來實現(xiàn)(圖3)。此外,先進的多模式微流控平臺正試圖在scRNA-Seq實驗中納入評估生理異質(zhì)性的選項:可以根據(jù)細胞的分子特征,或根據(jù)其生理特性繪制細胞圖。
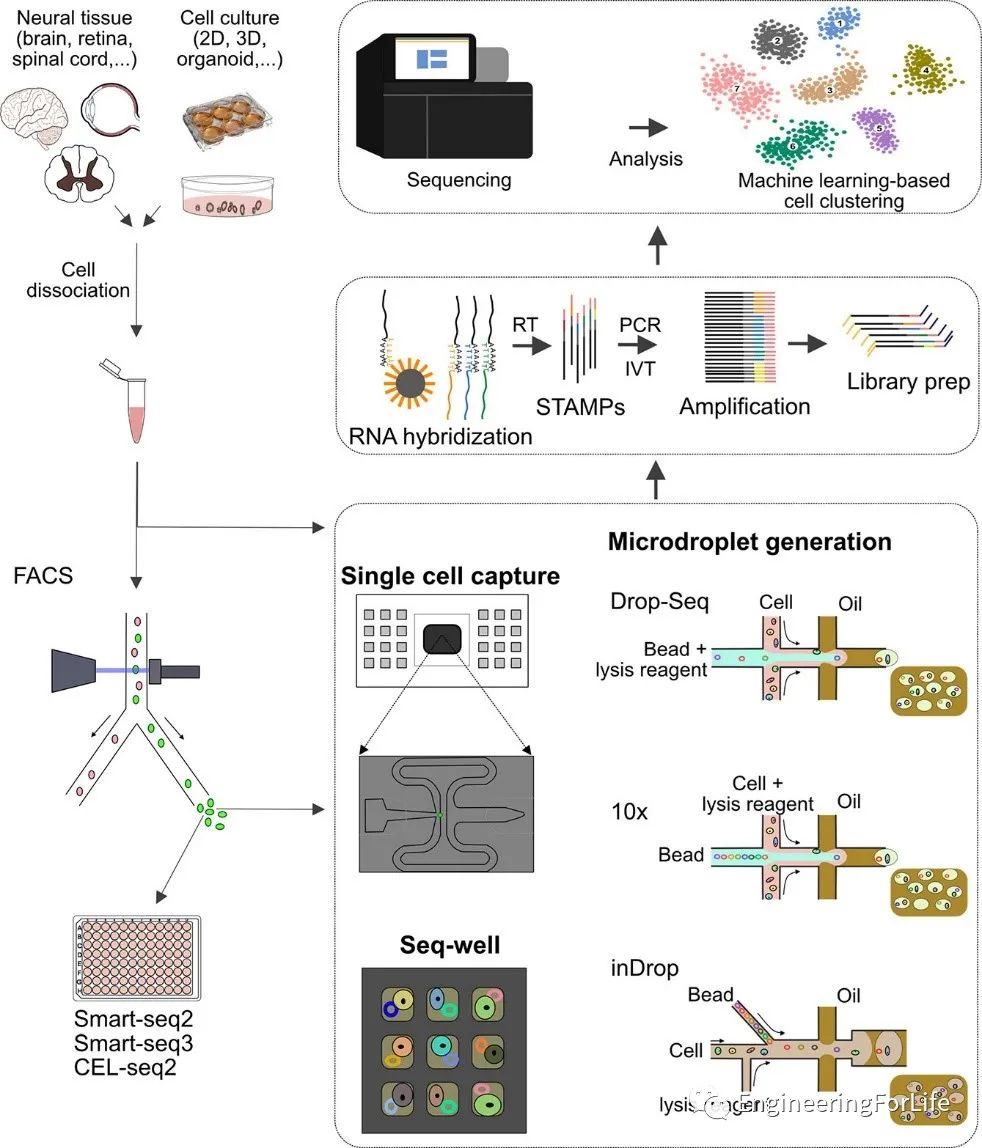
圖3 微流控技術(shù)對scRNA測序技術(shù)發(fā)展的貢獻
隨后,研究人員介紹了利用微流控梯度發(fā)生器構(gòu)建神經(jīng)元細胞生態(tài)位的相關(guān)工作。研究揭示通過使用較小尺寸的微通道可以增加神經(jīng)元干細胞的分化速率,表明新鮮培養(yǎng)基的連續(xù)供應對于神經(jīng)元干細胞的維持是至關(guān)重要的。目前,微流控技術(shù)已被用于影響多種神經(jīng)元功能,如促使未分化神經(jīng)突變成樹突的同時阻止軸突分化和生長;提高軸突導向效率;測試軸突對淺和陡引誘物梯度的反應;引導軸突錐體生長等。
此外,還可以利用微流控裝置來同時提供連續(xù)和不連續(xù)的化學梯度,或者將它們與物理線索如表面圖案和結(jié)構(gòu)相結(jié)合,以提供更真實的體內(nèi)微環(huán)境模型(圖4)。 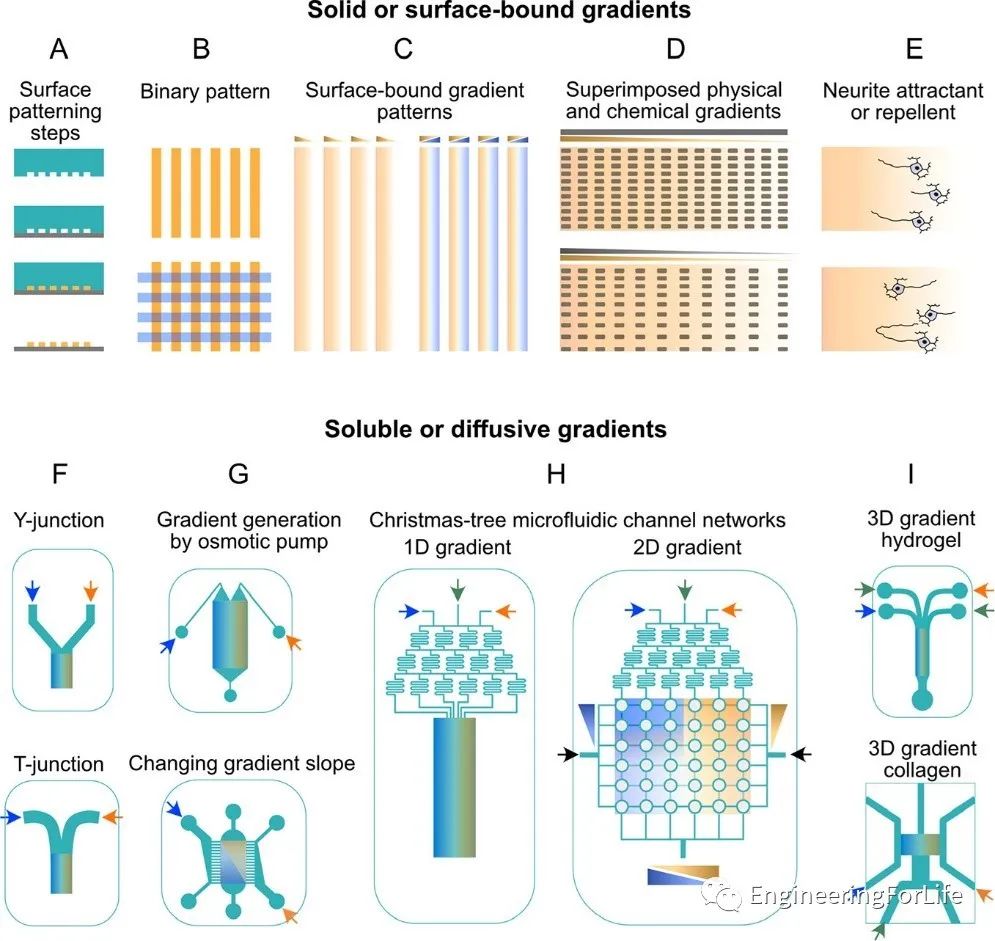
圖4 利用微流控梯度發(fā)生器構(gòu)建神經(jīng)元細胞生態(tài)位
最后,研究人員梳理了用于不同神經(jīng)元回路設(shè)計的微流控技術(shù)。主要包括用于軸突導向的微流控技術(shù)、用于神經(jīng)突分離和功能評估的微流控技術(shù)和用于分離樹突和突觸的微流控技術(shù)(圖5a-d)。 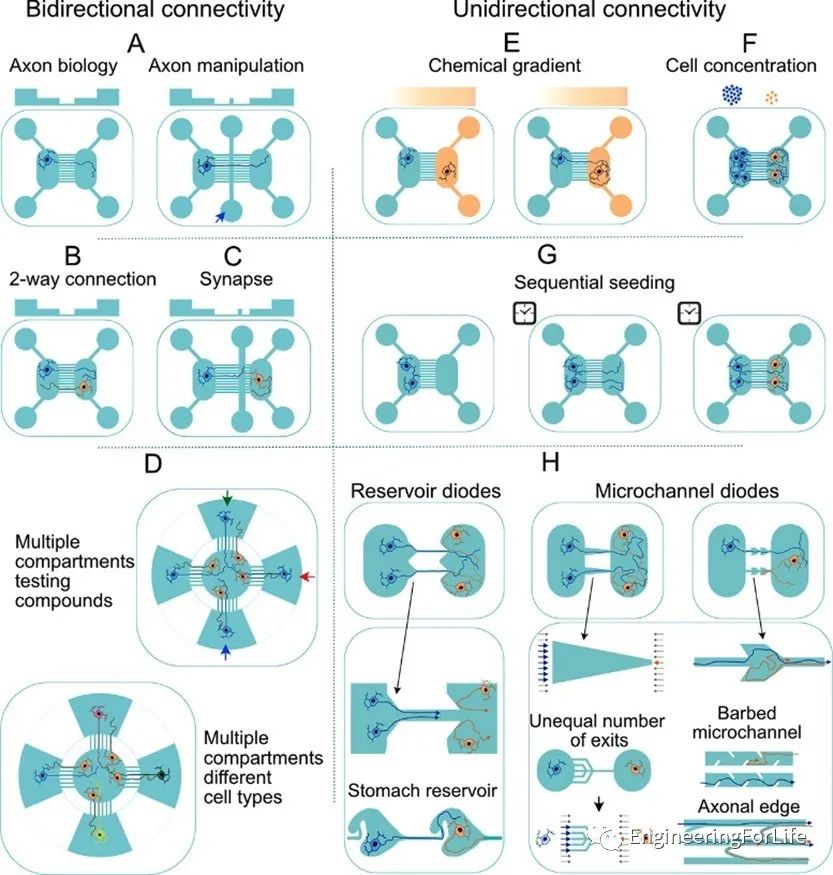
圖5 基于微流控技術(shù)進行神經(jīng)元回路構(gòu)建的主要方法
總體而言,微流控技術(shù)的進步使我們能夠加深對細胞和組織的結(jié)構(gòu)和功能的理解,最終為更準確地在體外模擬神經(jīng)退行性和發(fā)育性疾病以及開發(fā)先進的細胞替代療法提供關(guān)鍵信息。
審核編輯:劉清
-
微流控系統(tǒng)
+關(guān)注
關(guān)注
1文章
73瀏覽量
1867
原文標題:用于神經(jīng)元細胞和神經(jīng)回路研究的微流控技術(shù)綜述
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
神經(jīng)元是什么?神經(jīng)元在神經(jīng)系統(tǒng)中的作用
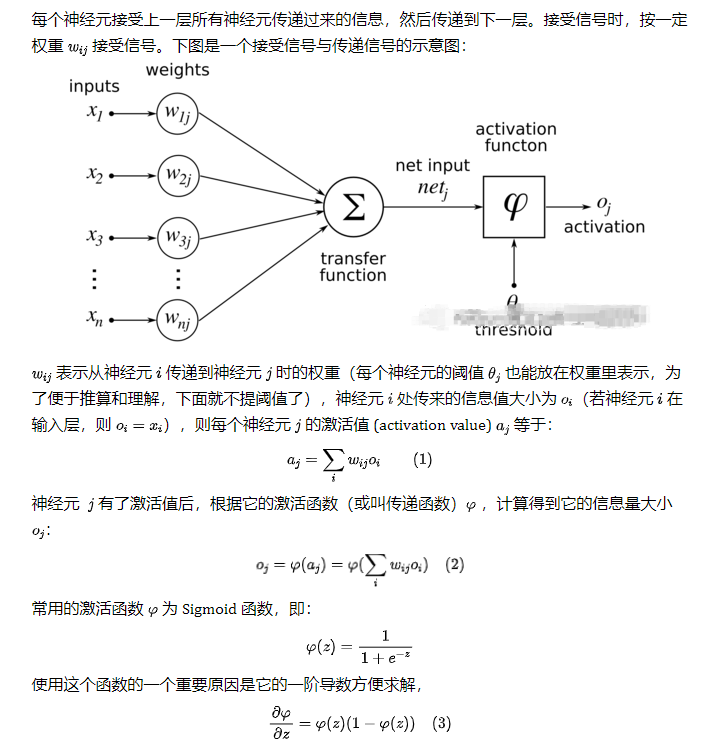
人工神經(jīng)元模型的基本構(gòu)成要素
生物神經(jīng)元模型包含哪些元素
人工智能神經(jīng)元的基本結(jié)構(gòu)
人工神經(jīng)元模型的基本原理及應用
人工神經(jīng)元模型的三要素是什么
神經(jīng)元的基本結(jié)構(gòu)包括哪三部分
神經(jīng)元的分類包括哪些
神經(jīng)元的結(jié)構(gòu)及功能是什么
神經(jīng)元的基本作用是什么信息
神經(jīng)元的信息傳遞方式是什么
基于微流控技術(shù)的微納米馬達用于遞送神經(jīng)干細胞和恢復神經(jīng)連通性




 利用微流控技術(shù)進行神經(jīng)元細胞分選
利用微流控技術(shù)進行神經(jīng)元細胞分選










評論