據麥姆斯咨詢報道,澳大利亞新南威爾士大學的研究人員進行了兩項研究,不僅揭示了造血干細胞前體如何在動物和人類中產生,而且揭示了它們是如何被人工誘導的。這些成果標志著人類向使用誘導多能干細胞治療疾病這一目標又邁進了一大步,將來有望消除對造血干細胞供體的需求。
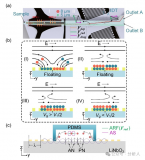
模擬胚胎心跳和血液循環(huán)的微流控裝置。細胞接種通道為紅色(食用染料),而心室收縮控制通道和循環(huán)閥控制通道分別為藍色和綠色
在疾病治療中,誘導多能干細胞是從成人身上提取的細胞,通過逆向工程轉化成干細胞,而不是使用活的人類或動物胚胎干細胞。
在近期發(fā)表于《細胞報告》的一項研究中,新南威爾士大學生物醫(yī)學工程學院的研究人員描述了他們在實驗室使用3cm × 3cm的微流控裝置,模擬胚胎心臟跳動和血液循環(huán)過程是如何導致人類造血干細胞前體的形成和發(fā)育的。這些系統(tǒng)促進了造血干細胞前體的發(fā)育,這種干細胞可以分化為白細胞、紅細胞、血小板等各種血液成分。
研究人員表示,該微流控裝置不僅創(chuàng)造了血液干細胞前體,還產生了分化血細胞,而且還創(chuàng)造了對這一過程至關重要的胚胎心臟環(huán)境的組織細胞,希望這項研究能幫助戰(zhàn)勝目前再生醫(yī)療面臨的挑戰(zhàn):供體造血干細胞短缺、供體組織細胞被排斥,以及圍繞體外受精胚胎使用的倫理問題。
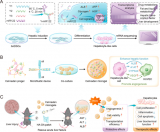
與此同時,在最近發(fā)表在《自然·細胞生物學》上的一篇文章中,新南威爾士大學醫(yī)學與健康學院的研究人員揭示了造血干細胞是如何在胚胎中產生的。在對小鼠的研究中,研究人員發(fā)現了哺乳動物血管內皮細胞轉變?yōu)樵煅杉毎奶烊粰C制。
雖然這些發(fā)現在轉化為臨床實踐之前還需要更多的研究,但可能為產生可植入的造血細胞提供一種潛在的新工具。
這兩項研究都是朝著理解如何、何時、何地以及哪些細胞參與生成造血干細胞邁出的重要一步。在未來,這些知識有望幫助接受高劑量放療和化療的癌癥患者解決造血干細胞短缺問題。
-
微流控
+關注
關注
16文章
526瀏覽量
18887 -
干細胞
+關注
關注
0文章
7瀏覽量
2633
原文標題:基于微流控技術揭示造血干細胞前體之謎,助力解決供體不足問題
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發(fā)布評論請先 登錄
相關推薦
微流控技術的生物學應用
芯片上集成功能性血管化類器官的微流控平臺
Aigtek高壓放大器在介電泳的微流控細胞分離技術中的應用
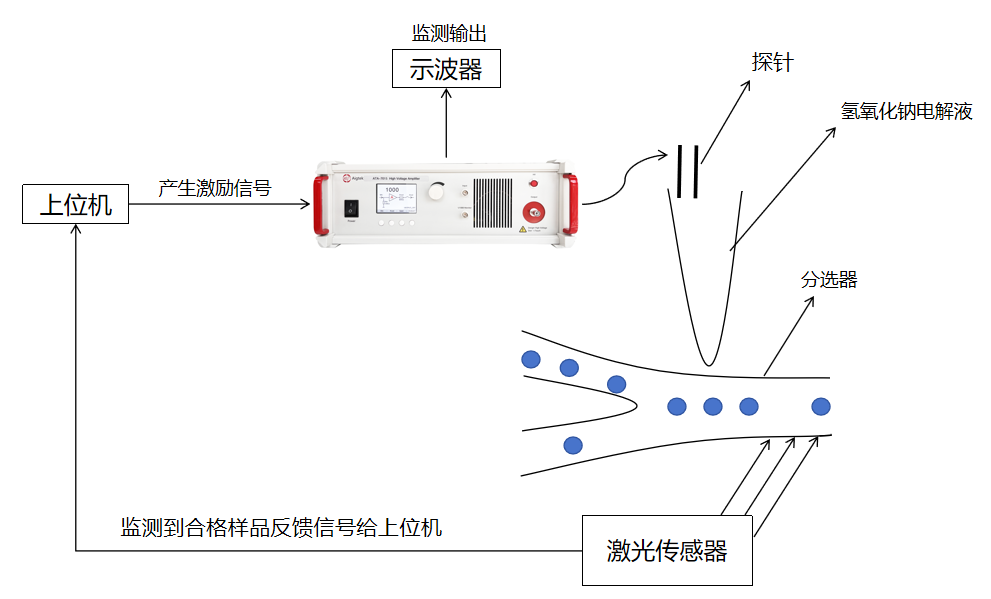
ATG-2000系列功率信號源在介電電泳細胞分選測試中的應用

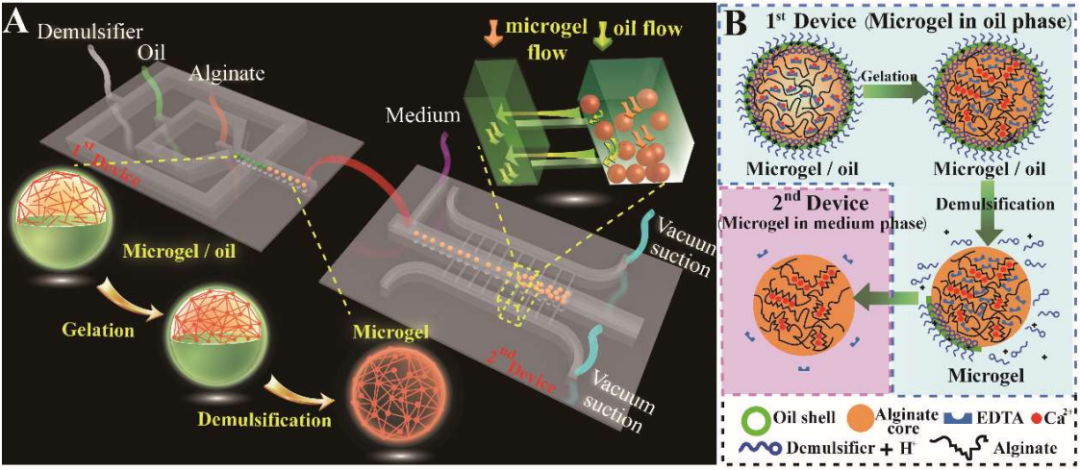
ATA-7020高壓放大器在微流控3D細胞微球培養(yǎng)中的應用
微流控芯片3大制作技術
淺談微流控芯片技術

美國研究人員使用干細胞制作芯片心臟,助力藥物安全性評估
優(yōu)可測推動微流控技術革新,精準助力生物醫(yī)學等行業(yè)的發(fā)展

基于微流控技術的微納米馬達用于遞送神經干細胞和恢復神經連通性




 基于微流控技術有望消除對造血干細胞供體的需求
基于微流控技術有望消除對造血干細胞供體的需求











評論