01
研究背景
金屬鈉負極的低還原電位和高理論容量使其有望實現高能量密度金屬鈉電池(SMBs),但其商業化面臨諸多挑戰,這些挑戰與電解質相容性和負極界面現象相關。
與金屬鋰負極不同,在使用傳統碳酸鹽電解質時,金屬鈉負極的固體電解質界面(SEI)穩定性較差。這些電解質的自發化學還原導致不穩定的鈍化膜,反復暴露負極到大量電解質溶液中,通過消耗活性材料加速電池失效。
與鋰類似,金屬鈉負極也表現出枝晶形貌,導致長循環穩定性較差。此外,這些枝晶還可能導致電池自發短路和安全問題。因此,需要對電解質進行優化,以實現穩定的鈉金屬負極。
02
成果簡介
近日,阿貢國家實驗室Christopher Johnson教授和加州大學Vincent Lavallo教授在Angew上發表了題為“A Carboranyl Electrolyte Enabling Highly Reversible Sodium Metal Anodes via a “Fluorine-Free”SEI”的論文。該論文提出了一種采用 [HCB11H11]1-(1)作為陰離子的新型無氟電解質。
用這種電解質組裝的Na對稱電池在2.0 mA cm-2下表現出極低的過電位,為0.032 V,在半電池構型中具有99.5%的高庫侖效率。循環后電極表面沒有鈉枝晶成核,并形成了穩定的無氟SEI。
03
研究亮點
(1)本工作首次報告了一種非氟化弱配位陰離子(WCAs),它使金屬鈉負極的循環庫倫效率高達99.5%,具有優異的長循環穩定性。
(2)電解質表征結果顯示,溶劑分離離子對和陰離子的異常分布決定了電解質的原位溶劑化結構。電極表面表征顯示,在長循環過程中沒有枝晶狀金屬鈉成核。鈍化膜的XPS表征顯示,SEI主要由有機物種組成,含硼物種的數量可以忽略不計。
(3)電解質原位溶劑化結構的表征證明,陰離子的還原穩定性以及1的弱配位性,是獲得高可逆金屬鈉負極的關鍵。
04
圖文導讀
[Na]+[HCB11H11]-通過HNMe+1與NaH在四氫呋喃中反應得到(圖1a)。與典型的鹽復分解方法相比,這里采用的合成策略只產生氣態的副產物,以及Na1。Na1在二乙二醇二甲醚(G2)中的溶解度限制在~0.93 M,不能制備1.0 M標準電解質溶液。因此,本研究制備了0.9 M Na1溶液,得到Na1/G2作為電解質(圖1b)。
通過同步輻射小角X射線散射(SAXS)實驗與分子動力學模擬,對Na1/G2的原位溶劑化結構進行嚴格的表征。在高q區觀察到的兩個峰表明,陰離子進入兩個不同的環境。多數陰離子-陰離子分隔距離為6.04 ?和11.5 ?(圖1c, d)。第一個峰(6?)對應于最接近的陰離子,它們之間沒有溶劑,導致形成小的陰離子-陰離子聚集體。
由于Na1在0.9M二乙二醇二甲醚溶液中均勻分布,第二個峰(12?)來自于陰離子的長程相互作用(圖1e)。在計算模型中發現,Na1/G2含有<1%的Na+-碳硼烷接觸離子對(CIP)。Na1/G2中的Na+溶劑化結構傾向于形成豐度大于99%的溶劑分離離子對(SSIP)。
電解質的固態晶體結構顯示,飽和Na+絡合物[Na(G2)2]+與碳硼酰B-H之間最近的相互作用距離為4.945 ?,說明Na1/G2中離子顯著解離(圖1b)。因此,電解質完全由離散的[Na(G2)n]+絡合物和碳硼烷陰離子組成,它們在溶液中分布不均勻。
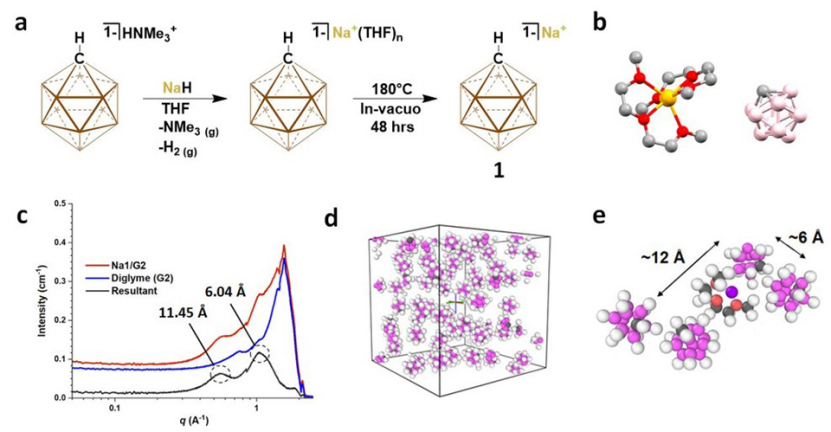
圖 1、(a)通過HNMe3+1與NaH的脫質子化,合成和制備Na1。(b)通過單晶X射線衍射分析確定的Na1/G2分子結構。(c)SAXS光譜表征了Na1/G2中原位陰離子-陰離子分離和陰離子團簇的存在。(d)分子動力學系統中陰離子分散的照片和(e)陰離子-陰離子分離的放大圖像。
圖2顯示,含Na1/G2的Na-Na電池在0.5 mA cm-2下顯示出穩定的<10 mV極化。從循環開始到超過1000小時,該電位一直保持穩定,這表明Na1/G2的自發化學還原足以穩定地生成SEI(圖2)。同樣,Na-Na電池在1.0和2.0 mA cm-2下也能穩定循環,極化電壓分別為15 mV和32 mV(圖2)。

圖 2、在不同電流密度和1.0 mAh cm-2面積容量下,采用Na1/G2電解質組裝的Na-Na對稱電池的循環性能。
接下來,組裝了含Na1/G2的Na-Cu和Na-Al半電池,以評估裸集流體上的鈉電鍍和剝離過程。Na-Cu半電池的首圈庫侖效率為96.5%,第二圈循環庫侖效率為99.2%,這表明幾乎不需要對電極表面進行修飾就可以實現高效的金屬電沉積(圖3a)。在前100個循環中,平均庫侖效率保持在99.8%,在300個循環后,平均庫侖效率保持在99.5%。
與對稱電池相似,從第一個循環開始,銅電極上鈉沉積和剝離表現出低的電壓極化(圖3b)。長循環后,電壓極化逐漸增加,從第一圈的30.5 mV增加到300圈的45.2 mV。
這可能是由于銅電極上重復形成新的鈉金屬,G2的化學還原,以及溶劑消耗導致的電池內阻增加。沉積后拆卸的半電池顯示出均勻的純金屬鈉層,具有金屬光澤,表明電解質和沉積的金屬鈉之間發生了最小的副反應(圖3a插圖)。
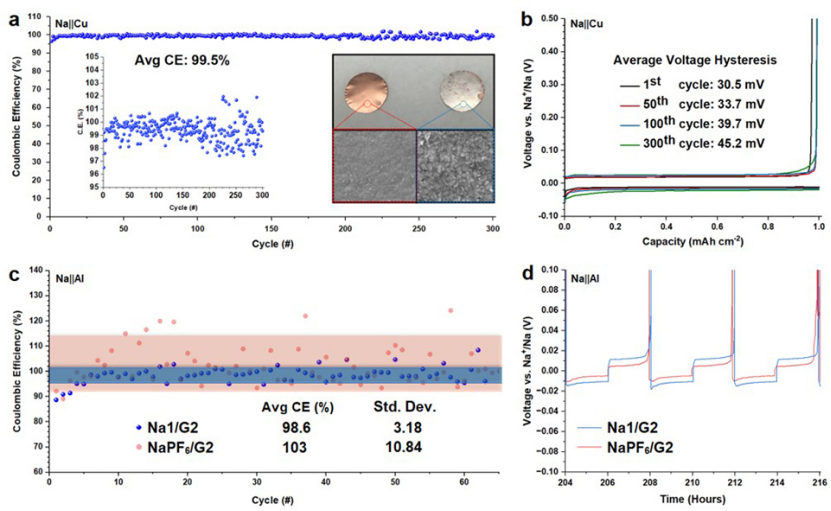
圖 3、(a)運行超過300次后,使用Na1/G2的Na-Cu半電池的庫侖效率(CE)。Na-Cu半電池中原始銅電極和沉積1.0 mAh·cm-2Na在銅基底上后的照片,下面是對應電極表面的掃描電鏡圖像。(b)在0.5 mA·cm-2@1.0 mAh·cm-2下,含Na1/G2的Na-Cu半電池電壓曲線。(c)Na-Al半電池的庫倫效率和(d)含有Na1/G2和NaPF6/G2的Na-Al半電池電壓曲線。
在Na1/G2組裝的Na-Al半電池中觀察到極高的庫侖效率(98.6%),而在NaPF6/G2電解液中,電池放電容量不穩定,循環穩定性差(圖3c),這表明化學惰性的Na1/G2與裸鋁電極具有較高的兼容性,盡管NaPF6/G2在循環過程中表現出略低的過電位(圖3d)。相比之下,1的高化學和電化學穩定性消除了Al和電解液之間的有害副反應。
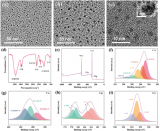
接下來,通過掃描電子顯微鏡(SEM)和能量色散X射線能譜(EDS)映射來表征金屬鈉在Na1/G2中的成核過程,以揭示這種高度可逆行為的起源。研究了金屬鈉在不同荷電狀態(SOC)下的成核過程,結果顯示該過程沒有枝晶狀鈉沉積(圖4a-c)。在20%荷電狀態下(0.2mAh cm-2),銅電極表面有均勻的金屬鈉沉積薄層(圖4b, d)。在滿電狀態下(1.0mAhcm-2),可以觀察到同樣均勻的金屬鈉沉積(圖4c, f)。
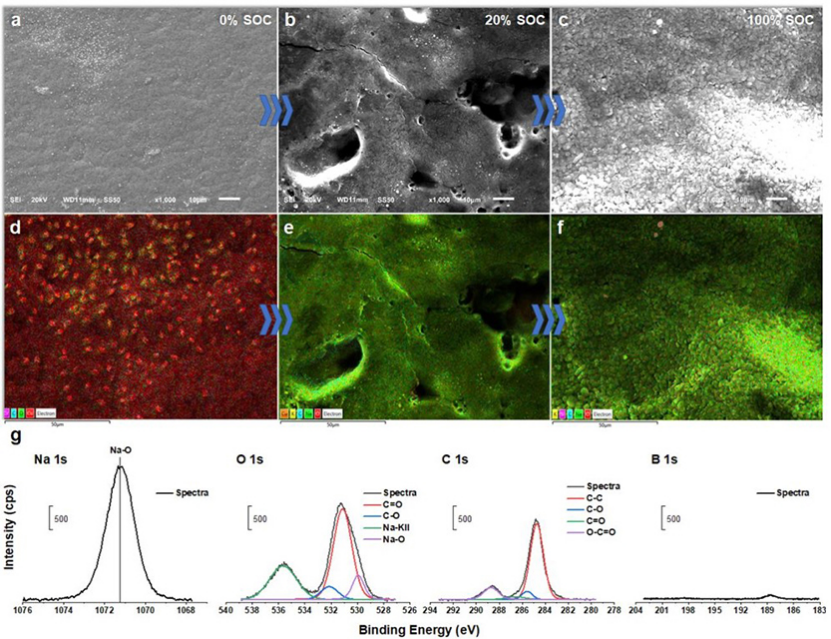
圖 4、Na-Cu半電池在不同荷電狀態下的SEM圖像和相應的EDS映射。(a, d)0% SOC,原始Cu電極(b, e)20% SOC, 0.2 mAh cm-2和(c, f)100% SOC, 1.0 mAh cm-2。(g)從拆卸的Na-Cu半電池中回收的鈉金屬負極XPS光譜。
表面XPS分析顯示,沉積的Na表面上的物質主要由含有Na-O, C-O, C-C和C-H的物種組成(圖4g)。在表面檢測到非常少量(約2.8%)的含硼物種,這與與原始1相關的B-H結合能相對應,表明簇的完整性保持。
05
總結與展望
本工作首次報告了一種非氟化弱配位陰離子(WCAs),并制備了Na1/G2電解液,它使金屬鈉負極的循環庫倫效率高達99.5%,具有優異的長循環穩定性。采用Na1/G2的電池高度可逆,這可歸因于多種因素,包括原位弱離子配位、無枝晶的Na金屬成核以及不含陰離子還原產物的SEI。Na-Cu和Na-Al電池的高庫倫效率得益于1的化學穩定性,以及僅由二乙二醇二甲醚化學還原形成的SEI。此外,Na1/G2的高熱穩定性和導電性使其能夠在常溫下運行。
06
文獻鏈接
A Carboranyl Electrolyte Enabling Highly Reversible Sodium Metal Anodes via a “Fluorine-Free” SEI.(Angewandte Chemie International Edition, 2022, DOI:10.1002/anie.202208158)
原文鏈接:
https://doi.org/10.1002/anie.202208158
審核編輯:劉清
-
soc
+關注
關注
38文章
4398瀏覽量
222990 -
電池電壓
+關注
關注
0文章
209瀏覽量
12029 -
EDS
+關注
關注
0文章
100瀏覽量
11946 -
固體電解質
+關注
關注
0文章
46瀏覽量
8581
原文標題:阿貢國家實驗室Angew:“無氟”SEI實現高度可逆的金屬鈉負極
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
HPM6E00的SEI使用討論
水系電池金屬負極腐蝕問題綜述
哪些電容器需要區分正負極
負極接二極管的負極是什么作用
p-π共軛有機界面層助力鈉金屬電池穩定運行
LDC1314檢測高度主要取決于什么,如何才能提高檢測高度?
多功能高熵合金納米層實現長壽命無負極鈉金屬電池

通過電荷分離型共價有機框架實現對鋰金屬電池固態電解質界面的精準調控



















評論