【研究背景】
金屬鋰負極由于其高比容量(3860 mAh g-1),是石墨的10多倍以上,被認為是鋰電池負極的“圣杯”材料。然而,鋰金屬的固有反應會導致其循環穩定性和安全性較差,使鋰金屬電池(LMBs)的商業化具有挑戰性。目前,鋰金屬電池在低電流密度(<1mA cm-2)循環數百圈后,可實現>99.5%的庫倫效率和>80%的容量保持率。然而,在高電流密度下,鋰金屬負極通常表現出較差的循環性能,這會限制鋰金屬負極在高功率電池的應用。
【成果簡介】
在此,斯坦福大學鮑哲南教授/崔屹教授報道了一種具有花狀納米結構的硬碳載體(CF)。花狀納米硬碳負極在充放電過程中會伴隨著鋰離子的脫嵌和鋰的電鍍/剝離,產生混合的鋰離子/鋰金屬負極容量。當使用商業電解液時,即使在12 mA cm-2(2 mAh cm-2)的電流密度下,CF電極的庫倫效率大于99%。優異的循環穩定性歸因于CF的開孔納米結構,其具有均勻的鋰鍍層形態和快速的離子擴散途徑。此外,CF||NMC811全電池在10 mA/cm2電流密度下進行200次循環后,容量仍可以保持~70%。該文章以Fast-charging of hybrid Lithium-ion/Lithium-metal anodes by nanostructured hard carbon host為題,發表在國際權威期刊ACS Energy Letters.
【詳情簡介】
1. 花狀碳的物理表征
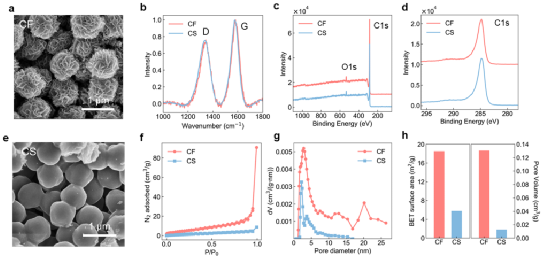
圖1 (a) CF的SEM圖像;(b) CF和CS的拉曼光譜;(c) CF和CS的XPS測量光譜;(d) CF和CS的高分辨率C 1s XPS光譜;(e) CS的SEM圖像;(f) CF和CS的N2洗脫附等溫曲線;(g) CF和CS的孔隙尺寸分布和 (h) BET表面積和孔隙體積。
研究納米結構對鋰電鍍行為的影響,作者合成了兩種硬碳顆粒:花狀硬碳顆粒(CF)和球形硬碳顆粒(CS)。圖1a、e分別為CF和CS的SEM圖像。CF具有獨特的開孔顆粒形態,該結構可以促進離子的擴散。圖1b顯示了CF和CS的拉曼光譜。重疊的D和G峰表明CF和CS具有幾乎相同的碳鍵結構。在XPS譜圖(圖1c),CF和CS的表面組分主要為C和O元素,此外,圖1d的高分辨率C1s XPS峰,也表明了兩種材料具有化學環境相似的碳。然而,由于CF上存在納米結構,CF和CS的孔隙結構有所不同。與CS相比,CF的N2吸附量要高得多,特別是在高壓區域,說明CF具有更多的介孔和大孔(圖1f)。N2等溫曲線得到的孔徑分布也顯示出CF中具有更多的介孔(圖1g)。CF的表面積和孔隙體積也高于CS(圖1h)。
2. 鋰電鍍行為的研究
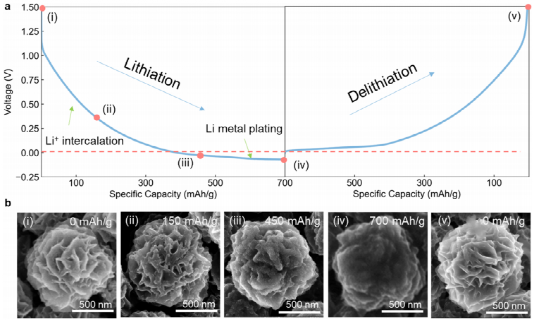
圖2 (a) CF的典型充放電電壓曲線;(b) 充放電過程中CF的形態演化。
作者首先研究了Li||CF半電池在CF上的鋰電鍍行為。典型的充電(鋰化)和放電(去鋰化)電壓曲線如圖2a所示。CF電極以700 mAh/g的比容量進行鋰化,以平衡比容量和循環壽命。CF的比容量主要來源于:鋰離子插層和鋰金屬電鍍。當局部電壓大于0V時(vs Li+/Li),由于CF的硬碳性質,鋰離子插層是主要的容量貢獻者。進一步的過鋰化導致電壓低于0 V(vs Li+ /Li),會發生鋰電鍍行為。
如圖2a所示,當Li鍍在CF上時,沒有出現明顯的鋰成核過電位。該現象與許多三維碳載體材料不同,表明Li可以均勻地電鍍在CF的納米結構上。SEM圖像可以進一步證實這一結果。圖2b中,作者研究了CF顆粒在不同充放電電壓時,鋰化和去鋰化過程中的形態演化。階段i,CF的“花瓣”尖銳而薄,沒有鋰化。階段ii,在鋰離子插入時,“花瓣”稍微增厚,這可能是由于插入引起的體積膨脹。當電壓低于0V(vs Li+/Li)和開始鋰電鍍時,發生了更顯著的變化。階段iii,花瓣變得明顯厚,交叉的“花瓣”之間的山谷開始被填滿。階段iv,當達到最大允許容量時,CF花瓣似乎被完全填充并被Li包裹。階段v,一旦剝離過程完成,CF的原始形態就被恢復了。形態演化過程表明,金屬Li可以均勻地在“花瓣”上和孔隙中進行沉積/剝離。

圖3(a,b)在CF顆粒(a)和CS顆粒 (b) 上的鍍Li示意圖;(c,d)鍍Li后CF的SEM圖像;(e,f)鍍Li后CS的SEM圖像。(g) 100次循環后CF電極表面的SEM圖像;(h) 100次循環后CF電極橫截面的SEM圖像;(i) 100次循環后CS電極表面SEM圖像;(j) 100次循環后CS電極橫截面的SEM圖像。
在相同的比容量和電流密度下,作者在CF和CS上觀察到明顯不同的鋰沉積形態。在第一次沉積過程結束時,可以觀察到:鋰絲從CS顆粒表面向外生長(圖3b,e,f),而CF顆粒上鋰的形態是均勻的(圖3a、c、d)。此外,在100次循環(鋰完全剝離)后,在CF和CS電極上觀察到有顯著差異的形態。圖3g,i顯示了沖洗后CF和CS電極的表面。CS電極表面被死鋰絲覆蓋(圖3i),而CF電極表面沒有可觀察到的死鋰(圖3g)。圖3h,j顯示了在相同的循環條件下(100次循環,完全剝離)下未沖洗的CF和CS電極的橫截面圖。作者在CS電極上觀察到一層厚厚的死鋰絲(圖3j),而CF電極上沒有死鋰層。同時,在CF電極上也沒有觀察到的厚SEI層(圖3h)。
CF上均勻的鋰形態歸因于三個因素:鋰離子嵌入、納米結構的影響和SEI膜結構。首先,鋰離子嵌入在鋰電鍍之前可以改變碳表面的鋰潤濕性。眾所周知,石墨和硬碳在沒有表面改性的情況下是親鋰的。有趣的是,當嵌入鋰離子時,它們是超親鋰的。親鋰表面通常被認為是鋰金屬電鍍的有益性質,因為它使鋰能夠均勻地潤濕表面而不是形成細絲。因此,鋰離子插層使CF表面親鋰,并使鋰的成核勢壘最小化。第二,納米結構提供了高表面積和大孔體積。如圖3h所示,CF的表面積和孔體積分別是CS的3倍和10倍。盡管CS在插層后是親鋰的,但由于低表面積和小孔隙體積,它只能在顆粒的外表面上容納有限的Li。相反,較高的CF表面積使局部電流密度最小化,并使可用的親鋰表面最大化,而較大的孔隙體積為CF顆粒內鋰的體積變化提供了足夠的空間。應注意,負極中應避免極高的表面積,因為在初始充電/放電過程中,它將消耗更多的容量來形成SEI。CF的表面積仍然是可接受的(18.5對比60 m2/g典型炭黑),與CS相比,其初始CE沒有明顯降低(圖S3)。第三,由于鋰金屬對CF結構的限制,在有限的鋰體積變化下,SEI損傷最小。
3. 電化學性能
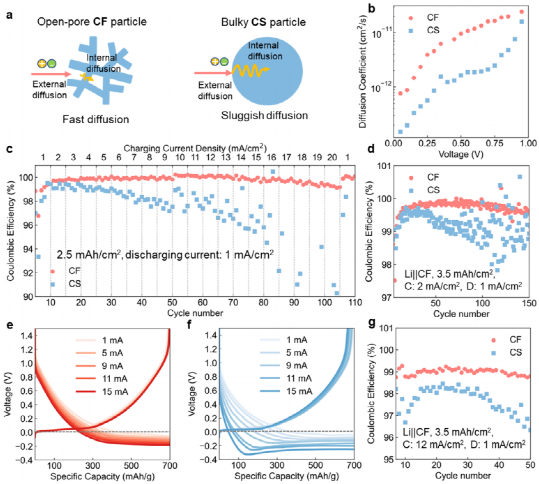
圖4 (a) CF和CS中的離子擴散路徑示意圖;(b) PITT法測定CF和CS的鋰離子擴散系數;(c) Li||CF和Li||CS半電池的倍率性能;(d) Li||CF和Li||CS半電池在2 mA/cm2下的循環性能;(e) Li||CF半電池和 (f) Li||CS半電池在不同電流密度(1-15 mA/cm2)下的電壓分布圖;(g) Li||CF和Li||CS半電池在12 mA/cm2下的循環性能。
此外,開孔結構可以提供更快的離子擴散途徑。與CS微球相比,CF的開孔結構賦予了其更短的離子擴散路徑,如圖4a所示。這與靜電位間歇滴定技術(PITT)測量的Li+擴散常數的結果一致(圖4b)。在鋰離子插層電壓窗口(0-1 V vs. Li/Li+)下,CF的Li+擴散常數幾乎比CS高一個數量級。因此,CF的開孔結構有望有利于快速充電。在充電(鋰化)過程中施加增量電流密度(1?20mA/cm2,每5次循環1mA/cm2),放電(脫鋰化)電流控制為1 mA/cm2(圖4c)。Li||CF半電池的面積容量主要因為CF電極材料上的嵌Li/鍍Li行為。Li||CF半電池在碳酸鹽電解質LP57/FEC中顯示高CE(》99.5%)。如此高的CE可維持在~16mA/cm2,在此以上CE略有下降。另外,當充電電流從20mA下降到1 mA/cm2時,電池可以恢復到原來的高CE(圖4c)。在低電流密度下,CS也表現出較高的CE(圖4c)。然而,隨著充電電流的增加,CEs迅速下降,電池在~16mA/cm2時短路。圖4e,f顯示了與圖4c對應的電壓曲線。CF在不同的電流密度下沒有明顯的成核過電位。同時,當充電電流從1mA/cm2增加到15 mA/cm2時,在電壓》 0 V vs. Li+/Li下的插入容量從428mAh/g緩慢下降到231 mAh/g。相反,在高電流密度下,CS表現出明顯的成核過電位峰。在電壓》0 V vs. Li/Li+時,CS的插層容量也從377衰減到43 mAh/g(圖4f)。圖4d,g分別顯示了Li||CF和Li||CS半電池在2 mA/cm2和12 mA/cm2下的恒流循環。當充電電流為2 mA/cm2時,CF和CS在充電開始時均表現出較高的CE(》99%)。然而,CS的CE隨著循環的增加迅速衰減。而CF電極在高電流密度(12 mA/cm2)下,仍然保持~99%的CE。
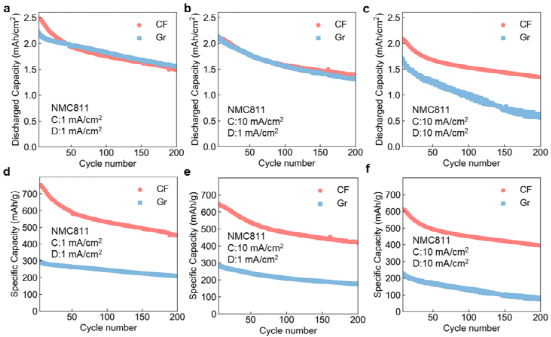
圖5 CF||NMC811和Gr||NMC811的全電池性能;(a) 在1 mA/cm2充電電流和1 mA/cm2放電電流下的放電容量;(b) 在10 mA/cm2充電電流和1 mA/cm2放電電流下的放電容量;(c) 在10 mA/cm2充電電流和10 mA/cm2放電電流下的放電容量;(d) 負極材料在1 mA/cm2充電電流和1 mA/cm2放電電流下的比容量;(e) 負極材料在10 mA/cm2充電電流和1 mA/cm2放電電流下的比容量。
作者進一步分別匹配了CF/Gr電極與商用NMC811正極的全電池,并且以恒定電流放電到《1.8 V(CF||NMC811)和《2.6 V(Gr||NMC811)。在相對較低的電流密度下,Gr||NMC811電池比CF||NMC811電池表現出更好的容量保留(圖5a)。然而,由于鋰電鍍行為,CF比Gr電極具有更高的比容量(圖5d)。盡管容量保留率較低,但在前200個周期中,與Gr電極相比,CF電極仍顯示出約2倍的比容量。當施加10 mA/cm2充電和1 mA/cm2放電電流時,Gr||NMC811的容量保留率下降(圖5b),而CF||NMC811與低電流情況相比具有相似的循環穩定性。同樣,由于鋰電鍍行為的貢獻,與Gr電極相比,CF具有2倍的比容量(圖5e)。當充放電電流均為10 mA/cm2時,Gr||NMC811電極的容量衰減較快,200次循環后只有~30%的容量可用,而CF電極在快充/快放情況下,保持了長達200次的穩定循環(~70%的容量保持率)(圖5c)。
【結論】
作者引入了一種開孔花狀硬碳(CF),使商業碳酸鹽電解質能夠實現快速充電的電池行為。金屬Li可以均勻沉積在硬碳表面,形成鋰離子/鋰金屬復合型負極。研究表明,獨特的納米結構使CF顆粒內均勻和保形的Li電鍍。與球形硬碳顆粒相比,CF的開孔結構提供了快速的離子擴散途徑,使其在高電流密度下具有良好的循環穩定性。
審核編輯:郭婷
-
鋰電池
+關注
關注
260文章
8223瀏覽量
172690 -
分辨率
+關注
關注
2文章
1074瀏覽量
42119
原文標題:?崔屹&鮑哲南教授:“花狀硬碳”同時具有“嵌Li+/鍍Li”行為、助力快充鋰電池
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦




 具有花狀納米結構的硬碳載體助力快充鋰電池
具有花狀納米結構的硬碳載體助力快充鋰電池











評論