【背景】
鋰硫電池以轉(zhuǎn)換反應(yīng)為基礎(chǔ),可以克服鋰離子電池(LIBs)中插入式氧化物陰極和石墨陽(yáng)極的局限性,使能量密度更高。鋰硫電池由硫陰極和鋰金屬陽(yáng)極組成。硫的電絕緣性質(zhì)意味著它必須被加載到一個(gè)導(dǎo)電的基體上--通常由多孔碳組成。然而,需要過(guò)量的電解液來(lái)填充碳基體的孔隙,這導(dǎo)致了陰極的電解液與硫(E/S)比率的增加和電池整體能量密度的下降。此外,碳通常是疏水性的,因此被電解質(zhì)浸潤(rùn)得很差--阻礙了離子擴(kuò)散,降低了容量和速率能力。這一缺點(diǎn)在實(shí)際的鋰硫電池中會(huì)被進(jìn)一步放大,這些電池通常在貧電解質(zhì)條件下運(yùn)行,由于在低E/S比率下多硫化物的濃度較高,導(dǎo)致電解質(zhì)粘度增加,因此離子傳輸相當(dāng)緩慢。此外,硫和碳之間的弱相互作用會(huì)導(dǎo)致硫在電解質(zhì)中溶解而流失。因此,鋰硫電池中硫的宿主材料應(yīng)該是高導(dǎo)電性、高密度和可濕潤(rùn)的,最好擁有與硫的強(qiáng)相互作用并具有電催化活性。
【工作介紹】
近日,劍橋大學(xué)Chhowalla Manish、Yang Jieun報(bào)道了的鋰化金屬性二硫化鉬納米片用于高性能鋰硫電池的研究。
作者使用鋰化金屬1T相二硫化鉬(LixMoS2)作為承載硫的無(wú)粘結(jié)劑導(dǎo)電陰極實(shí)現(xiàn)高性能鋰硫電池。過(guò)去研究表明,由金屬1T相MoS2的單層納米片組裝的緊湊型電極具有高導(dǎo)電性、親液性和催化活性。由于改善了對(duì)多硫化鋰的吸附,增強(qiáng)了Li+的傳輸,加速了電化學(xué)反應(yīng)動(dòng)力學(xué),以及卓越的多硫化物轉(zhuǎn)化的電催化活性,這些屬性導(dǎo)致了硫的利用率超過(guò)85%。將這些特性轉(zhuǎn)化為實(shí)用的軟包電池,實(shí)現(xiàn)了8.21 mAh cm-2的面容量和超過(guò)200次循環(huán)85%的容量保持率。基于LixMoS2的安時(shí)級(jí)(1.3±0.05Ah)軟包電池的重量級(jí)能量密度為441 Wh kg-1,體積級(jí)能量密度為735 Wh l-1。
【具體內(nèi)容】
一、LixMoS2的結(jié)構(gòu)和電化學(xué)表征
用丁基鋰化學(xué)方法對(duì)MoS2進(jìn)行化學(xué)剝離,制備了LixMoS2,并從半導(dǎo)電相轉(zhuǎn)化為金屬相。金屬相的LixMoS2可以通過(guò)在溶劑中超聲處理形成穩(wěn)定的分散體而剝離成單層的納米片。
納米片可以很容易地從分散體中重新堆積,以形成自支撐的薄膜。這些LixMoS2薄膜表現(xiàn)出相當(dāng)?shù)?a href="http://www.1cnz.cn/v/tag/1472/" target="_blank">機(jī)械靈活性和強(qiáng)度(圖1a)。圖1b中典型薄膜(1 mg cm-2, ~2.4 μm)的橫截面掃描電子顯微鏡(SEM)圖像顯示了一個(gè)具有密集堆疊的納米片的緊湊層狀結(jié)構(gòu)。在X射線衍射(XRD)圖(圖1c)中,在~7.8°處觀察到一個(gè)新的峰值,對(duì)應(yīng)于由鋰化產(chǎn)生的(001)面。與原始的2H MoS2相比,LixMoS2中的(002)峰也向更高的角度移動(dòng),表明納米片之間的層間距離較小。這歸因于帶負(fù)電荷的1T相MoS2納米片被夾帶的Li+陽(yáng)離子吸引。LixMoS2的拉曼光譜顯示了MoS2通常的A1g和E2g 1峰以及金屬1T相特有的額外的J1、J2和J3峰(圖1d)。如圖1e所示,使用X射線光電子能譜(XPS)發(fā)現(xiàn),鋰化樣品中金屬1T相的濃度為85%。這比非鋰化金屬M(fèi)oS2(表示為1T MoS2)要高,后者通常含有約70%的1T相。

圖1、LixMoS2的形態(tài)和性質(zhì)。
為了研究基于LixMoS2的陰極在鋰硫電池中的電化學(xué)性能,制備了LixMoS2/硫復(fù)合材料(硫>70wt%)并將其組裝到帶有鋰金屬陽(yáng)極的紐扣電池中(方法)。LixMoS2和其他對(duì)照MoS2陰極的恒流充放電(GCD)曲線表現(xiàn)出典型的鋰硫電池行為,分別在2.4V(Li2S6到Li2S4)和2.1V(Li2S4到Li2S2/Li2S)出現(xiàn)了兩個(gè)特征性的放電平臺(tái)(圖2a)。LixMoS2陰極在0.1C時(shí)顯示出1425 mAh g-1的比容量,遠(yuǎn)遠(yuǎn)高于由半導(dǎo)電的2H MoS2(364 mAh g-1)制成的陰極--即使在與導(dǎo)電碳混合后(表示為2H MoS2/C,728 mAh g-1)--以及非鋰化金屬1T MoS2(1179 mAh g-1)。值得注意的是,這一容量表明硫的利用率為85.2%(100%硫利用的理論容量為1,672 mAh g-1)。此外,在這些陰極中,LixMoS2在相同的條件下顯示出最低的極化電壓間隙,這表明在充電/放電過(guò)程中,由于電催化活性的提高,陽(yáng)極/陰極反應(yīng)更早。LixMoS2陰極相對(duì)較好的速率能力(1C時(shí)67%的容量保持率;圖2b)也揭示了其增強(qiáng)的Li+傳輸和反應(yīng)動(dòng)力學(xué)。
圖2c顯示了不同研究的LixMoS2陰極的體積容量和硫負(fù)載的比較。為了實(shí)現(xiàn)鋰硫電池的高容積容量,活性硫材料的堆積密度是至關(guān)重要的。在空隙率較高的多孔碳中,硫通常是松散的,空隙中充斥著電解液,大大增加了電池的整體重量,但對(duì)其容量沒(méi)有幫助。相比之下,緊湊的LixMoS2納米片允許硫被密集地包裝起來(lái),因此,在不影響容量的情況下,可以實(shí)現(xiàn)667g/l的體積載硫量。
因此,該陰極有可能提供950 Ah l-1的體積容量。LixMoS2陰極的低孔隙率也避免了對(duì)過(guò)多電解液的需求,而其出色的潤(rùn)濕性確保了在貧電解液條件下保持高性能。此外,電解液用量的減少和緊湊的硫封閉使多硫化鋰(LiPS)的溶解降到最低,而多硫化鋰會(huì)通過(guò)穿梭效應(yīng)導(dǎo)致容量下降。因此,活性材料固定化的改善使得LixMoS2陰極在1C的條件下循環(huán)500次后的容量保持率達(dá)到91%(圖2d),高于1T MoS2的70%、2H MoS2/C的47%和2H MoS2陰極的22%。

圖2、Li–S扣式電池中不同MoS2基陰極的電化學(xué)表征。
二、LixMoS2宿主在鋰硫化學(xué)中的作用
進(jìn)一步研究了造成LixMoS2陰極優(yōu)異性能的基本機(jī)制。在圖3中總結(jié)的結(jié)果表明,性能的提升主要?dú)w因于三點(diǎn):改善LiPS的吸附(圖3a);增強(qiáng)Li+的傳輸(圖3b,c);以及加速電化學(xué)反應(yīng)動(dòng)力學(xué)(圖3d-f)。這三個(gè)特性也導(dǎo)致了更高的電催化活性,如圖4中系統(tǒng)地描述的那樣,這導(dǎo)致了使用LixMoS2陰極的鋰硫電池的高容量和循環(huán)穩(wěn)定性。

圖3、不同MoS2基陰極的LiPS吸附、Li+傳輸和電化學(xué)反應(yīng)動(dòng)力學(xué)。
首先用Li2S4溶液對(duì)不同的MoS2宿主進(jìn)行了多硫化物吸附測(cè)量,因?yàn)樗徽J(rèn)為是LiPS的重要中間產(chǎn)物。也就是說(shuō),在整個(gè)鋰硫電池反應(yīng)中。S8 + 16e- + 16Li+ 8Li2S;轉(zhuǎn)移的16個(gè)電子中,有12個(gè)來(lái)自Li2S4通過(guò)2Li2S4 + 12e- + 12Li+ 8Li2S轉(zhuǎn)化為最終的Li2S(由相同數(shù)量的硫平衡)--也就是說(shuō),75%的容量來(lái)自這個(gè)步驟。它也對(duì)應(yīng)于最大的放電平臺(tái),約2.1V(圖2a),通常需要最長(zhǎng)的時(shí)間來(lái)進(jìn)行,這意味著Li2S4暴露在電解液中的時(shí)間更長(zhǎng),因此溶解和穿梭的概率更高。
因此,我們認(rèn)為,Li2S4產(chǎn)物的有效吸附對(duì)于同時(shí)促進(jìn)轉(zhuǎn)換過(guò)程(增加容量)和減少穿梭效應(yīng)(增加循環(huán)穩(wěn)定性)至關(guān)重要。圖3a的插圖顯示,大部分Li2S4被吸附在LixMoS2宿主上,留下了比其他宿主更透明的溶液,這一點(diǎn)被紫外-可見(jiàn)光(UV-Vis)光譜學(xué)定量證實(shí)(圖3a)。LixMoS2宿主對(duì)多硫化物的這種更高的親和力可以歸因于其金屬1T相的極性和通過(guò)鋰化引入的額外結(jié)合點(diǎn)。
接下來(lái),通過(guò)使用Randles-Sevcik方程,從循環(huán)伏安法(CV)結(jié)果中得出Li+離子擴(kuò)散系數(shù)(DLi)。CV曲線表現(xiàn)出兩個(gè)陰極峰和一個(gè)陽(yáng)極峰(圖3b)--與圖2a中GCD曲線中觀察到的兩個(gè)放電和一個(gè)充電平臺(tái)很一致。不同掃描速率下的峰值電流被用來(lái)提取不同陰極的DLi(圖3c)。LixMoS2陰極的DLi為5.1 × 10-8 cm2 s-1,比1T MoS2陰極(3.0 × 10-8 cm2 s-1)高出70%,這歸因于金屬M(fèi)oS2納米片之間的鋰的插層,它促進(jìn)了Li+在材料中的傳輸,使LixMoS2具有離子傳導(dǎo)性。這種額外的Li+傳導(dǎo)途徑對(duì)在貧電解質(zhì)條件下的工作有很大貢獻(xiàn)。值得注意的是,由于轉(zhuǎn)化為金屬1T相,LixMoS2陰極中的DLi比2H MoS2/C(4.9 × 10-9 cm2 s-1)高一個(gè)數(shù)量級(jí)。這種DLi的差異解釋了觀察到的基于MoS2的陰極的速率能力的差異(圖2b)。LixMoS2陰極增強(qiáng)的Li+傳輸也顯示在電化學(xué)阻抗光譜(EIS)曲線中(圖3d),其中低頻區(qū)域的較高斜率表明了理想離子擴(kuò)散行為的趨勢(shì)。
然后,我們通過(guò)使用EIS探測(cè)不同陰極上每個(gè)多硫化物轉(zhuǎn)化步驟所需的活化能(Ea)來(lái)研究電化學(xué)反應(yīng)的動(dòng)力學(xué)。測(cè)量是在發(fā)生重要反應(yīng)的電壓和不同溫度下進(jìn)行的。典型的Nyquist圖在2.1V(Li2S4轉(zhuǎn)換的關(guān)鍵步驟發(fā)生的地方)作為一個(gè)例子顯示在圖3d。用插圖中的電路擬合曲線表明,LixMoS2陰極擁有最低的內(nèi)阻(Rs)和電荷轉(zhuǎn)移電阻(Rct)。然后采用Arrhenius方程得到Ea(圖3e),其中電荷轉(zhuǎn)移電阻的倒數(shù)(1/Rct)被用來(lái)代表硫還原反應(yīng)(SRR)的速率,因?yàn)榉磻?yīng)是隨著電荷轉(zhuǎn)移進(jìn)行的。圖3f中總結(jié)了不同電壓下的Ea值。可以看出,對(duì)于每個(gè)陰極來(lái)說(shuō),在2.4V和2.1V的Ea值都高于其相鄰的電壓,這表明這些是關(guān)鍵步驟(2.4V和2.1V也是GCD曲線中兩個(gè)放電平臺(tái)的位置)。特別是2.1V的反應(yīng),對(duì)應(yīng)于從Li2S4到Li2S2/Li2S的轉(zhuǎn)化過(guò)程,在所有電壓中顯示出最高的Ea-表明它是整個(gè)鋰硫電池反應(yīng)的速率決定性步驟。在不同的陰極中,LixMoS2在每個(gè)多硫化物轉(zhuǎn)化步驟中明顯表現(xiàn)出最低的Ea。例如,在2.1V的關(guān)鍵步驟中,LixMoS2陰極的Ea分別比1T MoS2和2H MoS2低~34%和~70%。這歸因于LixMoS2中的插層鋰起到了儲(chǔ)鋰的作用,因此多硫化物可以直接與宿主上的這些局部鋰位點(diǎn)反應(yīng),而不是只與電解質(zhì)中的溶解鋰離子反應(yīng),從而導(dǎo)致更快的動(dòng)力學(xué)。圖3中的結(jié)果表明,LixMoS2陰極的LiPS吸附能力有所提高,同時(shí)Li+的傳輸和反應(yīng)動(dòng)力學(xué)也有所增強(qiáng)。
三、電催化SRR
接下來(lái)系統(tǒng)地分析了不同MoS2宿主在Li2S4轉(zhuǎn)化中的SRR特性,發(fā)現(xiàn)這是需要最高Ea的關(guān)鍵速率決定性步驟。圖4a中的線性掃描伏安法(LSV)曲線顯示,LixMoS2擁有2.12V的起始電位,大大高于1T MoS2(2.03V)、2H MoS2/C(1.95V)和2H MoS2(1.91V)。也就是說(shuō),LixMoS2的過(guò)電位最低,這表明SRR的電催化活性最高。這也被更高的半波電位和更大的擴(kuò)散極限電流密度(JD)所證實(shí)。圖4b顯示了從LSV曲線中獲得的Tafel斜率,該曲線以增加電流密度所需的電位形式描述了電催化劑的反應(yīng)動(dòng)力學(xué)和活性16(以mV dec-1為單位)。LixMoS2表現(xiàn)出比1T MoS2(168 mV dec-1)、2H MoS2/C(195 mV dec-1)和2H MoS2(227 mV dec-1-1)低得多的Tafel斜率(66 mV dec-1),表明電催化活性更高,反應(yīng)動(dòng)力學(xué)加快--與圖3f中測(cè)量的相對(duì)低Ea一致。值得注意的是,盡管具有相似的電化學(xué)活性表面積,LixMoS2的催化活性卻優(yōu)于1T MoS2,這表明鋰化過(guò)程為SRR引入了更多的活性位點(diǎn)。

圖4、使用旋轉(zhuǎn)圓盤電極系統(tǒng)研究Li2S4溶液中不同MoS2主體的電催化硫還原反應(yīng)。
從圖4a中的LSV曲線可以看出,LixMoS2的JD值高于其他對(duì)照MoS2宿主。鑒于在測(cè)量中使用了不同材料的等質(zhì)量負(fù)載,LixMoS2的較高電流表明,在SRR過(guò)程中轉(zhuǎn)移了更多的電子。為了進(jìn)一步研究電子轉(zhuǎn)移,在不同的旋轉(zhuǎn)速率下進(jìn)行了LSV測(cè)量(圖4c),并根據(jù)Koutecky-Levich方程使用結(jié)果JD來(lái)計(jì)算電子轉(zhuǎn)移數(shù)。圖4d中總結(jié)了不同MoS2宿主的電子轉(zhuǎn)移數(shù)。LixMoS2顯示的電子轉(zhuǎn)移數(shù)約為10.6,大于1T MoS2(8.7)、2H MoS2/C(5.5)和2H MoS2(2.8)。考慮到理想情況下Li2S4完全轉(zhuǎn)化為L(zhǎng)i2S需要轉(zhuǎn)移12個(gè)電子,10.6的電子轉(zhuǎn)移數(shù)相當(dāng)于88.3%的轉(zhuǎn)化率,這與使用LixMoS2陰極的紐扣電池獲得的85.1%的硫利用率很一致。LixMoS2促進(jìn)轉(zhuǎn)化為最終產(chǎn)物L(fēng)i2S的這種較高的電催化活性也被恒電位Li2S沉積研究證實(shí)。
上述結(jié)果表明,LixMoS2對(duì)SRR表現(xiàn)出卓越的電催化活性,增強(qiáng)了Li+的傳輸,加速了反應(yīng)動(dòng)力學(xué),并改善了對(duì)LiPS的吸附以減輕穿梭效應(yīng)。此外,插層鋰為L(zhǎng)i2S成核提供了場(chǎng)所,從而使Li2S成長(zhǎng)為粒子團(tuán),而不是沿著表面橫向沉積。這有效地延緩了由絕緣Li2S薄層的均勻覆蓋引起的表面鈍化,從而導(dǎo)致更高的放電容量。LixMoS2宿主的另一個(gè)重要特征是,它們同時(shí)作為導(dǎo)電基底和電催化劑工作。也就是說(shuō),典型的Li-S宿主由分散在導(dǎo)電框架(通常是碳)上的非導(dǎo)電電催化劑(如二氧化錳)組成,這引入了內(nèi)部固-固界面電荷轉(zhuǎn)移阻力--減少了到達(dá)活性點(diǎn)的電子數(shù)量。相比之下,導(dǎo)電的LixMoS2有利于電子傳輸?shù)诫姶呋钚渣c(diǎn),從而使SRR有效進(jìn)行。此外,最近有研究表明,Li+與1T相MoS2具有很強(qiáng)的結(jié)合力,這有利于最大限度地減少LiPS在電解液中的溶解,因此抑制了穿梭效應(yīng)。LixMoS2的離子傳導(dǎo)性使得Li+能夠從宿主材料上的鋰化位點(diǎn)注入多硫化物,也彌補(bǔ)了低E/S比工作條件下電解液的導(dǎo)電性降低。這些優(yōu)點(diǎn)使LixMoS2獨(dú)特地適用于提高鋰硫電池的性能。
四、制造基于LixMoS2的鋰硫軟包電池
在上述發(fā)現(xiàn)的基礎(chǔ)上,作者將基本材料特性轉(zhuǎn)化為高性能的軟包電池,并與最先進(jìn)的儲(chǔ)能裝置(如LIB)進(jìn)行比較。

圖5、基于LixMoS2的Li–S軟包電池的性能。
用LixMoS2陰極和鋰金屬陽(yáng)極制造了軟包電池(尺寸為6厘米×4.5厘米),使用預(yù)先優(yōu)化的E/S比率為2.4μl mg-1。對(duì)于實(shí)用的儲(chǔ)能設(shè)備(例如,軟包電池級(jí)別的鋰硫電池和鋰離子電池),面積容量(Careal)是衡量性能的一個(gè)關(guān)鍵指標(biāo)。在鋰硫電池中,增加Careal的最直接的方法是增加面積硫的負(fù)載。然而,負(fù)荷的增加通常伴隨著較厚的電極上離子擴(kuò)散的遲緩,導(dǎo)致比容量的下降,從而導(dǎo)致Careal的下降。圖5a說(shuō)明了這種權(quán)衡。從圖5a中可以看出,本工作中,當(dāng)硫含量為7.5 mg cm-2時(shí),Careal是最優(yōu)化的(陰極中的硫含量保持在71.4 wt%不變),達(dá)到了8.21 mAh cm-2的Careal。超過(guò)8 mAh cm-2的Careal是迄今為止報(bào)告的鋰硫軟包電池的最高值之一(圖5b),并大大超過(guò)了商業(yè)鋰離子電池的基準(zhǔn)值3 mAh cm-2。
此外,基于LixMoS2的軟包電池表現(xiàn)出卓越的速率能力(圖5b),即使在5 mA cm-2的高電流密度下(相當(dāng)于在1小時(shí)內(nèi)完成快速充電過(guò)程)也能保持超過(guò)4 mAh cm-2。
能量密度也被廣泛用作評(píng)估整體設(shè)備性能和在不同的電池系統(tǒng)之間進(jìn)行比較的指標(biāo)。然而,文獻(xiàn)中報(bào)道的原型電池往往擁有比實(shí)際電源所需的總?cè)萘康停?1 Ah)。例如,大多數(shù)商業(yè)電池在1-2Ah或更高的容量水平上運(yùn)行。因此,比較在Ah水平下運(yùn)行的電池的能量密度是更有意義的。為此,我們通過(guò)堆疊多層電極組裝了Ah級(jí)Li-S軟包電池,實(shí)現(xiàn)了1.33 Ah的總?cè)萘俊N覀兊腁h級(jí)軟包電池與最先進(jìn)的儲(chǔ)能技術(shù),如LIBs、Li-S電池和鉛酸電池之間的能量密度比較見(jiàn)圖5c。可以看出,基于LixMoS2的軟包電池同時(shí)提供了441 Wh kg-1的高重力能量密度和735 Wh l-1的體積能量密度。這些能量密度是迄今為止報(bào)告的鋰硫軟包電池中最高的,并且相對(duì)于商業(yè)鋰硫和LIB系統(tǒng),包括商業(yè)制造商的鋰硫電池和LFP、NCM 811、NCM622和NCA,分別來(lái)自比亞迪、CATL、LG和松下。
電池的循環(huán)壽命是現(xiàn)實(shí)世界可行性的另一個(gè)關(guān)鍵參數(shù)--特別是對(duì)于通常不像鋰離子電池那樣穩(wěn)定的鋰硫電池。本工作的軟包電池在200次循環(huán)后表現(xiàn)出85.2%的容量保持率,相當(dāng)于每循環(huán)的容量衰減只有0.074%。這樣的循環(huán)穩(wěn)定性優(yōu)于許多以前的報(bào)告值,甚至可以與商業(yè)電池相媲美。例如,iPhone手機(jī)中的LIB被設(shè)計(jì)為可以在超過(guò)200個(gè)完整的充電周期內(nèi)保持其80%的原始容量。我們基于LixMoS2的鋰硫軟包電池的這些結(jié)果顯示了下一代儲(chǔ)能裝置的潛力。
【結(jié)論】
該工作報(bào)告了一種硫宿主材料--鋰化二維金屬M(fèi)oS2納米片,它可以實(shí)現(xiàn)高性能的鋰硫電池。LixMoS2中的插層鋰為改善多硫化物的吸附引入了結(jié)合點(diǎn),為增強(qiáng)Li+的傳輸提供了傳導(dǎo)途徑,并作為鋰源以實(shí)現(xiàn)更有效的電化學(xué)反應(yīng)動(dòng)力學(xué)。這些特性共同緩解了貧電解質(zhì)對(duì)鋰硫化學(xué)的影響。因此,使用本工作的陰極材料可以實(shí)現(xiàn)重量級(jí)能量密度為441 Wh kg-1和體積級(jí)能量密度為735 Wh l-1的Ah級(jí)鋰硫軟包電池。該設(shè)計(jì)原則可應(yīng)用于更廣泛的同時(shí)需要電和離子導(dǎo)電性和電催化活性的材料。
【材料制備方法】
LixMoS2和對(duì)照樣品的制備
LixMoS2是通過(guò)將散裝MoS2粉末(2H MoS2與有機(jī)鋰試劑插層合成的。在氬氣下將散裝MoS2粉末(0.3g)浸入正己烷(15ml)中;接下來(lái)將正丁基鋰溶液(2.5M的正己烷,2ml)加入混合物中,然后回流2天。冷卻后,用正己烷(3×50ml)洗滌該產(chǎn)物,以除去剩余的有機(jī)鋰調(diào)節(jié)劑和有機(jī)殘留物。所得的LixMoS2粉末被干燥并儲(chǔ)存在惰性氣氛下以避免氧化。1T MoS2的制備方法是將LixMoS2粉末在去離子水(1mg ml-1)中超聲處理30分鐘,然后離心去除鋰陽(yáng)離子。2H MoS2/C是通過(guò)球磨2H MoS2與Super P碳以9:1的質(zhì)量比制備的。
用于陰極的MoS2樣品/硫復(fù)合材料的制備
LixMoS2(LixMoS2/S)和1T MoS2(1T MoS2/S)的硫復(fù)合材料是通過(guò)共沉淀法制備的,以避免在常用的熔融擴(kuò)散法中進(jìn)行高溫退火造成的部分相變(從1T到2H)。
將LixMoS2(20mg)和升華硫(50mg)粉末在超聲的幫助下分散在二硫化碳溶液(5.0M的THF,20ml)中。然后將分散液在陽(yáng)極氧化鋁膜(孔徑0.02μm)上過(guò)濾,接著在室溫下真空干燥。面積硫含量與薄膜的厚度成正比,由相同濃度的分散體的數(shù)量來(lái)調(diào)整。體積含硫量是在面積含硫量和相應(yīng)的薄膜厚度的基礎(chǔ)上計(jì)算的。LixMoS2和升華硫之間的質(zhì)量比為1:2.5(硫比例=71.4 wt%)。作為對(duì)照,裸露的LixMoS2薄膜也是在沒(méi)有硫的情況下制備的。1T MoS2/S的制備過(guò)程類似,但將溶劑改為乙醇。其他硫復(fù)合材料(即2H MoS2/S和2H MoS2/C/S)是通過(guò)熔融擴(kuò)散法制備的。首先,將2H MoS2或2H MoS2/C(100mg)與升華硫(250mg)一起進(jìn)行球磨,以獲得細(xì)粉。然后將混合物密封在氬氣下的特氟隆高壓釜中,并在155℃下保持12小時(shí)。在自然冷卻到室溫后,收集硫復(fù)合材料。
審核編輯 :李倩
-
鋰離子電池
+關(guān)注
關(guān)注
85文章
3338瀏覽量
78777 -
納米
+關(guān)注
關(guān)注
2文章
708瀏覽量
38267 -
能量密度
+關(guān)注
關(guān)注
6文章
288瀏覽量
16854
原文標(biāo)題:Nature Energy:鋰化二硫化鉬納米片用于高性能鋰硫電池
文章出處:【微信號(hào):清新電源,微信公眾號(hào):清新電源】歡迎添加關(guān)注!文章轉(zhuǎn)載請(qǐng)注明出處。
發(fā)布評(píng)論請(qǐng)先 登錄
復(fù)旦彭慧勝/高悅Nature新突破:外部補(bǔ)鋰技術(shù)革新電池性能破解缺鋰難題

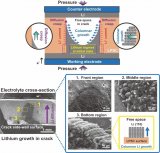
清華大學(xué):自由空間對(duì)硫化物固態(tài)電解質(zhì)表面及內(nèi)部裂紋處鋰沉積行為的影響
北航&北大《Nature》:連續(xù)化制備高性能納米復(fù)合薄膜材料的新突破

利用拉曼光譜測(cè)量二硫化鉬薄片層數(shù)的三種方法
北京大學(xué)龐全全硫基電池再發(fā)Nature:硫化物基全固態(tài)鋰硫電池
王東海最新Nature Materials:全固態(tài)鋰硫電池新突破

篩選理想的預(yù)鋰化正極應(yīng)用于無(wú)負(fù)極金屬鋰電池

原位焊接離子導(dǎo)電斷點(diǎn)以實(shí)現(xiàn)高度可逆的全固態(tài)鋰硫電池

全固態(tài)鋰金屬電池的鋰陽(yáng)極夾層設(shè)計(jì)
物聯(lián)網(wǎng)行業(yè)中的常用電池方案_鋰錳電池
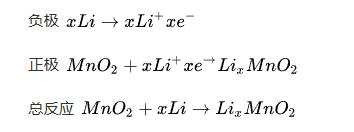
LTO充電小型鋰二次電池解決方案


















評(píng)論