血小板是生理性止血和病理性血栓形成的核心參與者。機械血流參數(血液動力學)是血小板信號轉導和功能的重要驅動因素。心血管疾病和/或影響其功能的血液接觸醫療器械會引起血小板各種血液動力學的變化,包括狹窄部位的壁面剪切應力/應變的增加;附著在血管壁、血栓或醫療器械表面上的拉伸力和壓縮力的變化;以及由于紅細胞著邊和流動再循環引起的區域內質量傳輸現象。血小板將這些外部機械信號轉導為細胞內生化信號(機械轉導)。這些不同的機械轉導機制的關鍵聯系是細胞溶質鈣[Ca2?]c通量,它整合了不同的信號轉導途徑并驅動相關的血小板激活事件,例如血小板形狀變化和整合素αIIb β?的激活。
目前,已有多種技術被用于進行血小板機械轉導機制的研究,包括錐板和平行板流變測定法、微流控層析法、基于剛性和可變形彈性基板的靜態粘附測定法,以及微量移液器抽吸或磁珠牽引法。然而,這些技術雖然可用于粘附受體介導的血小板機械轉導機制研究,但無法用于缺乏粘附受體或表面粘附作用的自由流體中血小板機械轉導機制的研究。此外,常見的基于流體流動的技術,例如微毛細管技術、直通道微流控技術和平行板技術,通常涉及混合動力學(包含剪切和拉伸分量),并且相關的研究大多數只關注壁面剪切效應。為了更準確地定義驅動血細胞和血小板行為的血液動力學參數,相關研究方法逐漸由使用可以提供穩態層流剪切流的簡單直通道轉變為使用更復雜的幾何結構,例如階梯式微收縮幾何結構、具有復雜分叉微通道的微流控系統、交叉槽式裝置和雙曲線收縮結構。
據麥姆斯咨詢報道,近期,來自澳大利亞莫納什大學(Monash University)、墨爾本大學(The University of Melbourne)以及皇家墨爾本理工大學(RMIT University)的研究人員聯合提出了一種雙曲線微流控測定方法,用于研究不同拉伸應變狀態下血小板的激活。通過理論計算和實驗方法的結合,該研究探索了瞬時和時間相關的拉伸應變動力學對血小板Ca2?信號和機械轉導方式的影響。此外,通過使用5個具有不同幾何結構的雙曲線微流控測定系統,該研究明確了觸發最大血小板[Ca2?]c通量的拉伸應變上限。最后,該研究進行了藥理學概念驗證實驗,闡明了血小板肌動蛋白細胞骨架和環狀微管在血小板拉伸應變傳感(ε˙-S)中的作用。相關研究成果以“A microfluidic method to investigate platelet mechanotransduction under extensional strain”為題發表于Research and Practice in Thrombosis and Haemostasis期刊。
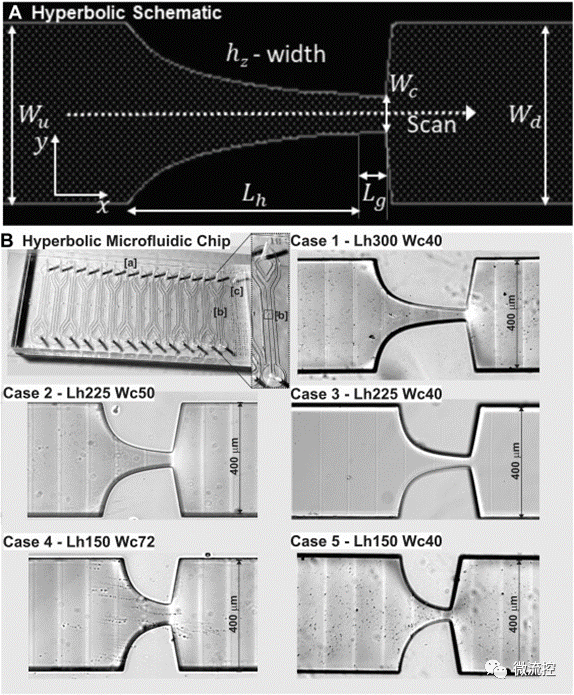
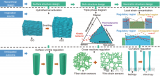
雙曲線微流控芯片的設計
研究結果表明,在缺乏典型粘附的情況下,受體介導的血小板對747/s~3319/s范圍內的拉伸應變率的初始增加和隨后的減少高度敏感。此外,研究證明血小板可快速響應拉伸應變的變化率,且其閾值為7.33 × 10?/s/m,最佳范圍為9.21 × 10?/s/m~1.32 × 10?/s/m。此外,該研究證明了基于肌動蛋白的細胞骨架和環狀微管在調節拉伸應變介導的血小板機械轉導中的關鍵作用。
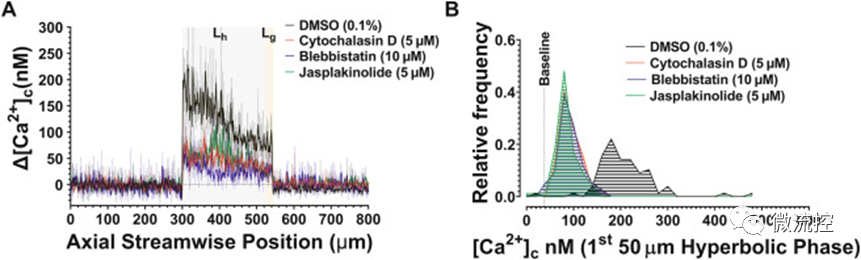
血小板拉伸應變傳感(ε˙-S)過程中[Ca2?]c通量受肌動蛋白細胞骨架動力學調節
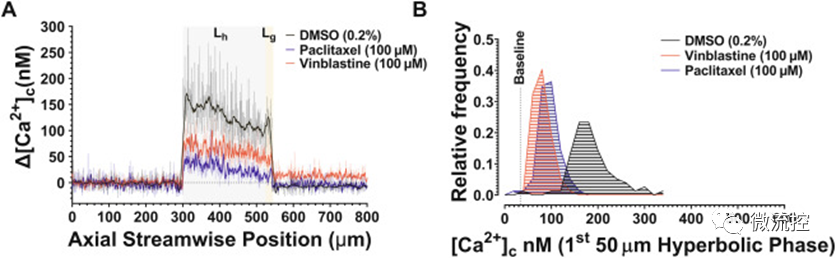
血小板拉伸應變傳感(ε˙-S)過程中[Ca2?]c通量受微管動力學調節
總體而言,該研究開發了一種雙曲線微流控測定方法,用于在定義的準均勻拉伸應變率下評估血小板機械轉導。通過改變雙曲線微流控芯片的幾何結構和輸入流速,該測定方法可以用于探索適用于生理和病理血流環境下的不同拉伸應變機制。這種方法打開了一個新的血小板信號轉導機制研究的窗口,并且可能在識別易患與高度動脈狹窄相關的血栓栓塞并發癥的患者或在其中拉伸應變率是主要血液動力學驅動因素的機械循環支架(MCS)系統中具有潛在的診斷效用。在未來的研究中,研究人員的目標是利用所描述的方法進一步探索支持拉伸應變傳感(ε˙-S)的信號轉導過程。更好地理解這種新型的不依賴于粘附作用的信號轉導機制可能會促進抗血小板療法的新發展,這些療法專門針對超生理血流動力學,可最大限度地降低全身出血的風險,并在與醫療器械相關的血栓形成管理方面優于目前的療法。
論文鏈接: https://doi.org/10.1016/j.rpth.2023.100037
審核編輯 :李倩
-
醫療器械
+關注
關注
19文章
823瀏覽量
51430 -
微流控
+關注
關注
16文章
526瀏覽量
18886
原文標題:雙曲線微流控測定方法,用于拉伸應變下血小板機械轉導機制研究
文章出處:【微信號:Micro-Fluidics,微信公眾號:微流控】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
常用的微流控芯片類型
北海道大學:基于ZnO納米粒子激光誘導石墨烯的超靈敏可拉伸應變傳感器
微流控陣列芯片和普通芯片的區別
南京大學:高靈敏度和高線性度的可拉伸應變傳感器的分層結構設計
ASML、恩智浦等半導體企業尋求荷蘭新一屆內閣強化芯片投資;歌爾股份撤訴,與敏芯股份5年專利拉鋸戰落幕




 雙曲線微流控測定方法,用于拉伸應變下血小板機械轉導機制研究
雙曲線微流控測定方法,用于拉伸應變下血小板機械轉導機制研究










評論