研究背景
目前現有的基于碳酸酯的最先進電解質無法滿足極限鋰離子電池(LiNi0.8Mn0.1Co0.1O2 (NMC811)||石墨鋰)的大部分要求,如期望具有支持較高電壓(≥4.5伏)、快速充電(≤15分鐘)、寬溫度范圍(±60攝氏度)充放電(不鍍鋰)和不可燃性的能力。因為沒有有效的可以概括此類電解質中電池性能、溶劑化結構和固體電解質-相間化學之間關系的原則來指導電解質的設計。
成果簡介
近日,美國馬里蘭大學王春生教授,美國陸軍實驗室Oleg Borodin教授聯合提出了一種基于一系列軟溶劑的電解質設計方案,該策略在弱Li+溶劑相互作用、足夠的鹽解離和所需的電化學之間取得平衡,以滿足所有上述要求。值得注意的是,4.5伏NMC811||石墨硬幣電池的面積容量超過2.5毫安小時每平方厘米,當這些電池在- 50攝氏度(- 60攝氏度)以0.1C的C速率充放電時,保留了75%(54%)的室溫容量。而NMC811||石墨袋電池與低電解質(2.5克每安培小時)實現穩定的循環,平均庫侖效率超過99.9%在?30攝氏度。綜合分析進一步揭示了NMC811陰極與石墨陽極之間的阻抗匹配,這是由于形成了相似的富氟化鋰界面,從而有效地避免了低溫鍍鋰。這種電解質設計原則可以推廣到在極端條件下工作的其他堿金屬離子電池。
研究亮點
1. 在本文中,作者提出了獨特的平衡電解液設計原則,即取具有適中的DN值和介電常數的溶劑,滿足該條件可使得電池應用于極端條件。這可以使Li+與溶劑的結合能最低且鋰鹽解離性最高。
2. 加入具有高還原電位的MDFSA作為共溶劑,進一步降低Li+的溶劑化程度,促進富LIF的SEI和富lif的CEI的形成。
3.正極和負極的熱力學(容量)和動力學(阻抗)匹配使實際面積容量超過2.5 mAh cm-2的NMC811||石墨電池具有在較寬的溫度范圍內(-60℃~60℃)進行快速充放電的能力,無需鍍鋰。
4. 全電池在-30℃的溫度條件下進行300次循環后仍保持超過83%的容量,平均庫倫效率超過99.9%。
圖文導讀
首先作者建立了平衡電解質的設計原則,溶劑選擇有兩個標準,第一個是低冰點、適中沸點和較寬的電化學穩定窗口,第二個是軟溶劑化能力,確保低Li+離子脫溶能,同時不犧牲離子解離能力,如圖1a所示。根據圖1b,c大多數已知的具有高鹽解離能力的極性溶劑具有高DN(》10)(圖1b中的I和II區)16,17,具有低DN和低介電常數的極性溶劑具有較差的鹽解離能力(圖1b,c中的III區),代表非溶劑化稀釋劑。其中存在一個平衡區域(IV區),由具有中等介電常數的低DN溶劑組成,導致中等的Li+—溶劑結合能和鹽解離。由上述標準選定了一個氟化酯族(二氟乙酸乙酯(EDFA), 2,3,3,3-四氟丙酸甲酯(M4FP),二氟乙酸甲酯(MDFA)和2,2-二氟-2(氟磺酰)乙酸甲酯(MDFSA);圖1d所示的化學結構)作為溶劑,因其氟化酯溶劑(MDFA、EDFA和M4FP)具有更寬的電化學穩定窗口,更高的熱穩定性和超低冰點,其中甲基(3,3,3-三氟哌酸鹽)(M3FP)先前在- 60°C低溫下已在鋰金屬電池中顯示出較好的結果。
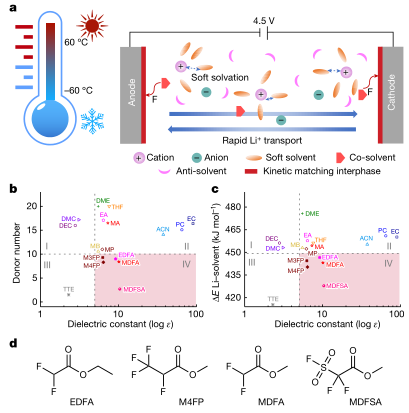
圖1 |電解質設計策略。a,說明了軟溶劑與Li離子之間的軟溶劑化,鋰離子的快速遷移和寬溫度范圍(±60°C)的穩定性。b, DN與介電常數的溶劑關系圖。位于IV區的溶劑稱為軟溶劑,其中較低的DN和較高的介電常數有效地降低了Li+—溶劑的親和力,而不犧牲動力學遷移。c, DFT計算的Li+ -溶劑結合能與實驗介電常數的關系。雨,乙腈;DMC,碳酸二甲酯;測距裝置,乙二醇二甲醚;EA,乙酸乙酯;EC,碳酸乙烯;MB,丁酸甲酯;MP,丙酸甲酯;PC,碳酸丙烯;四氫呋喃(四氫呋喃。d,軟溶劑化溶劑的化學結構。
為了最大限度地提高離子導電性,軟溶劑需要與高解離性和可溶解性鋰鹽相結合。LiTFSI具有較高的解離性和較弱的Li+結合能,在MDFA、EDFA和M4FP溶劑中的溶解度分別為5.0 M、4.5 M和3.0 M,是較好的選擇。
軟溶劑化溶劑本質上有利于在溶液中形成主要的離子對和聚集體,因此也促進富氟化鋰(LiF)固體電解質界面相(SEI)和正極電解質界面相(CEI)的形成。加入2.2 V高還原電位的MDFSA作為共溶劑(氟磺酰基取代的二甲基二甲基呋喃;分子結構如圖1d所示),進一步降低Li+的溶劑化程度,促進富lif的SEI和富lif的CEI的形成。當TTE在混合溶劑中的體積比超過40%時,加入1,1,2,2-四氟乙基-2,2,3,3-四氟丙基醚(TTE)稀釋劑可使電解質不易燃。
在SEI自限形成過程中,增加LiF含量有望降低其厚度,即使在低溫下也會降低區域特定電阻。在不同電流和溫度下,SEI和CEI相似的富含lif的成分也改善了石墨陽極和NMC811陰極之間的過電位、容量和動力學匹配,允許最大的電池容量和通過控制電池電壓防止Li0電鍍。相比之下,傳統碳酸鹽電解質中形成的無機-有機SEI/CEI導致陽極和陰極之間的容量不匹配和過電位,從而影響了全電池的高速率和低溫性能。
其次作者探索了選擇電解質的理化性質和溶劑化結構。將LiTFSI溶解到不同溶劑中后,利用拉曼光譜對TFSI?···Li+配位進行了表征。由圖2a可知MDFA具有最低的溶劑化能力,LiTFSI鹽濃度的增加和TTE的加入進一步降低了Li+ -溶劑配位,導致離子聚集增加。利用核磁共振(NMR)探索電解質在不同溶劑(乙酸甲酯(MA)、EDFA、MDFA和M4FP)下的溶劑化結構。M4FP最小的Δδ為2.0 ppm(圖2b)與Li+ -溶劑最弱的相互作用直接相關,與DN值一致。對所制備的電解質的離子電導率進行了測試如圖2c所示。正如上文所述,M4FP基電解質的離子電導率最低,因為它具有最低的DN和介電常數。在20℃時,EDFA、MDFA和M4FP的離子電導率分別為1.8 mS cm?1、1.7 mS cm?1和0.6 mS cm?1,略低于EC/DEC電解質(6.4 mS cm?1)。然而,如圖2C所示,由于電解質凝固(圖2d),在低于- 20°C的溫度下,mdfa基電解質的離子電導率優于EC/DEC電解質。綜合考慮Li+—溶劑結合能、離子電導率、電化學穩定窗口等因素,選擇1m LiTFSI MDFA/ MDFSA-TTE電解液進一步探索可能性。利用x射線對分布函數(PDF)進一步分析了1 M LiTFSI MDFA/ MDFSA-TTE電解質的溶劑化結構。實驗結果與分子動力學(MD)在實(R)空間(圖2e)模擬結果吻合較好。MD模擬箱的快照(圖2f)表明TTE和MDFA的加入促進了離子聚集。在混合MDFA/MDFSA - tte溶劑電解質中,Li+主要由1.92個MDFA和1.66個TFSI?離子配位,MDFSA貢獻0.09個(圖2g)。
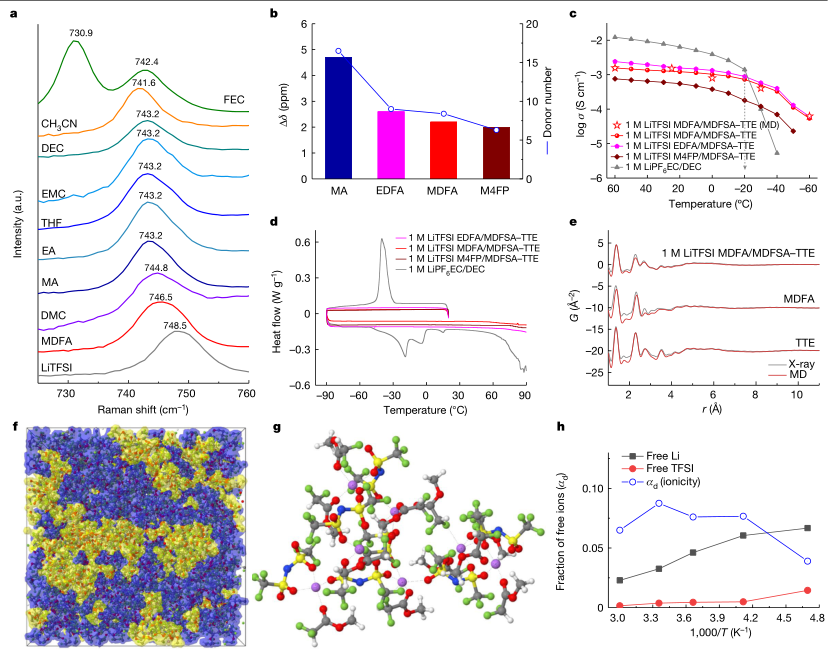
圖2 |電解質的物理性質。a, 1 M LiTFSI在不同溶劑中的拉曼光譜。b,在不同溶劑中含LiTFSI和不含LiTFSI的Δδ(羰基碳的13C NMR譜)的總結。c,不同電解質導電性的溫度依賴性。紅色星號為不同電解質MD. d、DSC冷卻和加熱曲線預測的電導率值。e, 1 M LiTFSI MDFA/ MDFSA-TTE電解質和單一溶劑的PDF數據。灰線,實驗數據;紅線,MD模擬預測。f-h, MD仿真結果。f, 1m MDFA/ MDFSA-TTE仿真盒快照。LiTFSI-MDFA為黃色等值面,TTE和MDFSA為藍色等值面。g, 25°C時MD模擬的代表性離子聚集體。Jmol采用的配色方案有:Li紫色;N,藍色;F,綠色;S,黃色;C、灰色;O,紅色;H,白色。h,游離Li+和TFSI的分數-定義為在5.0 ?范圍內不與Li - n (TFSI)的任何反離子配位的離子,以及MDFA/ MDFSA-TTE電解質中1 M LiTFSI的動力學不相關運動ad(離子性)的程度。
接著作者探索了4.5 v NMC811||石墨全電池的電化學性能。圖3a顯示,1 M LiTFSI MDFA/ MDFSA-TTE電解質的全電池性能優于EC/ DEC電解質。1 M LiTFSI MDFA / MDFSA-TTE電解質經過400次循環后顯示容量保留80.1%,平均CE為99.94%。與1M LiPF6 EC/DEC相比,唄性能的改善如圖3b所示,1C時的容量為202 mAh g?1,2C時的容量185 mAh g–1,3C時的容量169 mAh g-1,4C時的容量140 mAh g-1(此處,C速率由充電時間決定,1C等于1小時,依此類推)。使用1M LiTFSI MDFA/MDFSA–TTE的不同C下電池的相應充電/放電電壓曲線如圖所示3c。
NMC811||石墨全電池在低溫下也表現出優異的性能。圖3d顯示了在?30°C時,260次循環后仍能保留93.9%的容量,平均CE為99.98%。在低至?50°C/?60°C的溫度下,觀察到容量衰減略快。圖3e比較了NMC811||石墨全電池在兩種不同溫度下的性能。?30°C下EC/DEC電解液凝固不能在工作,而1M MDFA/ MDFSA-TTE電解質的NMC811||石墨全電池在低溫下的容量顯示出較高的容量:在0°C、?20°C、?30°C、?40°C、?50°C和?60°C循環時,容量分別為206.8 mAh g?1(95%)、194.5 mAh g?1(90%)、188.7 mAh g?1(87%)、184.6 mAh g?1(85%)、161.0 mAh g?1(75%)和115.5 mAh g?1(54%)。圖3f為1 M LiTFSI MDFA/ MDFSA-TTE電解質在不同溫度下全電池的代表電壓曲線。此外使用1 M MDFA/ MDFSA-TTE電解液的NMC811||石墨全電池,即使在- 60°C的超低溫操作后,也能在25°C完全恢復原始容量。
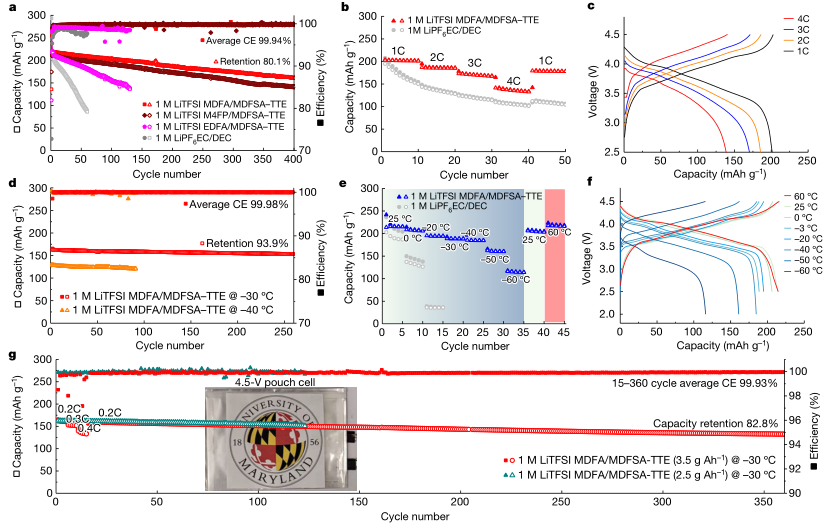
圖3 NMC811||石墨全電池的電化學性能。a、25°C下0.5C時的循環性能。b, c,利率表現在25°C (b)和相應的電壓概要文件(c), d-f長循環性能在0.2C,-30°c /?40°c (d),循環性能在不同溫度下0.1攝氏度(60°C, 25°C, 0°C,-20°C,?30°C,-40°C,?50°C和?60°C) (e)和相應的電壓概要文件使用1 M細胞e LiTFSI MDFA / MDFSA-TTE電解質(f)。g,囊細胞性能?30°C和速度0.2C使用2.5 g Ah?1或3.5 g Ah?1電解質。使用3.5 g Ah?1電解質(紅色)的電池在不同的C速率下(0.5C循環,0.3C循環,0.4C循環5次,0.2C循環345次)進行速率性能測試。插圖:4.5V電池的照片。
最后作者進行了循環后電極界面化學表征
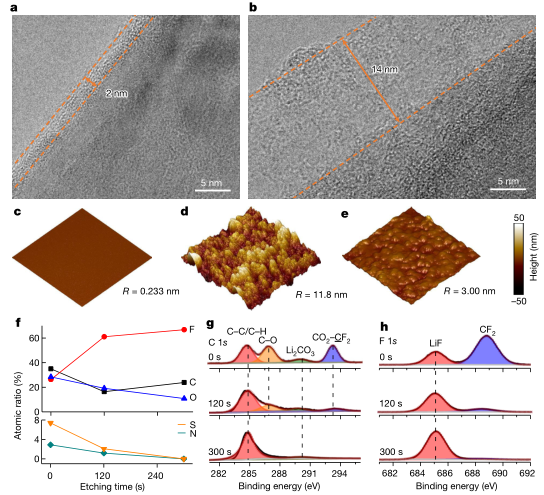
圖4 ?30℃循環后石墨陽極上SEI層的表征。a,b,含有1 M LiTFSI MDFA/ MDFSA-TTE電解質(a)和1 M LiPF6 EC/DEC電解質(b)的HRTEM圖像。橙色虛線用于勾勒出循環石墨陽極上的SEI。c - e,在1 M LiPF6 EC/DEC電解質和1 M LiTFSI MDFA/ MDFSA-TTE電解質中循環前(c)和循環后(d)的石墨電極形貌(e)。在0.5 μm × 0.5 μm面積上的AFM粗糙度(R)比較。f - h, 1 M LiTFSI MDFA/ MDFSA-TTE電解質中循環石墨SEI的XPS結果:定量SEI中元素的原子比(f),相應深度剖析結果的列中顯示C 1s (g)和f 1s (h)光譜。
為了確定界面化學性質,作者系統地研究了石墨陽極上SEI的形貌和組成。
在高分辨率透射電子顯微鏡(HRTEM)下,在MDFA/MDSFA基電解質中循環20次后,在石墨陽極上觀察到均勻而薄的約2 nm的SEI(圖4a)。如此低的厚度體現了基于LIF的界面相在絕緣電子隧穿中的有效性。相比之下,EC/DEC基電解質的SEI層要厚得多,約為14 nm(圖4b)。利用電化學原子力顯微鏡(AFM)研究了SEI的粗糙度和厚度。如圖4c-e所示,原始石墨顆粒表面光滑,粗糙度約為0.233 nm。AFM得到的MDFA/MDSFA基電解液中循環石墨的粗糙度增加到約3.0 nm(圖4e) 與HRTEM觀察結果一致,遠小于EC/ dec基電解液中約11.8 nm的粗糙度(圖4d)。
為了鑒定循環石墨陽極上SEI的化學成分,采用了x射線光電子能譜(XPS)和Ar+濺射深度分析。從1 M LiTFSI MDFA/ MDFSA-TTE電解液中回收的石墨SEI中檢測到的元素及其相關原子比如圖4f所示,C 1s和F 1s光譜分別如圖4g和圖4h所示,可以得出在該電解質中形成了一個內層富含LiF,外層富含有機物的堅固的雙分子層SEI。
總結與展望
在該篇論文中,作者建立了在極端條件下工作的高能電池的電解質設計原則。該原理的核心是識別具有相對較低DN(小于10)和高介電常數(大于5)值的溶劑,這將最小化Li+ -溶劑結合能,同時仍能解離鋰鹽。該設計原理為高電壓、快速充電和寬溫度工作電池開辟了方向。
審核編輯 :李倩
-
鋰離子電池
+關注
關注
85文章
3288瀏覽量
78579 -
電解質
+關注
關注
6文章
821瀏覽量
20528 -
電解液
+關注
關注
10文章
860瀏覽量
23396
原文標題:王春生教授nature:用于極端工作條件下的鋰電電解液設計
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
電解液電容器老化電壓與電解液火花電壓的關系
電解液——鋰電池的‘血液’
現在的鋰電池都是用什么樣的電解液?電解液里加入什么添加劑?
鋰電池電解液價格走勢
電解液寬溫性能的影響因素和寬溫電解液研究進展



















評論