真菌和細菌是生態系統正常運轉的關鍵因素。由于簡單的細胞結構、快速的生長能力及成熟的基因操作,一些真菌和細菌(如釀酒酵母、大腸桿菌等)已作為模式生物被廣泛用于細胞衰老、基因組學及代謝組學的研究。然而,細胞的異質性、環境脅迫適應機制、菌落內細胞相互作用等問題要求更靈活的研究方法實現細胞至亞細胞水平的分析。
微流控芯片,作為操作微尺度流體的高效平臺,可集成梯度發生器、電極陣列和液滴生成結構等多種功能單元,用于捕獲、固定和培養細胞,也可耦合熒光成像、拉曼光譜、電阻抗等檢測技術獲取細胞的生物物理特性和動態行為信息。
據麥姆斯咨詢報道,基于上述技術,東南大學電子科學與工程學院、集成電路學院、MEMS教育部重點實驗室朱真教授課題組發表了集成微流控系統在真菌和細菌生化分析研究進展的綜述文章。
該綜述文章詳細介紹了用于真菌及細菌操縱的典型微流控結構,分析了檢測技術的集成模式、優缺點及主要應用場景。結合不同的微流控結構和檢測技術,總結了集成微流控系統在生物分子檢測、表型分析、濃度測量及抗生素敏感性測試等方面的研究進展,給出了當前集成微流控系統的不足之處及未來發展趨勢。
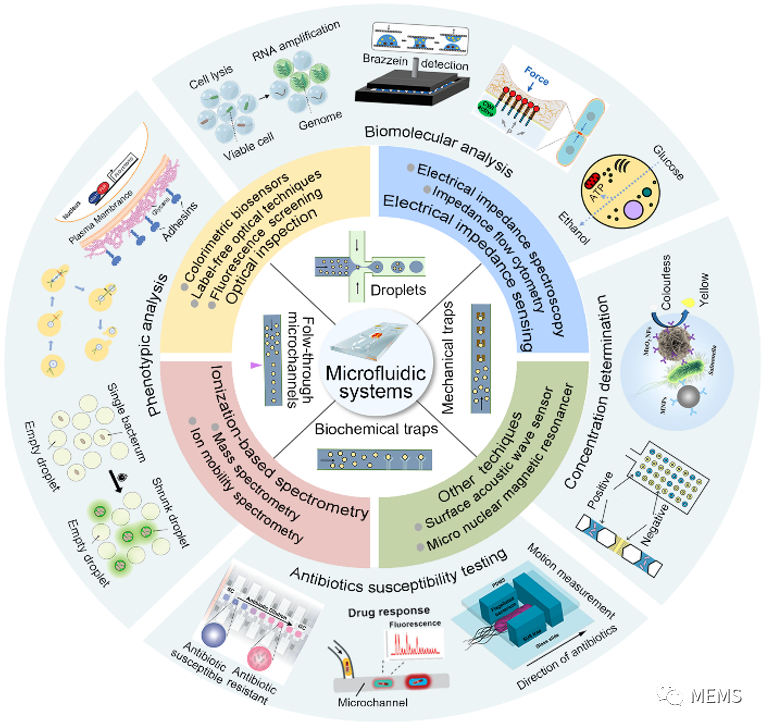
圖1 集成功能單元及檢測技術的微流控系統用于真菌和細菌分析
相關工作以“Recent advances of integrated microfluidic systems for fungal and bacterial analysis”(《用于真菌和細菌分析的集成微流控系統的最新進展》)為題發表在國際著名期刊TrAC-Trends in Analytical Chemistry上。

首先,作者們綜述了三種用于真菌及細菌操縱的微流控結構。第一種是微流控通道,通常為交錯網絡結構,可結合流體動力、聲場、光鑷或其它物理場實現樣品分離、聚焦、篩選。第二種是微屏障、微腔室等物理結構或生化探針表面形成捕獲陷阱,用于固定樣品并進行原位、實時跟蹤觀察。第三種是微液滴,通過同軸型、T型、流動聚焦型微流道結構包裹樣品生成多種尺寸的油-水液滴,結合親疏水圖案、蛇形通道、圓形阱陣列等微結構捕獲并孵育微液滴,或利用電極陣列實現液滴的可控融合。近幾年興起的多孔水凝膠微液滴允許液滴內外部之間的小分子雙向傳輸,在液滴介質交換上具有顯著的優越性。
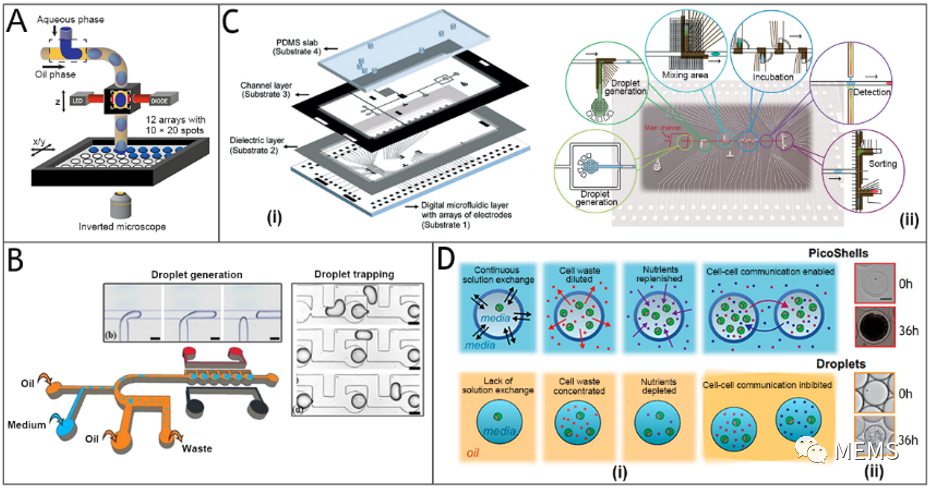
圖2 液滴微流控用于細菌和真菌的樣品捕獲、孵育、融合
隨后,作者們綜述了可集成于微流控系統的檢測技術。主要包括:
(1)光學檢測技術,如熒光檢測、傅里葉變換紅外光譜、拉曼光譜及比色生物傳感,通常集成在芯片外部,實現寬范圍化合物的非侵入式高靈敏檢測。熒光檢測技術是目前為止使用最廣泛的分析技術。
(2)電阻抗傳感,主要包括阻抗流式細胞儀(IFC)和電阻抗譜(EIS)。寬頻段的阻抗譜可以揭示細胞、細胞膜、細胞器的生物物理信息。
(3)電離質譜法,主要通過電噴霧電離、基質輔助激光解吸離子化技術處理微流體,后引入質譜儀和離子遷移譜儀精準檢測微量目標物。
(4)聲表面波(SAW)傳感器及微核磁共振技術的集成方式及應用也被探討。
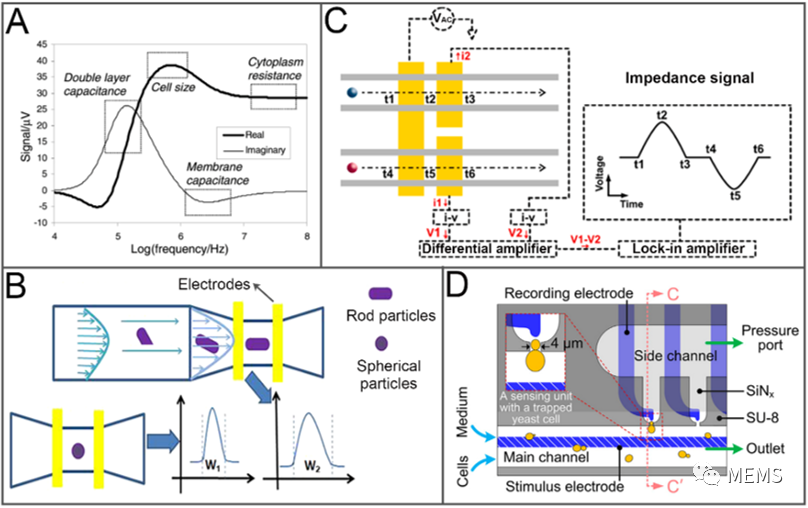
圖3 電阻抗傳感用于真菌和細菌的阻抗信號檢測
此外,作者們總結了近三年集成細胞操縱和檢測技術的微流控系統在細菌和真菌分析中的應用及研究進展:
(1)生物分子檢測。微液滴的超高通量及高置信度細胞分離用于微生物的單細胞基因測序,稱為Drop-Seq,其中聚合酶鏈式反應、多重置換擴增和環介導等溫擴增技術用于獲取足量的核酸。物理捕獲陷阱、微液滴用于研究細胞壁跨膜蛋白、胞內核-液泡連接蛋白等生物分子對機械力、滲透壓、營養底物環境壓力的響應。微腔室及微液滴內真菌和細菌分泌的重組蛋白及代謝物也被成功定量分析。
(2)細胞表型分析。研究者采用熒光及電阻抗技術分析細胞的生長動力學參數變化,包括生長速率、細胞質量及體積、細胞隔膜環直徑。滲透壓相關蛋白、pH穩態蛋白、核孔復合體等與細胞衰老的關系也被深入研究。
(3)細胞濃度測量。該過程主要利用生化陷阱捕獲細胞,結合電化學信號、熒光強度、比色反應測定目標菌體濃度。
(4)抗生素敏感測試(AST)。通過微閥、擴散-對流混合微流體、級聯液滴結構、圣誕樹結構等多功能模塊集成的微流控芯片,縮短測試時間,提高靈敏度。
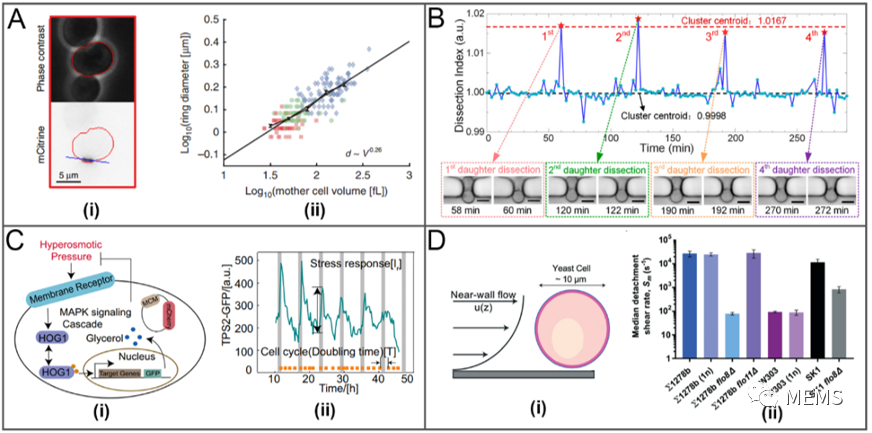
圖4 真菌和細菌細胞的表型分析
最后,作者們分析了目前數據處理、細胞生理活動監測等方面的不足,并提出在未來人工智能(AI)工具,如機器學習和數學建模,將結合微流控系統以更全面的角度分析真菌和細菌的生物物理特性及動態行為變化。
審核編輯:劉清
-
傳感器
+關注
關注
2550文章
51046瀏覽量
753133 -
發生器
+關注
關注
4文章
1368瀏覽量
61680 -
SAW
+關注
關注
11文章
145瀏覽量
27175 -
傅里葉變換
+關注
關注
6文章
441瀏覽量
42592 -
微流控系統
+關注
關注
1文章
73瀏覽量
1867
原文標題:綜述:用于真菌和細菌分析的集成微流控系統的最新進展
文章出處:【微信號:MEMSensor,微信公眾號:MEMS】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
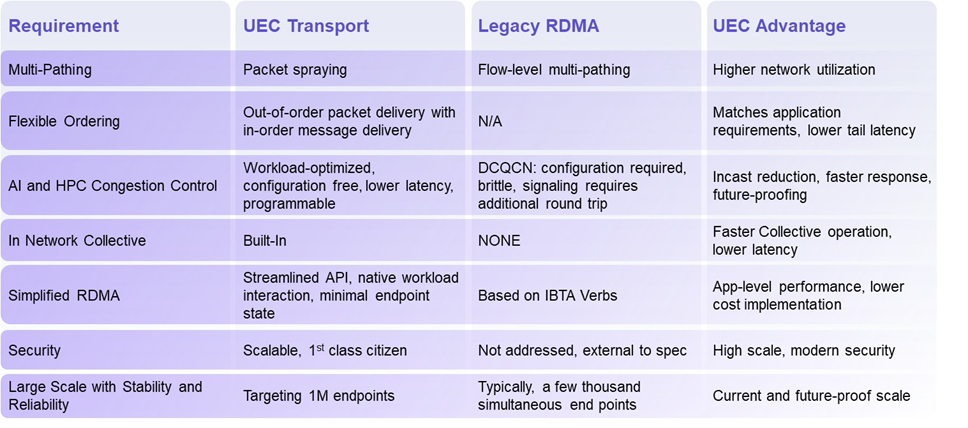
揭秘超以太網聯盟(UEC)1.0 規范最新進展(2024Q4)
Qorvo在射頻和電源管理領域的最新進展
小鵬汽車圖靈芯片及L4自動駕駛新進展
芯片和封裝級互連技術的最新進展
高燃回顧|第三屆OpenHarmony技術大會精彩瞬間
納芯微收購麥歌恩新進展:從79.31%到100%股權收購,整合優勢全面釋放

5G新通話技術取得新進展
最新進展!Intel 18A產品,成功點亮!
廣東的5G-A、信號升格和低空經濟,又有新進展!

百度首席技術官王海峰解讀文心大模型的關鍵技術和最新進展

將薄膜鈮酸鋰光子技術應用于新一代數據中心光收發器中
四個50億+,多個半導體項目最新進展!
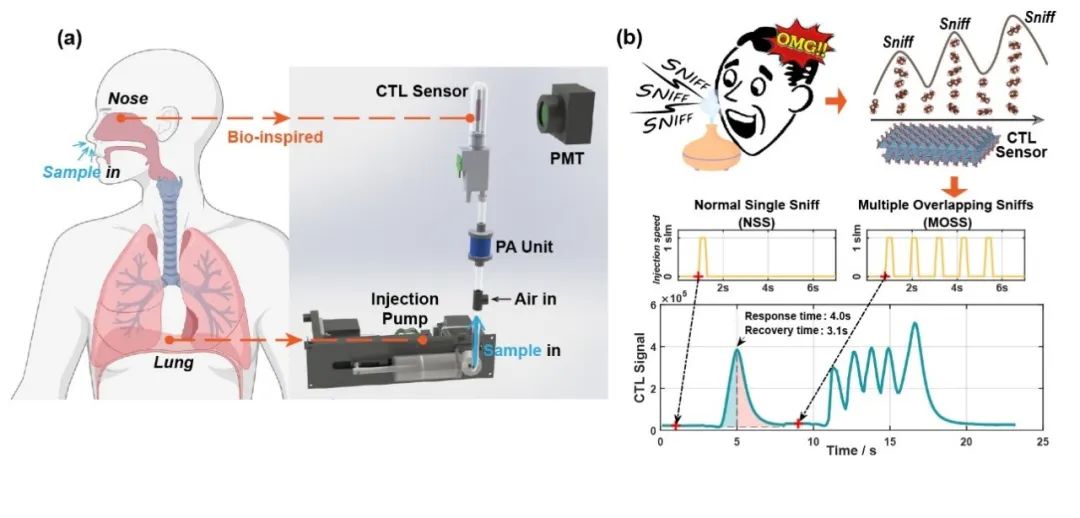
清華大學在電子鼻傳感器仿生嗅聞方向取得新進展
語音識別技術最新進展:視聽融合的多模態交互成為主要演進方向





 用于真菌和細菌分析的集成微流控系統的最新進展
用于真菌和細菌分析的集成微流控系統的最新進展










評論