01 什么是CRISPR?

基因攜帶著生物體的遺傳信息,是儲存著生命的種族、血型、孕育、生長、凋亡等過程的一套精確的密碼,決定了生物體的性狀。
隨著科學研究的深入,某些場景我們需要人為改變這些密碼,調控生物體的各種性狀,諸如性別、毛色、膚色等等(當然性狀也受環境的影響),這種行為被稱為基因編輯。然而基因編輯并非易事,原因之一便是基因眾多,組成簡單生命最少要 265 到 350 個基因。這些基因上沒有標簽,無從知道哪段基因對應了什么性狀。而且基因存在于微小的 DNA 中,尺度在納米級別。微小而繁復,使得基因編輯就像是在一團亂麻中找到想編輯的一段進行微型手術,難度不言而喻。
而在1987年被科學家在大腸桿菌中發現的一段“無法確定功能”的DNA成為了基因編輯技術的一大契機,這段DNA后期被稱為CRISPR。CRISPR是生命進化歷史上,細菌和病毒進行斗爭產生的免疫武器,簡單說就是病毒能把自己的基因整合到細菌,利用細菌的細胞工具為自己的基因復制服務,細菌為了將病毒的外來入侵基因清除,進化出 CRISPR-Cas9 系統,利用這個系統,細菌可以不動聲色地把病毒基因從自己的基因組上敲除,這是細菌特有的免疫系統,是古菌和細菌抵抗病毒等外源遺傳物質入侵的一種獲得性免疫系統。微生物學家掌握了細菌擁有多種切除外來病毒基因的免疫功能,其中比較典型的模式是依靠一個復合物,該復合物能在一段RNA指導下,定向尋找目標DNA序列,然后將該序列進行敲除。許多細菌免疫復合物都相對復雜,其中科學家掌握了對一種蛋白Cas的操作技術,并先后對多種目標細胞DNA進行敲除。
通俗地說,CRISPR 技術是一種基因敲除(基因編輯)的技術。這種技術無視基因帶來的挑戰,它的強大之處在于能夠實現精確的基因編輯,達到指哪打哪的程度,實現更高效率的基因敲除。在過去的十年里,圍繞著 CRISPR 技術的研究數量發生了爆炸式增長。這些研究帶來了諸多富有創新性的應用,比如使用 CRISPR 技術對 DNA 納米結構進行工程化設計或是通過基因編輯來治療遺傳疾病(例如鐮狀細胞病),這些突破性研究極大地革新了傳統基因編輯技術。
02 CELESTA光源用于 CRaft-ID 成像
 混合基因敲除篩選(Pooled genetic knockout screens)在功能基因組學界廣泛用于鑒定與細胞表型相關的基因,而基因敲除方法中最典型的則為CRISPR 方法。但是這類篩選方法大多采用比較粗獷的篩選指標,如生長速率、合成致死和熒光報告等方法。
混合基因敲除篩選(Pooled genetic knockout screens)在功能基因組學界廣泛用于鑒定與細胞表型相關的基因,而基因敲除方法中最典型的則為CRISPR 方法。但是這類篩選方法大多采用比較粗獷的篩選指標,如生長速率、合成致死和熒光報告等方法。
近年來,隨著單細胞測序的普及,將其與混合基因敲除篩選法相結合,實現了全轉錄組范圍內的定量分析,大大提升了篩選的通量。但是,這些方法仍然不能對亞細胞層面的表型進行分析,如在成像層面能夠觀察到的時空分辨率下的一些表型。因此,將匯集的 CRISPR 基因篩選與細胞和亞細胞成像讀數相結合對于改善基于圖像的基因敲除研究中的表型定義至關重要。
2020年5月11日,加州大學圣地亞哥分校的華裔學者Gene W Yeo及其同事在Nature methods雜志上發表題為Pooled CRISPR screens with imaging on microraft arrays reveals stress granule-regulatory factors的研究論文。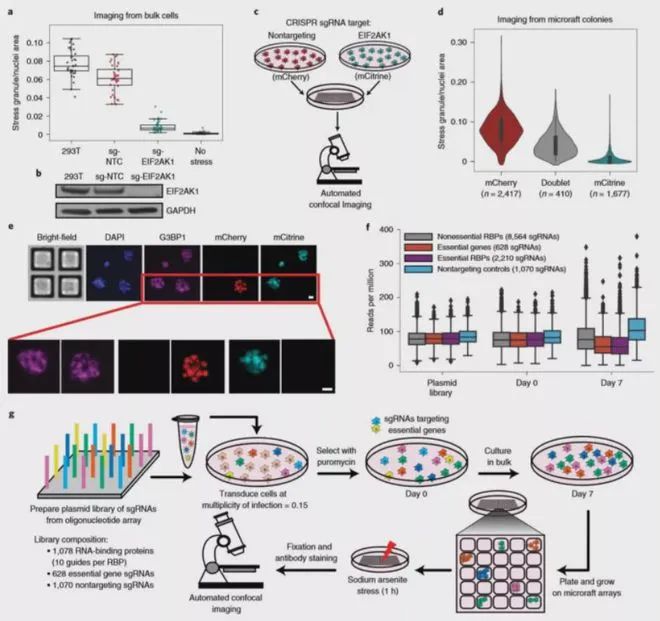
在這篇文章中,作者將 Pooled CRISPR-Cas9 篩選與微筏陣列(又稱基因芯片)技術以及高內涵成像相結合,開發了新技術“CRaft-ID”。作者選用了包含 >1,000 個 RBPs 的 gRNA 文庫(> 12,000 個 sgRNA)對細胞進行了感染,然后在 20 個微筏陣列上進行單細胞培養,篩選得到 119050 個應激刺激后的單細胞集落和 5262 個未進行應激刺激的對照集落。隨后采用自動高分辨率共聚焦成像來識別應激顆粒的調節因子,并開發了機器學習工具來識別 CRISPR 基因敲除后應激顆粒豐度降低的基因克隆。
其中,微筏陣列的共聚焦成像是使用與 CrestOptics X-Light V2 L-FOV 旋轉盤共聚焦耦合的虹科 CELESTA 光源完成的。在這種大通量成像應用中,顯微鏡光源需要具有極佳的光源強度和長時間工作的穩定性,虹科CELESTA 光源滿足所有嚴苛要求。虹科 CELESTA 光源的405 nm,520 nm,546 nm和638 nm線分別用于激發DAPI,mCitrine,mCherry和Alexa Fluor 633的熒光。該篩選鑒定并驗證了六種以前已知的應激顆粒調節劑,以及17種RNA結合蛋白(RBP)。當它們耗盡時,可減少亞砷酸鈉誘導的人體細胞中應激顆粒,這為應激顆粒提供了新的生物學見解。基于虹科 CELESTA 光源構建的 CRaft-ID 篩選平臺拓展了 CRISPR 篩選在高內涵成像中的應用,使得我們能夠對亞細胞層面和細胞形態的表型進行遺傳因子分析,而這些在以前是無法實現的。由于該方法采用的微筏陣列、通用的CRISPR文庫、現成的共聚焦成像技術和基于 PCR 的 DNA 測序,因此具有廣泛的應用前景。
03虹科CELESTA光源介紹



虹科CELESTA
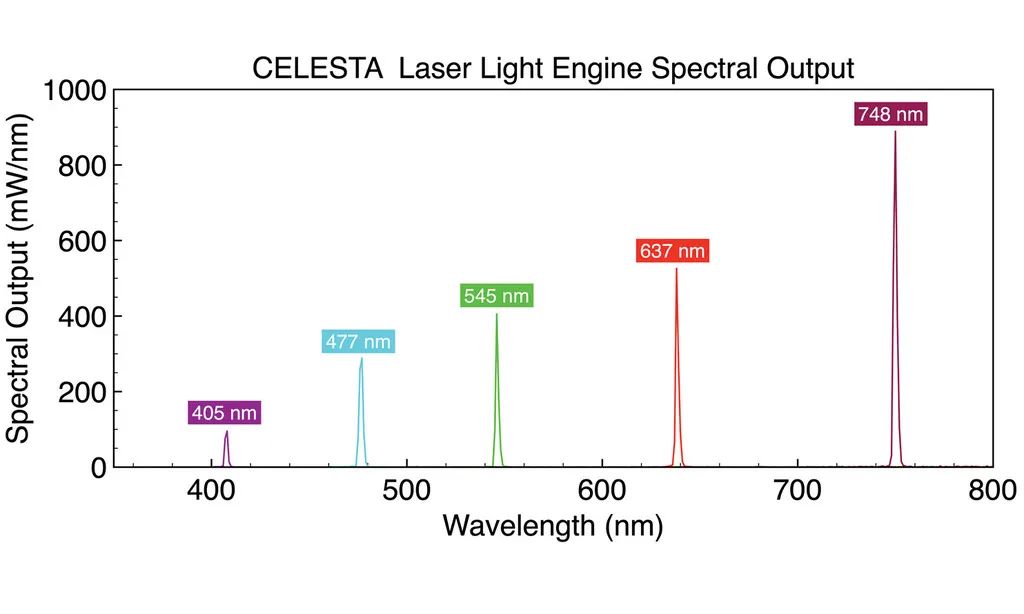
虹科 CELESTA 和 CELESTA quattro 光源包括4-7個可單獨控制的固態激光光源陣列(在400-800nm范圍提供7個可選波長),并且支持快速切換。CELESTA 光引擎在1.5mm直徑光纖的遠端出光,其7個激光器中的每一個都能提供約1W的輸出功率。
同樣,CELESTA quattro 光源以相同的輸出功率規格提供了一個具有性價比的4或5通道選擇。激光輸出與復雜的控制和監測系統相結合,為旋轉盤共聚焦顯微鏡、空間分辨率轉錄組學和其它高級成像應用提供所需的高清晰度性能。
-
光源
+關注
關注
3文章
705瀏覽量
67804
發布評論請先 登錄
相關推薦
分析共聚焦激光顯微鏡成像的常見問題
共聚焦激光顯微鏡在材料科學中的應用
共聚焦激光顯微鏡對比超分辨顯微鏡
共聚焦激光顯微鏡的光學系統解析
共聚焦激光顯微鏡的使用注意事項
共聚焦激光顯微鏡工作原理
共聚焦顯微鏡有什么用?

共聚焦、光學顯微鏡與測量顯微鏡的區分
顯微成像與精密測量:共聚焦、光學顯微鏡與測量顯微鏡的區分
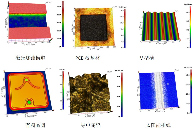
用于材料領域的共聚焦顯微鏡可以看到什么?

共聚焦顯微鏡和激光共聚焦顯微鏡的區別詳解
共聚焦顯微鏡和激光共聚焦顯微鏡的區別詳解

顯微測量|共聚焦顯微鏡大傾角超清納米三維顯微成像
顯微測量|共聚焦顯微鏡大傾角超清納米三維顯微成像





 虹科案例|CELESTA光源用于Craft-ID技術的共聚焦成像
虹科案例|CELESTA光源用于Craft-ID技術的共聚焦成像










評論