研究背景
水系電解液中的質子可以作為水系可充電電池中除主載體陽離子之外的另一種類型的電荷載體用于插入/萃取。盡管關于質子效應有許多不同的說法,但在過去十年中,在沒有直接證據的情況下,已經報道了相互矛盾的實驗結果及其解釋。因此,系統的檢查和分析是闡明在水系可充電電池中質子嵌入狀況的必要條件。近日,韓國首爾國立大學Jang Wook Choi &韓國科學技術院Sung-Yoon Chung團隊利用V2O5陰極和燒杯型電池,在充足的ZnSO4電解液中,證明了在低pH條件下(pH≤3.0),質子先于鋅離子插入陰極。與之形成鮮明對比的是,在硬幣型電池中,當pH變高(pH≥4.0)或電解質體積相當低時,質子對放電電壓和容量的影響不顯著。在鈉離子、鎂離子和鋁離子電解質中也證實了依賴pH的質子插入的類似行為。為了解決關于質子插入的爭議,本研究強調質子的影響在很大程度上取決于水系電池中電解液的pH值和相對體積。
研究亮點
本文利用V2O5正極材料,研究了不同pH電解液中的載流子的差異,并在不同金屬離子電解液體系中得到了驗證。對于水系電池中嵌入載流子的討論具有重要意義。 在充足電解液,低pH條件(pH≤3.0)下,質子插入通常發生在相對較高的電位,此外對于放電容量具有較明顯的影響。而在少量電解液的情況下,沒有發現放電行為的實質性差異,表明質子對此沒有顯著影響。
因此在評價質子在水系電池中的作用時,需要綜合考慮正極材料與電解液的相對質量比例以及pH值。
圖文導讀
圖1.不同pH值電解液放電行為的比較.
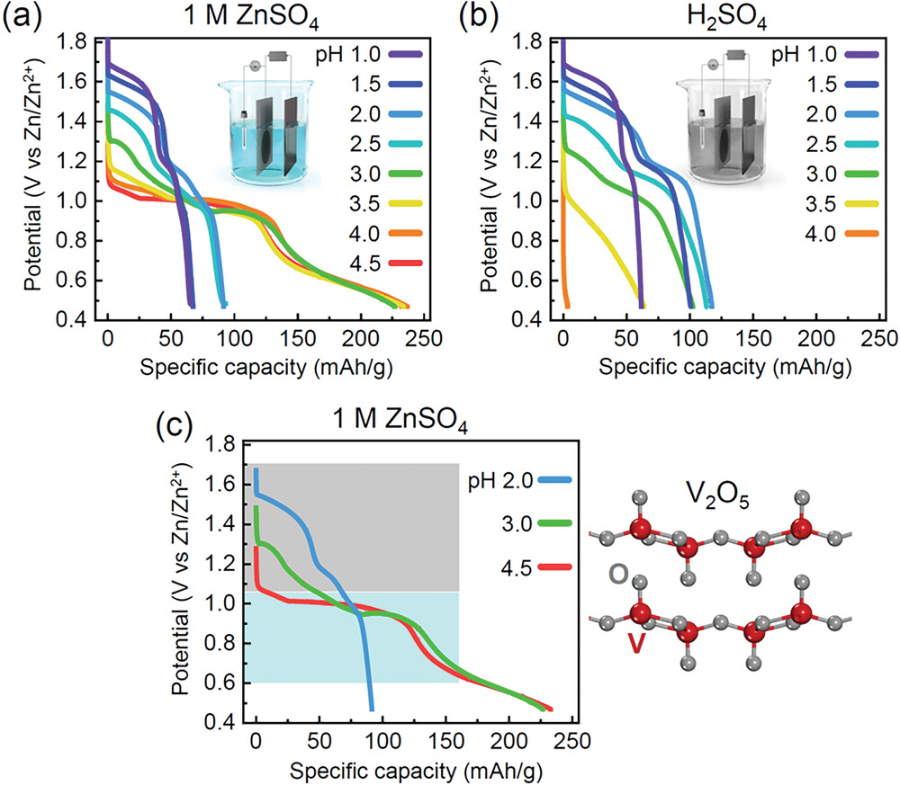
所有恒流放電曲線均在燒杯型電池中得到。a)電池內電解液采用1 M ZnSO4水溶液。為了調整pH值,將H2SO4溶液與每種電解液相應混合。b)僅使用不含鋅鹽的H2SO4溶液作為電解液。c)在ZnSO4電解質中獲得的三條具有代表性的放電曲線。兩個電位范圍分別用灰色和青色陰影表示。
▲通過比較在不同pH環境下的放電曲線,觀察到在pH≤3.0的情況下,放電初期出現的高電位與質子插入有關。這與pH為1.0-3.0的H2SO4溶液中獲得的在1.1-1.7 V之間的放電曲線幾乎相同。而在pH≥3.5時,H2SO4電解液中幾乎沒有明顯的放電容量,證明了低pH下質子的電化學插入。
圖2.不同放電深度下陰極顆粒中鋅的能譜圖.
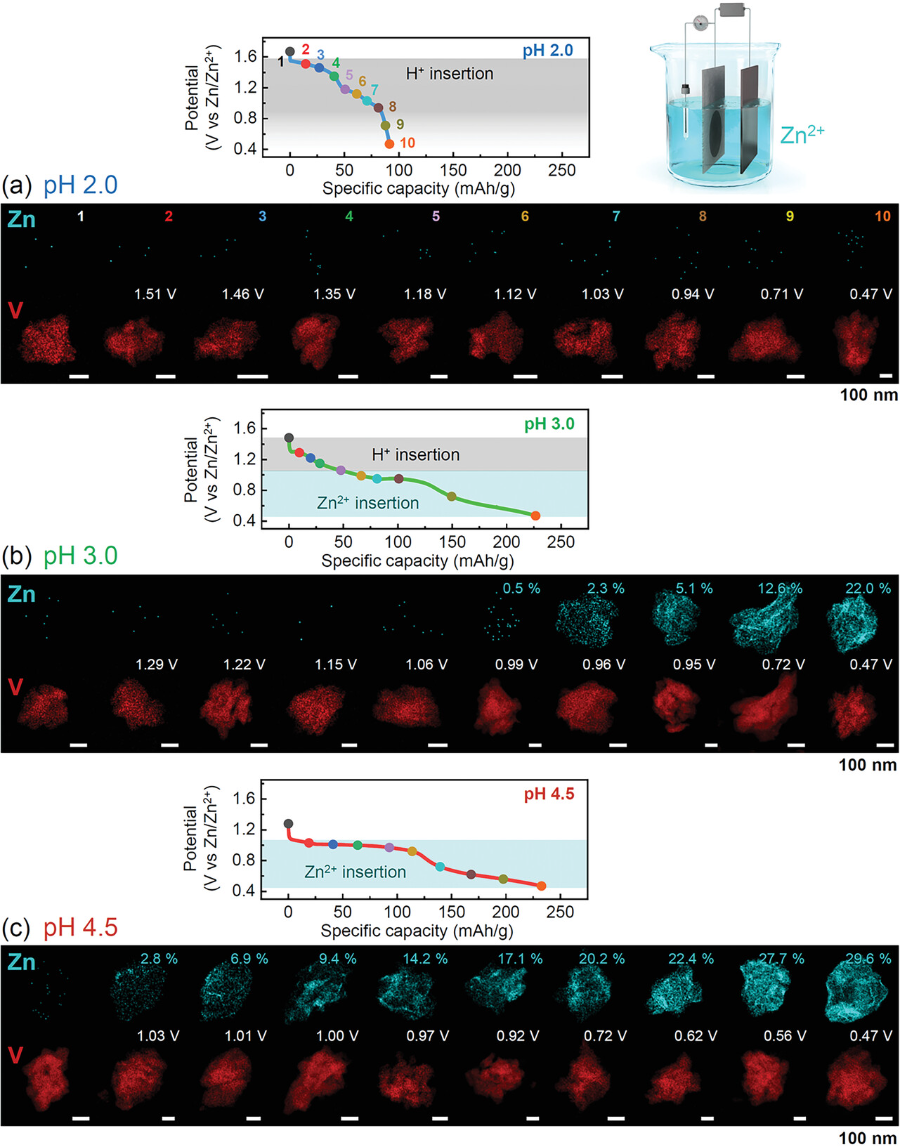
在三種pH條件下,分別得到10張EDS maps:a) pH 2.0;b)3.0;c) 4.5。與pH值為4.5時Zn含量逐漸增加相比,pH值為2.0時沒有Zn插入,pH值為3.0時整個放電過程中從0.99 V開始檢測到顯著的Zn特征。還給出了鋅的定量濃度。
▲利用EDS能譜圖直接可視化了在三種不同pH條件下的V2O5顆粒中插入了多少鋅離子,作為放電深度的函數。在pH 2.0的情況下,幾乎沒有檢測到鋅,有力地支持了質子是電化學插入的主要電荷載體而非鋅離子。而在高pH條件下(圖2c),沒有觀察到1.2 V以上的高電位放電平臺,并且從放電開始Zn濃度一直在增加。因此,在該pH條件下,質子對總容量幾乎沒有貢獻。
圖3.不同放電深度下V2O5的三組XANES光譜.
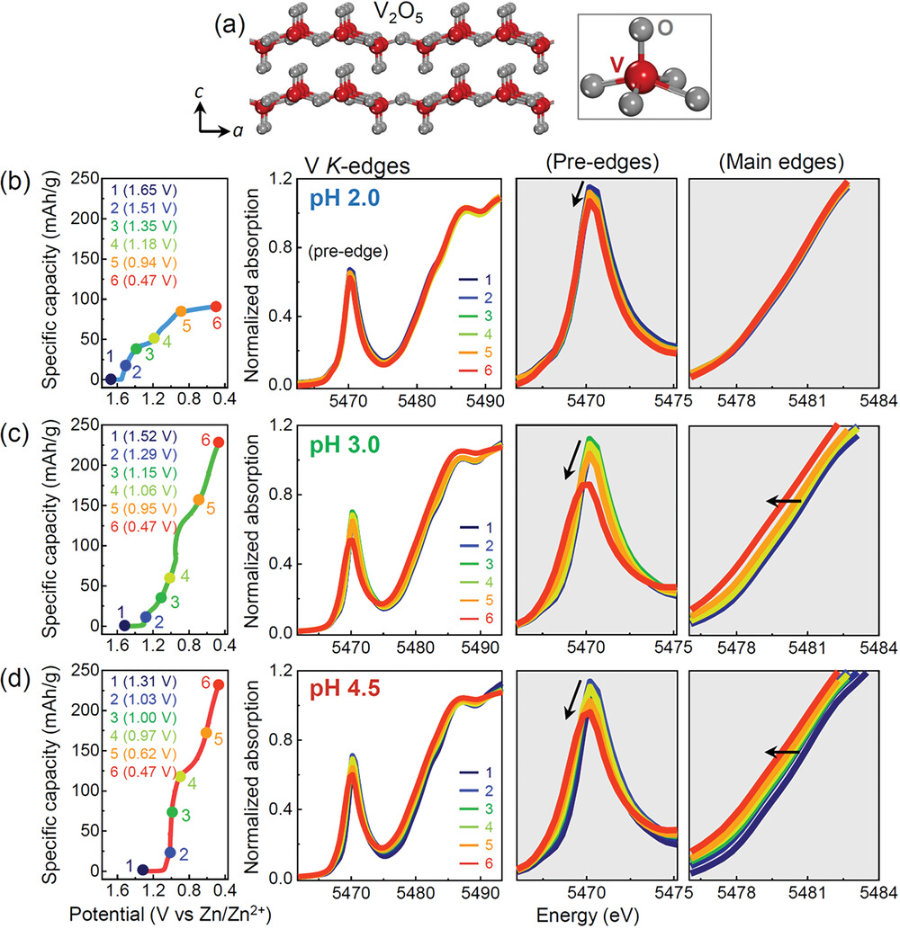
a)給出了V2O5的晶體結構。五個非中心對稱氧配體在放大圖中呈現。在3種pH條件下分別得到6個光譜:pH為b) 2.0;c) 3.0;d) 4.5。
▲對不同pH環境下六種不同放電深度的樣品進行XANES分析。由于V與五個非中心對稱的氧配體配位(見圖3a的插圖),這種強烈扭曲的氧方錐體環境偏離了對稱的氧八面體,從而導致了V 3d態與O 2p態的大量混合。因此,額外的偶極禁止1s→3d躍遷導致V2O5中存在吸收預邊。除了主邊緣的低能位移外,預邊緣強度的降低是V2O5氧化態降低的另一個標志。在pH為3.0和4.5的情況下,隨著放電反應的進行,主吸收邊向較低能量值移動,預邊強度減小(圖3c,d),這直接表明V被還原了。在pH為2.0的情況下,主吸收邊的移動沒有明顯的區別,但預邊緣的強度明顯降低(圖3b)。因此,結合圖2a中沒有Zn的EDS圖和圖3b中的XANES光譜,提供了在低pH條件下放電反應中質子插入的一致證據。
圖4.V2O5粒子的三組EXAFS光譜和HAADF STEM圖像.
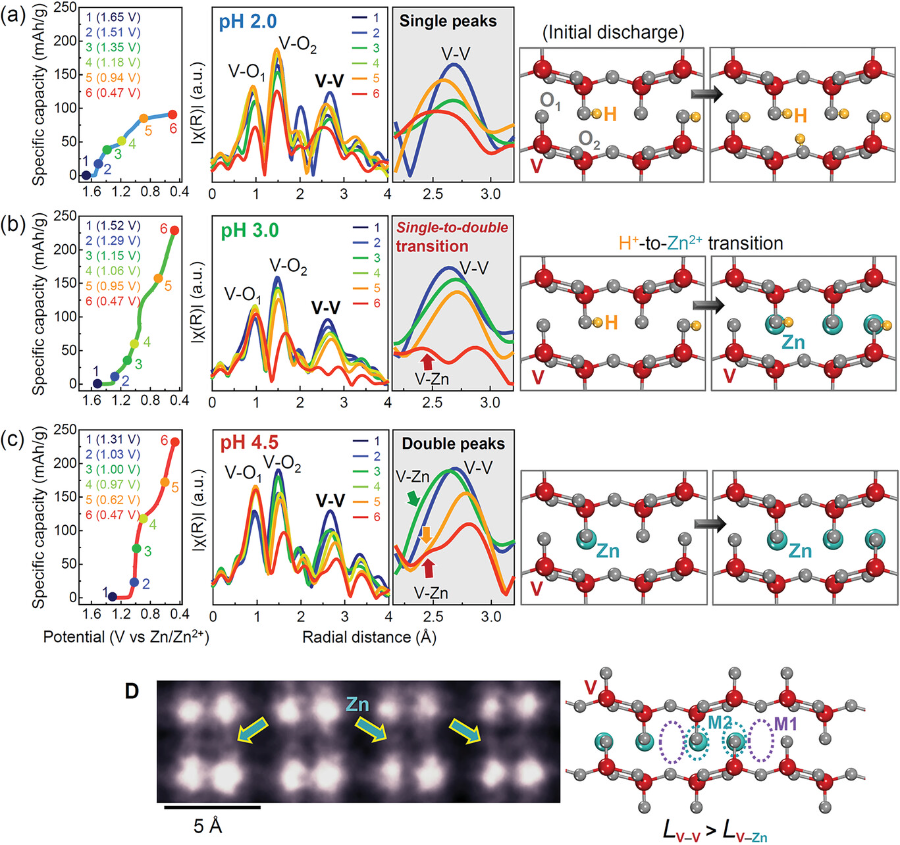
在以下三種pH條件下,電解質在不同放電水平下的傅立葉變換光譜分別為:a) pH 2.0;b) 3.0;c) 4.5。在每種情況下,表示V-V的峰在中間一列中被放大,并附有載流子離子插入的示意圖。d) HAADF-STEM圖像顯示Zn嵌入到V2O5框架中。如圖中箭頭所示,直接說明Zn占據了M2的間隙位,而不是M1的間隙位。LV-V和LV-Zn分別表示V-V和V-Zn的鍵距。
▲傅里葉變換光譜中的前兩個主要峰來自兩個不同的V-O鍵,第三個峰對應于V-V鍵。從圖4a中間列放大圖中可以看出,在pH為2的情況下,整個放電過程中V-V峰之間的單峰形狀沒有變化。而隨著放電反應的進行,在pH為3.5的條件下,由最初的單峰型V-V峰轉變為雙峰型。圖4b中V-V峰的紅色箭頭說明了另一個峰的出現,這個峰是由插入到間隙位置的Zn離子作為V-Zn形成的。圖4b中的一系列EXAFS光譜揭示了在放電初始階段首先插入質子,然后Zn離子參與了低于1 V (vs Zn/Zn2+)的放電反應。
圖5.不同放電深度下的XPS結果.
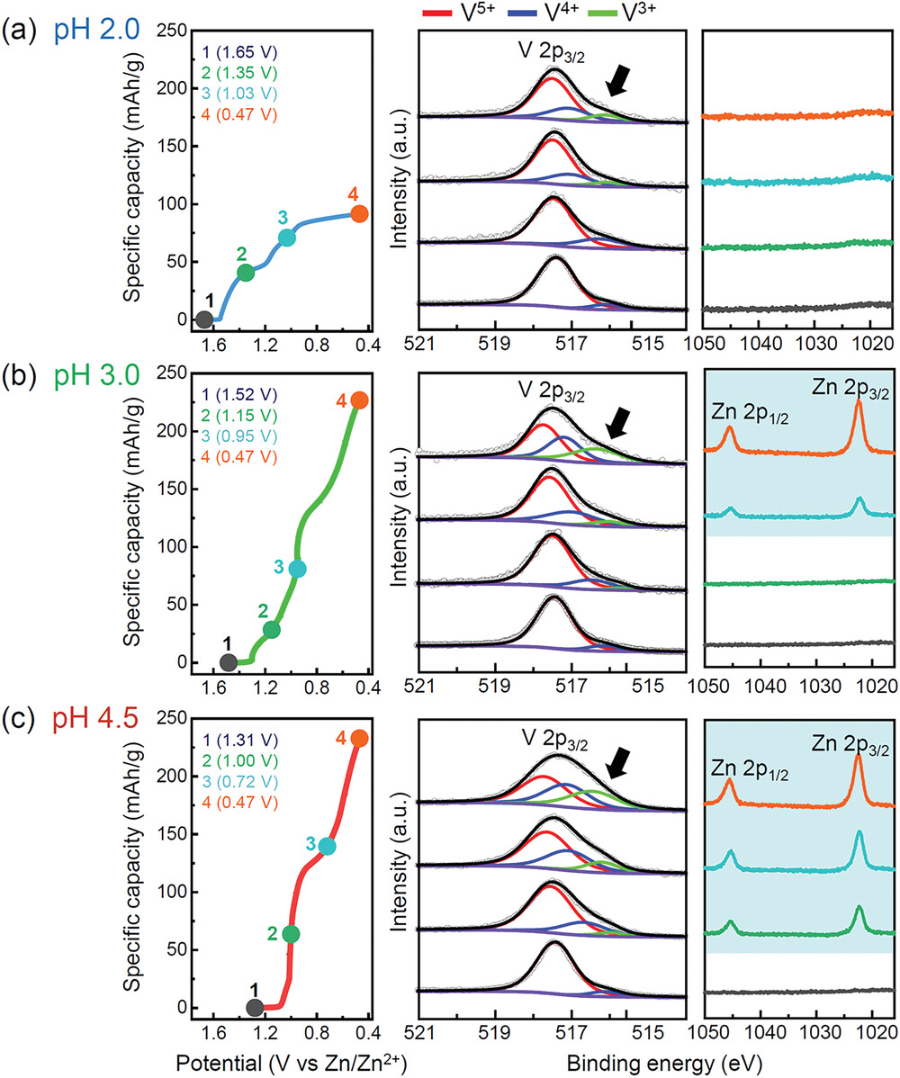
對在3種pH電解液中放電的陰極顆粒進行了非原位XPS分析:(a) pH 2.0;b)3.0;c) 4.5。在所有三個樣品中,V4+/3+肩峰(黑色箭頭)的一致出現表明放電反應是通過H+或Zn2+插入發生的。在pH為3.0和4.5的情況下,XPS對Zn的檢測結果與圖2所示的EDS圖吻合較好。
▲圖5a中未檢測到Zn的存在,表明在低pH條件下無鋅離子插入。而在V 2p3/2峰附近出現一個較低結合能的寬峰,表明V5+由于質子插入還原為V4+和V3+。在圖5b中,當pH為3.0時,在0.95 V之前沒有檢測到Zn,盡管在整個放電反應過程中,V4+/V3+峰的強度逐漸增加。因此,這些XPS結果與之前的結論一致,一致支持插入載流子隨著pH增加從H+向Zn2+的轉變。
圖6. 鈉、鎂、鋁在不同放電深度下的EDS maps.
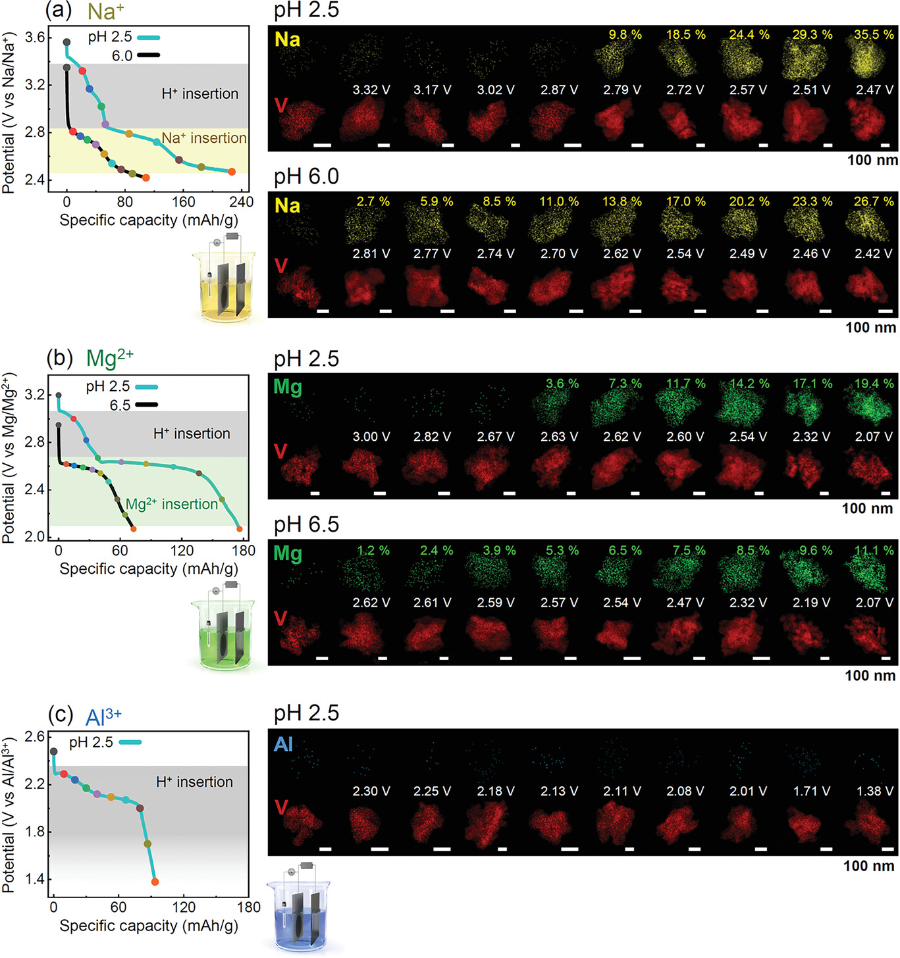
在燒杯電池放電過程中,使用了含有a) Na2SO4,b) MgSO4和c) Al2(SO4)3的電解質來檢測其它化學物質作為插入載體。在低pH條件下(pH 2.5),質子在高電位范圍內的插入似乎在所有三種情況下都占主導地位。
▲同時,作者發現這種依賴于pH的插入-載流子轉變不僅局限于鋅離子化學,而且在其它體系中也可以觀察到。在低pH環境下,質子在更高的放電電壓內嵌入,先于三種陽離子。而在高pH條件下(6.0 ~ 6.5)放電時,每種陽離子都是主要的插入載流子。其中,使用Al2(SO4)3鹽無法獲得高pH電解液(pH>2.5)。有趣的是,在硫Al2(SO4)3電解液中,整個放電過程中都沒有檢測到Al,這表明與Al/Al3+相比,Al插入的放電電位遠低于1.4 V。
圖7.硬幣型電池試驗中陰極顆粒中Zn的放電曲線和EDS maps.
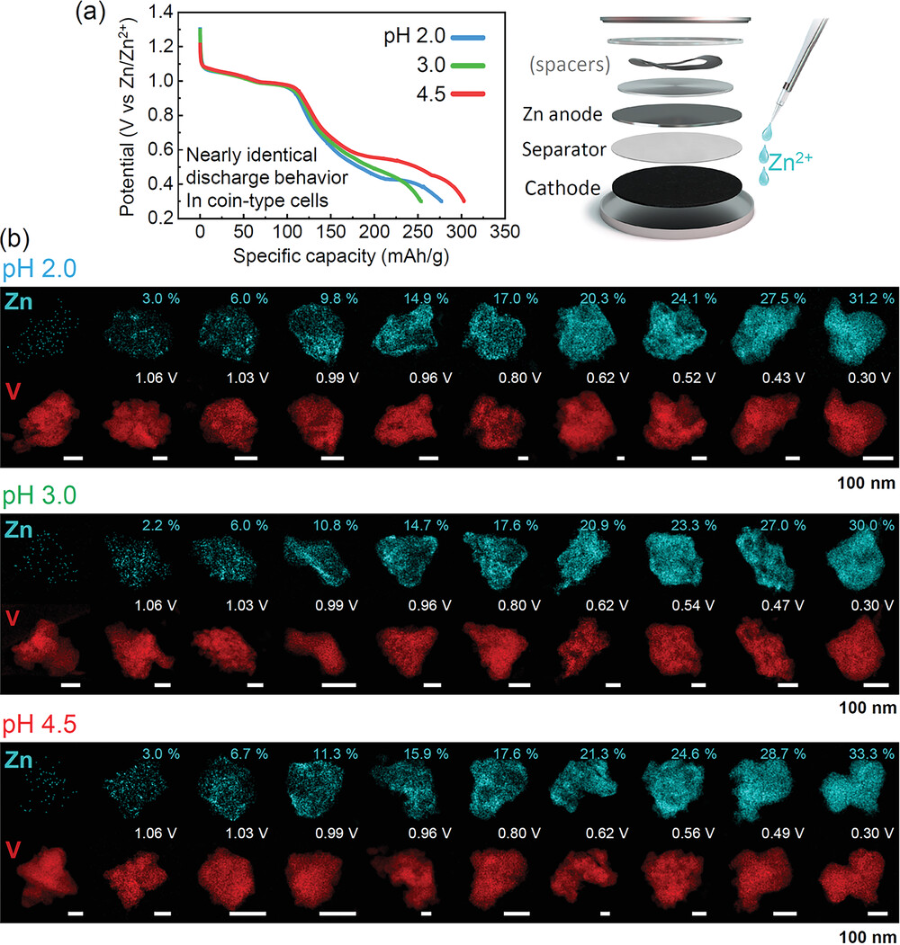
a)無論硬幣電池中電解質的pH值如何,都可以確定幾乎相同的放電行為,其中采用了非常少量的電解質。b)三個樣品從放電反應開始就檢測到Zn。各V2O5顆粒中鋅的定量濃度也在圖中給出。
▲盡管電解質是不可缺少的組成部分,但通常需要最少量的電化學非活性電解質來最大化電池系統的總體體積能量密度。于是使用極少量的電解液(70μL)和鋅金屬陽極組裝成硬幣型電池進行同樣的分析。圖7顯示不同pH條件下表現出幾乎相同的放電行為(圖7a),和從放電開始陰極顆粒中的Zn濃度就開始逐漸增加(圖7b)。證明了當采用少量電解質時,放電過程中沒有明顯的質子插入。
研究總結
本研究提供了一組一致的實驗分析和測量,證明了電解液中質子對水系條件下氧化物陰極放電電壓和容量的影響。雖然本文在這項工作中處理的是一種單一的氧化物陰極材料,但通過使用含有大量電解質的燒杯電池,證明了在低pH條件下(pH≤3.0),質子插入可以先于Zn2+和其他陽離子(包括Na+,Mg2+和Al3+)的插入。相比之下,在使用少量電解質的硬幣電池測試中,在三種不同的pH條件下,沒有發現放電行為的實質性差異,這表明質子對此沒有顯著影響。因為質子的總數也取決于電解質的體積,所以在評價質子在水系電池中的作用時,正極材料的質量與電解液質量之間的相對比例以及pH值似乎是另一個需要考慮的重要參數。
審核編輯:劉清
-
電解質
+關注
關注
6文章
815瀏覽量
20089 -
電解液
+關注
關注
10文章
849瀏覽量
23155 -
XPS
+關注
關注
0文章
97瀏覽量
12009 -
EDS
+關注
關注
0文章
96瀏覽量
11538
原文標題:韓國首爾國立大學&韓國科學技術院AFM:金屬離子與質子:跟蹤插入到水系電池陰極氧化物的電荷載流子
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
金屬氧化物太陽能電池研究取得突破
氧化物半導體甲烷敏感元件詳解
載流子——電流的搬運工
金屬氧化物氣敏傳感器
鋰離子電池鋰錳氧化物正極的研究進展
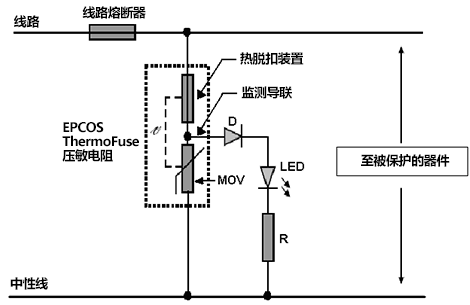
(MOV)層疊金屬氧化物壓敏電阻
固體氧化物電池的原理及系統結構
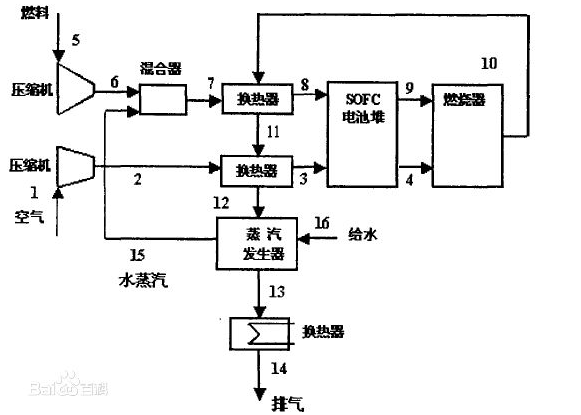
固體氧化物燃料電池工作原理




 金屬離子與質子:跟蹤插入到水系電池陰極氧化物的電荷載流子
金屬離子與質子:跟蹤插入到水系電池陰極氧化物的電荷載流子











評論