【工作介紹】
初始庫侖效率(ICE)高于 90% 對工業鋰離子電池(LIB)至關重要,但許多電極材料都不符合標準。由于(i) Li^+^ 生成的固態反應不完全和(ii) Li^+^ 擴散遲緩,鋰捕集破壞了高容量電極(如轉換型電極)的 ICE。目前緩解鋰捕集的方法強調(ii),即通過納米化(小于 50 納米)將 Li^+^ 擴散距離最小化,但隨后會形成嚴重的固態電解質相(SEI)和較低的體積能量密度。
近日,新加坡南洋理工大學材料科學與工程學院陳曉東教授(新加坡國家科學院院士)團隊通過提高固態再轉化反應性來減輕鋰捕獲以獲得高初始庫侖效率。
作者將重點放在(i)方面,證明可以通過提高固態反應活性來減輕鋰捕獲。作為概念驗證,三元 LiFeO2陽極(其放電產物含有高活性空位豐富的鐵納米顆粒)可緩解鋰捕集,并使平均 ICE 顯著提高至 92.77%,遠高于二元 Fe2O3陽極(75.19%)。同步加速器技術和理論模擬顯示,富含鐵空位的局部化學環境可有效促進鐵和LI2O之間生成 Li^+^ 的固態再轉化反應。組裝好的小袋電池進一步證明了 ICE 的優越性。這項工作提出了一種調節固有固態化學的新模式,以改善電化學性能,促進各種先進電極材料的工業應用。
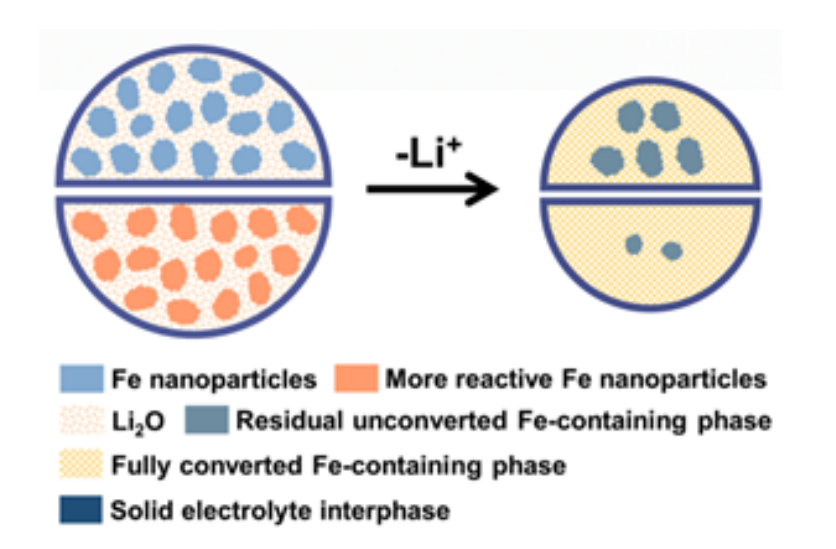
【主要內容】
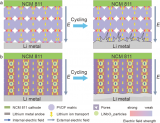
高能量密度鋰離子電池(LIB)是便攜式電子產品、電動汽車、可再生能源利用和負碳社會的理想之選。能量密度由容量、電壓和初始庫侖效率(ICE)決定。雖然高容量和高電壓電極已得到廣泛研究,但 ICE 卻經常被忽視。工業用鋰離子電池要求 ICE 高于 90%(圖 1a),但大量電極材料仍無法達到這一標準。在緩解 SEI 形成造成的不可逆Li+損失方面已經取得了長足的進步,如表面改性、電解質優化和預鋰化等,但作為具有復雜固態反應的高容量電極的主要機理--鋰捕集卻很少被探究,仍然具有挑戰性。
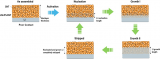
鋰捕集可用下式表示(例如,轉換型Fe2O3陽極):
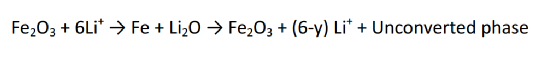
通常情況下,Fe2O3在放電過程(鋰化)后可完全還原為 Fe/ 復合材料,但Li+在隨后的充電過程(脫鋰化)后無法完全釋放,仍會殘留含有低平衡 Fe 的未轉化相(如殘留的未反應 Fe 納米顆粒)(圖 1b)、例如,充電態的 FeF3微絲在第一次循環后的未反應中間相要比充電態的 FeF3納米線多得多。NiO 納米顆粒比(亞)微粒具有更高的可逆容量和更低的電壓滯后。雖然納米顆粒(小于 50 納米)和多孔(分層)結構等納米結構可在充電過程中促進Li+擴散,但這些結構會形成嚴重的 SEI,且體積能量密度較低。
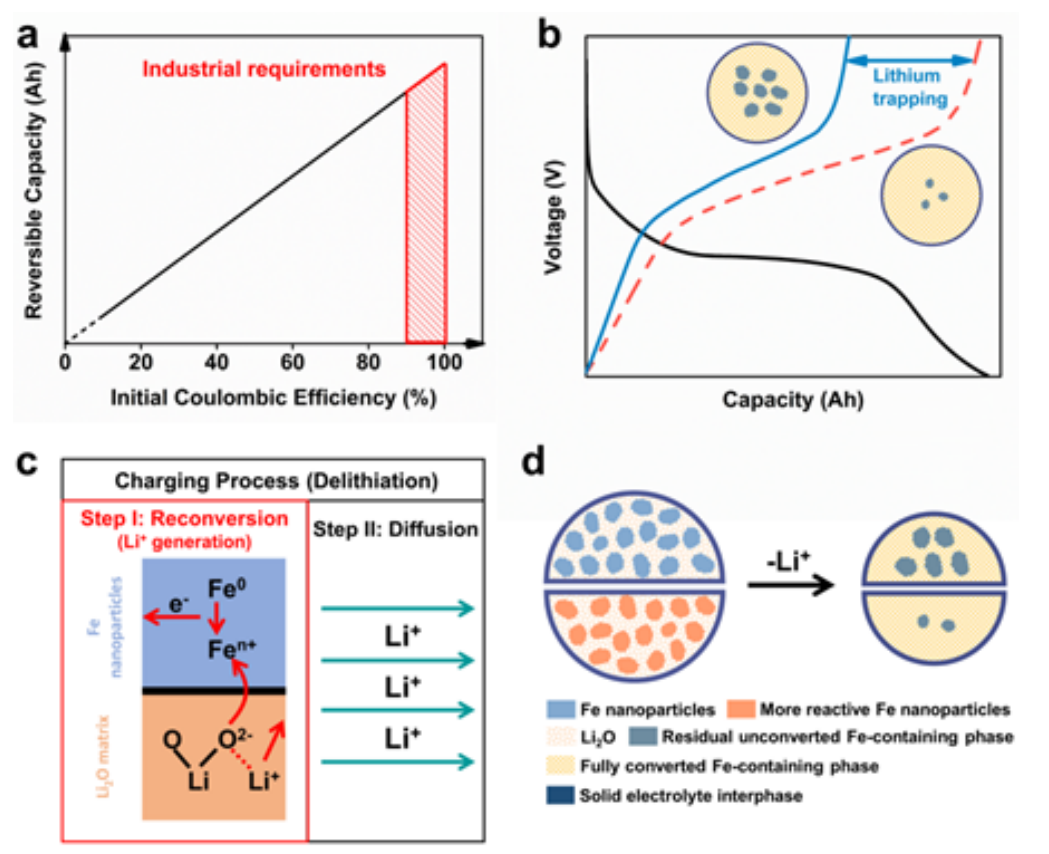
圖 1.a) 商業化電極材料對 ICE 的工業要求(大于 90%)。在充電過程中,Li+無法完全釋放,仍存在未轉化的含鐵相。它包含一個再轉化反應(步驟 I:金屬納米顆粒與反應生成Li+)和隨后的Li+擴散(步驟 II)。
【要點】
為了解決上述問題,本工作以轉換型氧化鐵基陽極為模型系統,重新研究了充電機制(圖 1c)。在充電過程中,Li+首先從金屬 Fe 納米顆粒和LI2O基質之間的固態再轉化反應中產生(步驟 I),然后從電極內部擴散到電解質中(步驟 II)。
與步驟 II 中遲緩的Li+擴散相比,步驟 I 中不完全的再轉化反應和殘留的未轉化相是鋰捕獲的更內在原因。受此啟發,我們打破了操縱外在物理性質(如納米縮放)的做法,更加關注內在的固態再轉化反應。鐵納米顆粒與LI2O基質之間的再轉化反應的發生和進展高度依賴于金屬納米顆粒(< 10 nm)。因此,反應性更強的鐵納米顆粒(如富缺陷鐵納米顆粒)將促進鐵的消耗和?Li+?的生成(圖 1d)。可以使用三元 LiFeO2?和二元?Fe2O3?作為模型體系來研究這一概念。鐵納米粒子的局部結構與鐵氧化物的原始晶格結構有關。
與二元Fe2O3只有邊緣共享的 FeO6八面體不同,陽離子異構的三元 LiFeO2還含有 LiO6八面體,這阻礙了鐵離子的遷移并導致更多的鐵空位形成。因此,排出的 LiFeO2中富含高活性空位的鐵納米粒子將促進再轉化反應并減輕鋰捕獲。
值得注意的是,LiFeO2和Fe2O3中的鐵價都是 +3,這表明在 LiFeO2陽極不存在預鋰化。由于捕獲的鋰來自反電極,因此 LiFeO2中的晶格鋰也不能作為補償不可逆容量損失的鋰源。 本工作證明了鋰捕集可以通過提高固態再轉化反應活性得到有效緩解,從而增強 ICE。同步輻射 X 射線吸收光譜(XAS)和對分布函數(PDF)顯示,與放電的Fe2O3相比,放電的 LiFeO2中含有鐵納米顆粒,其中鐵空位更多。
同步輻射 XAS 進一步揭示了鋰捕獲來自殘留的未轉化金屬 Fe,而富含空位的 Fe 納米粒子可以減輕這種負面影響。密度泛函理論(DFT)計算驗證了富含鐵空位的局部化學環境更有利于鐵納米顆粒與基體之間的固態再轉化反應,從而促進鐵的消耗和Li+的生成,進而緩解鋰捕獲。
得益于此,三元 LiFeO2粒子(0.5-1 μm)的平均 ICE 高達 92.77%,遠高于二元Fe2O3粒子(0.5-1 μm,75.19%)。通過使用與商用 LiNi1/3Mn1/3Co1/3O2(NMC111) 陰極耦合的軟包電池,進一步證明了其卓越的 ICE。這種緩解鋰捕集的獨特機制和策略賦予了大尺寸材料在納米材料中一些特殊的電化學特性,并促進了高能量密度電極的商業化。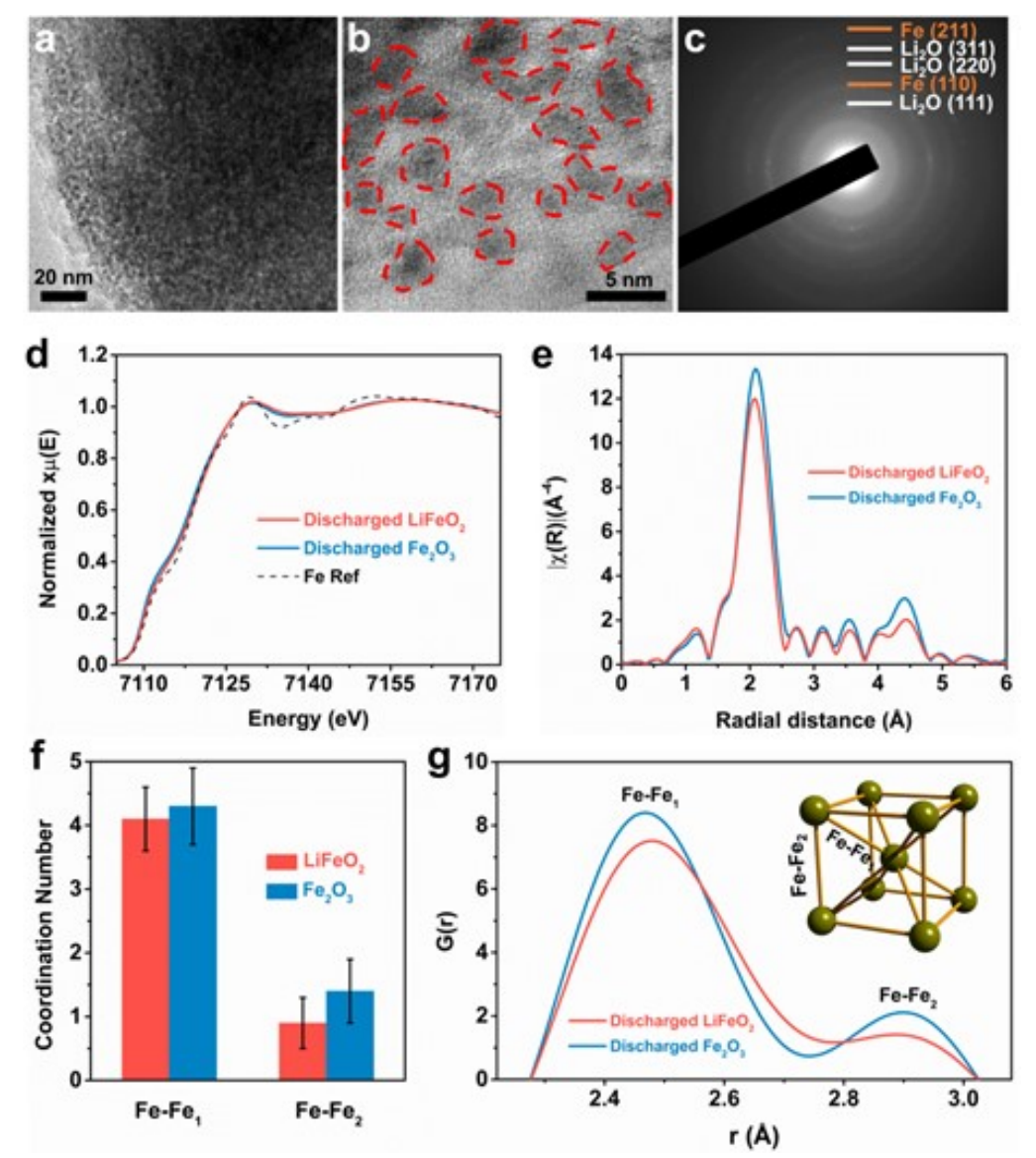
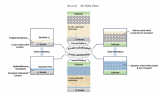
圖 2.a, b) 放電 LiFeO2的典型低倍和高倍 HRTEM 圖像。c) 放電 LiFeO2的相應 SAED 圖樣。d) 分別為放電 LiFeO2、放電Fe2O3和 Fe Ref 的歸一化 Fe Kedge XANES 光譜。e) 放電 LiFeO2和放電Fe2O3的 Fe K-edge EXAFS |χ(R)| 光譜。f) Artemis 擬合收集的放電 LiFeO2和Fe2O3中金屬 Fe 的配位數。g) 放電 LiFeO2和Fe2O3陽極中 Fe 納米粒子的 PDF。g) 中的插圖是 bcc Fe 的晶格結構。Fe-Fe1 和 Fe-Fe2 路徑分別是 bcc Fe 的第一和第二近鄰。
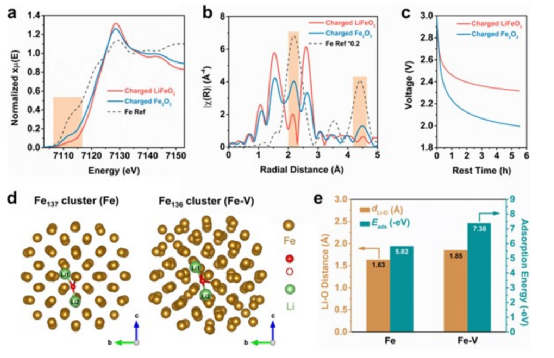
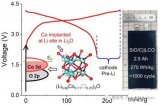
圖 3.a) 充電態 LiFeO2、充電態Fe2O3和 Fe Ref 的歸一化 Fe K-edge XANES 圖譜。b) 充電態的 LiFeO2、充電態的Fe2O3和 Fe Ref 的相應 Fe K 邊 EXAFS |χ(R)| 光譜。c) LiFeO2和Fe2O3陽極在第一個周期后靜置 5.5 小時的電壓曲線。d) 通過 DFT 計算得到的 Fe137 簇(Fe)和 Fe136 簇的 Fe 空位(Fe-V)模型。e) Fe 和 Fe-V 上吸收的的 Li-O 距離和吸附能。Fe 空位可以促進 Fe 納米粒子與基體之間的固態再轉化反應。
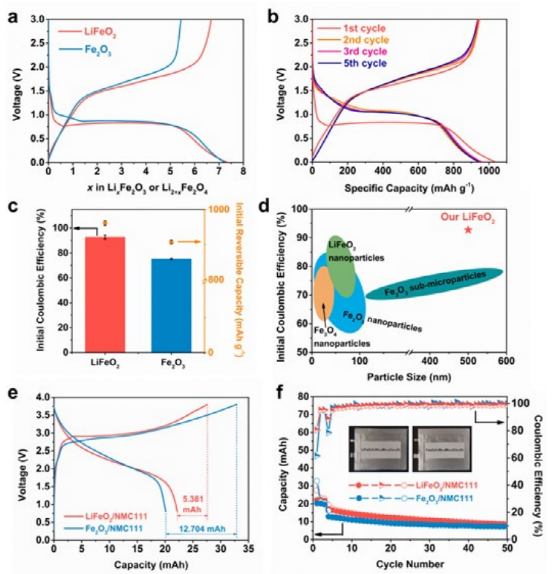
圖 4.a) LiFeO2和Fe2O3的初始放電/充電曲線。測試電流密度為 0.04 A g -1 。b) LiFeO2第 1、2、3 和 5 個周期的放電/充電曲線。c) LiFeO2和Fe2O3的 ICE 和充電比容量統計研究。e) 0.06 mA cm-2下的初始電恒流/放電電壓曲線;以及 f) 0.3 mA cm-2下基于 LiFeO2和Fe2O3的軟包電池的循環穩定性。
【結論】
在這項研究中,我們發現可以通過提高固有的固態再轉化反應活性來減輕鋰捕獲,并最終提高 ICE。作為概念驗證,三元 LiFeO2(0.5-1 μm)的放電產物含有高活性富空位鐵納米顆粒,其平均 ICE 可達到約 92.77%,優于二元Fe2O3(0.5-1 μm,約 75.19%)。同步輻射 XAS 和 PDF 證明,富含空位的鐵簇是在 LiFeO2的鋰化過程中產生的,這有利于減少鋰捕獲。DFT 模擬進一步驗證了 Fe 和LI2O之間的固態再轉化反應性得到了有效促進,有利于 Fe 的消耗和Li+的生成。通過結合 LiFeO2陽極,軟包電池的整體性能得到了有效改善,顯示出巨大的實際應用潛力。這種不同尋常的機制和以固有固態反應機制為重點的策略,有利于開發綜合性能優異的先進電極材料,并提供完整的工業產品。
審核編輯:劉清
-
鋰離子電池
+關注
關注
85文章
3238瀏覽量
77686 -
加速器
+關注
關注
2文章
796瀏覽量
37840 -
DFT算法
+關注
關注
0文章
27瀏覽量
7535 -
固態電解質
+關注
關注
0文章
83瀏覽量
5419 -
軟包電池
+關注
關注
1文章
175瀏覽量
7974
原文標題:南洋理工大學陳曉東院士AM:提高固態再轉化反應活性,緩解鋰捕獲,實現高初始庫侖效率
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
相關推薦
原位焊接離子導電斷點以實現高度可逆的全固態鋰硫電池

通過電荷分離型共價有機框架實現對鋰金屬電池固態電解質界面的精準調控
欣界能源發布“獵鷹”鋰金屬固態電池
環境條件下微通道反應器中丙烷的高效轉化
微反應器和微混合器的區別
純鋰新能源全固態電池成功量產
將廢正極材料升級為高穩定性鋰硫電池的雙功能催化劑!





 提高固態再轉化反應活性,緩解鋰捕獲實現高初始庫侖效率
提高固態再轉化反應活性,緩解鋰捕獲實現高初始庫侖效率













評論