最新的AlphaFold模型不再局限于蛋白質(zhì)折疊,還能夠在配體、蛋白質(zhì)、核酸以及翻譯后修飾等方面生成高度精確的結(jié)構(gòu)預測。DeepMind 其衍生公司 已將該系統(tǒng)用于藥物設(shè)計。
大約五年前,谷歌最多產(chǎn)的以AI為中心的研究實驗室之一,DeepMind,推出了 AlphaFold。這是一種可以準確預測人體內(nèi)許多蛋白質(zhì)結(jié)構(gòu)的人工智能系統(tǒng)。
從那時起,DeepMind 對系統(tǒng)進行了改進,于 2020 年發(fā)布了更新且功能更強大的 AlphaFold 版本--AlphaFold 2。
實驗室的工作仍在繼續(xù)。
10月31日,DeepMind表示,最新版本 AlphaFold 已經(jīng)出爐,不少人將其取名為“ AlphaFold 3”。
據(jù)悉,最新的 AlphaFold 系統(tǒng)由DeepMind及其衍生公司 Isomorphic Labs (專注于利用 AI 做藥物發(fā)現(xiàn))共同開發(fā),不再局限于蛋白質(zhì)折疊,還能夠在配體、蛋白質(zhì)、核酸以及翻譯后修飾等方面生成高度精確的結(jié)構(gòu)預測。且 Isomorphic Labs 公司已經(jīng)將該系統(tǒng)用于藥物發(fā)現(xiàn)工作。
不過最新版本的“ AlphaFold 3 ”還處于預覽階段,后續(xù)開發(fā)工作還在進行。
AlphaFold新版本有哪些升級?
第一大升級:預測蛋白質(zhì)數(shù)據(jù)庫(PDB)中大多數(shù)分子類型的結(jié)構(gòu),達原子精度。
根據(jù)DeepMind的說法,AlphaFold可以預測蛋白質(zhì)數(shù)據(jù)庫(一個廣泛使用的科學數(shù)據(jù)庫)中幾乎所有分子的結(jié)構(gòu)。DeepMind聲稱,該模型通常以“原子精度”生成這些預測。
AlphaFold 新版本不僅可以估計蛋白質(zhì)的形狀,還可以估計其他生物分子的形狀。包括:小分子(配體)、蛋白質(zhì)、核酸(DNA和RNA)、具有翻譯后修飾(PTM)的分子。
第二大升級:預測相關(guān)配體的結(jié)構(gòu)。
所謂配體,是指其他不同分子與蛋白質(zhì)結(jié)合,并導致蛋白質(zhì)功能方式發(fā)生變化。配體在細胞信號傳導中起著重要作用,細胞信號傳導是細胞相互影響行為的關(guān)鍵生物過程。
一種情況是,當配體附著或結(jié)合到蛋白質(zhì)上時,組合結(jié)構(gòu)稱為“蛋白質(zhì)-配體復合物”。研究人員歷來使用一種稱為“對接”的方法評估這種復合物的形狀。但這一方法的局限性是,只有當有大量關(guān)于蛋白質(zhì)-配體復合物的蛋白質(zhì)成分的數(shù)據(jù)可用時,才能使用這種方法。
根據(jù) DeepMind 的說法,新版本的 AlphaFold 新版本可以比“對接”方法更準確地預測蛋白質(zhì)-配體復合物的形狀。與這些方法相比,AlphaFold 新版本需要的數(shù)據(jù)要少得多。
DeepMind最新模型為蛋白質(zhì)-配體結(jié)構(gòu)預測設(shè)定了新的標準,在預測蛋白質(zhì)-配體相互作用方面,新AlphaFold的性能比傳統(tǒng)方法高出約20%,并且還可以預測尚未進行結(jié)構(gòu)表征的全新蛋白質(zhì)。
因此,AlphaFold 新版本可能會使科學家更容易研究新發(fā)現(xiàn)的蛋白質(zhì)-配體復合物,而這些復合物的信息很少,而且可以幫助科學家識別和設(shè)計潛在的藥物新分子。
Isomorphic Labs 最新公布了3個案例實驗:抗癌分子的結(jié)合(PORCN)、關(guān)鍵癌癥靶標的共價配體結(jié)合(KRAS),脂質(zhì)激酶變構(gòu)抑制劑(PI5P4Kγ)的結(jié)構(gòu)預測。結(jié)果顯示,該模型預測的結(jié)構(gòu)與案例實驗中測定的結(jié)構(gòu)非常接近。
這一舉動引起相關(guān)學者和藥企的關(guān)注。有人在國內(nèi)外社交平臺表示:“設(shè)計新的分子比開發(fā)工具更重要,開發(fā)類似工具的人可能要改行,畢竟設(shè)計新的高價值的分子才可能是更好的生財之道。”
不過,也有人希望新版本能力再做進一步提升:很多時候,最新的 Alphafold 的相對準確率(RMSD誤差<2A)也只有50-60%,這對于藥物設(shè)計來說往往會有很多問題。
更進一步說,蛋白質(zhì)和小分子復合物的結(jié)構(gòu)預測,應(yīng)該是結(jié)合了AI和CADD兩種方法,即分別基于數(shù)據(jù)庫和物理原理,
第三大升級:預測核酸、以及翻譯后修飾結(jié)構(gòu)。
核酸是關(guān)鍵遺傳信息的攜帶者,并破譯翻譯后修飾--即蛋白質(zhì)誕生后發(fā)生的化學變化。
例如,在 CasLambda 與 crRNA 以及 DNA 結(jié)合的結(jié)構(gòu)中,CasLambda 共享 CRISPR-Cas9 系統(tǒng)的基因編輯能力,通常被稱為“基因剪刀”,研究人員可以利用它來改變動植物和微生物的DNA,而 CasLambda 的較小尺寸可能使其在基因編輯中更加有效。
據(jù)一位從事藥物設(shè)計的公司創(chuàng)始人評價:做核酸藥物的人有福了,至少有個結(jié)果。不過結(jié)果是否準確,還需找個有經(jīng)驗的CADD(計算機輔助藥物設(shè)計)研究員來評估。
此外,也有人指出,“我更關(guān)心 Alphafold 3 是否可以用于預測病毒的蛋白質(zhì)結(jié)構(gòu)。AFDB(數(shù)據(jù)庫)中有很多預測結(jié)構(gòu),幾乎涵蓋了所有物種,但沒有病毒。而且新版本對RNA結(jié)構(gòu)預測還不太好。”
總體而言,至于 AlphaFold 3 具體性能表現(xiàn),DeepMind 和 Isomorphic Labs 研究人員透露:
?考慮到比較系統(tǒng)使用已知的蛋白質(zhì)結(jié)構(gòu)作為基礎(chǔ),AlphaFold 3 在配體對接的準確性方面,優(yōu)于開源分子建模模擬軟件 AutoDock Vina 等傳統(tǒng)系統(tǒng);
?與AlphaFold 2.3相比,AlphaFold 3 在預測蛋白質(zhì)-蛋白質(zhì)結(jié)構(gòu)方面,抗體結(jié)合結(jié)構(gòu)顯著增強;
?此在蛋白質(zhì)-核酸相互作用方面,AlphaFold 3 優(yōu)于其他競爭方法,如RoseTTA2FoldNA等;
?在 RNA 結(jié)構(gòu)預測方面,AlphaFold 3 優(yōu)于自動化技術(shù),但略低于頂級CASP 15 參賽者,后者涉及專家手動干預。
但饒有意味的是,針對最新版本,DeepMind的博客文章并沒有介紹方法,也沒有對比薛定諤的方法。這可能是競爭關(guān)系的原因。
無論如何,從表面上看,AlphaFold 3 的功能有了大幅度的提升,如果真如DeepMind所說,那么新版模型擴展的功能和性能提升可以加速生物醫(yī)學突破,為疾病通路、基因組學、生物可再生材料、植物免疫、潛在治療靶點、藥物設(shè)計機制提供各種全新的可能性。
“AlphaFold3 ”能否繼續(xù)開源?
盡管 AlphaFold 最新版本推出不到兩天,但已經(jīng)有不少人已經(jīng)開始期盼望繼續(xù)開源,“因為學術(shù)界對蛋白質(zhì)的研究已經(jīng)空前高漲。”
一個典型例子是:
盡管 OpenAI 的 ChatGPT 在 2022 年底亮相時就席卷全球,但 2022 年被引用次數(shù)最多的論文并非關(guān)于生成人工智能(AIGC),甚至不是來自大型科技公司,而是歐洲分子生物學實驗室(EMBL-EBI)和 DeepMind 出版的“AlphaFold 蛋白質(zhì)結(jié)構(gòu)數(shù)據(jù)庫”,被引次數(shù)為 1331 次。
更有趣的是,引用量第二同樣屬于“蛋白質(zhì)折疊模型”--ColabFold。該系統(tǒng)由馬克斯·普朗克多學科科學研究所(MPG)打造,引用次數(shù)為 1138 次。
從一定程度上說,盡管企業(yè)界將2022年描述為“生成人工智能年”,但學術(shù)界則認為:2022年絕對是“蛋白質(zhì)折疊預測年”。
“目前 Alphafold 擁有3項以上的專利,這不該是理所當然的,也不該是常態(tài)。不過AF歷代版本確實是目前生物領(lǐng)域最先進的工具,沒有之一。”
更有人指出,“閉源不是最好的解決方案,為什么大多數(shù)國家都傾向于使用AlphaFold ?我有點懷疑大多數(shù)國家是否有人才和預算,來制造像AlphaFold 和蛋白質(zhì)數(shù)據(jù)庫這樣的東西。”
據(jù)悉,DeepMind在 AlphaFold 3發(fā)布當天披露,已累計超過140萬用戶(來自190多個國家)訪問了AlphaFold蛋白質(zhì)結(jié)構(gòu)數(shù)據(jù)庫。
不過未來“AlphaFold 3”能否真正推動藥物開發(fā),還有待時間去驗證。
-
AI
+關(guān)注
關(guān)注
87文章
32439瀏覽量
271628 -
數(shù)據(jù)庫
+關(guān)注
關(guān)注
7文章
3868瀏覽量
65006 -
DeepMind
+關(guān)注
關(guān)注
0文章
131瀏覽量
11059
原文標題:「AlphaFold 3」要來了?DeepMind最新推出新一代蛋白質(zhì)結(jié)構(gòu)預測工具,已用于藥物設(shè)計
文章出處:【微信號:IoT_talk,微信公眾號:醫(yī)健AI掘金志】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
華為依托昇騰AI打造蛋白結(jié)構(gòu)預測工具
差示掃描量熱儀在食品行業(yè)的應(yīng)用

AI for Science:人工智能驅(qū)動科學創(chuàng)新》第4章-AI與生命科學讀后感
AI實火!諾貝爾又把化學獎頒給AI大模型
差示掃描量熱儀測試蛋白質(zhì)的應(yīng)用案例

創(chuàng)客中國AIGC專題賽冠軍天鶩科技:AI蛋白質(zhì)設(shè)計引領(lǐng)者

EvolutionaryScale推出基于NVIDIA GPU模型的新型蛋白質(zhì)研究方案
利用微流控探針誘導的化學質(zhì)膜穿孔,實現(xiàn)單細胞胞內(nèi)蛋白質(zhì)遞送
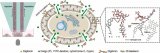
谷歌DeepMind推出新一代藥物研發(fā)AI模型AlphaFold 3
洪亮團隊在生信期刊JCIM發(fā)布最新成果,蛋白質(zhì)工程邁入通用人工智能時代
長電科技近日推出新一代“5G+”通信芯片封裝方案
TE Connectivity推出新一代RAST 5.0高保持力連接器
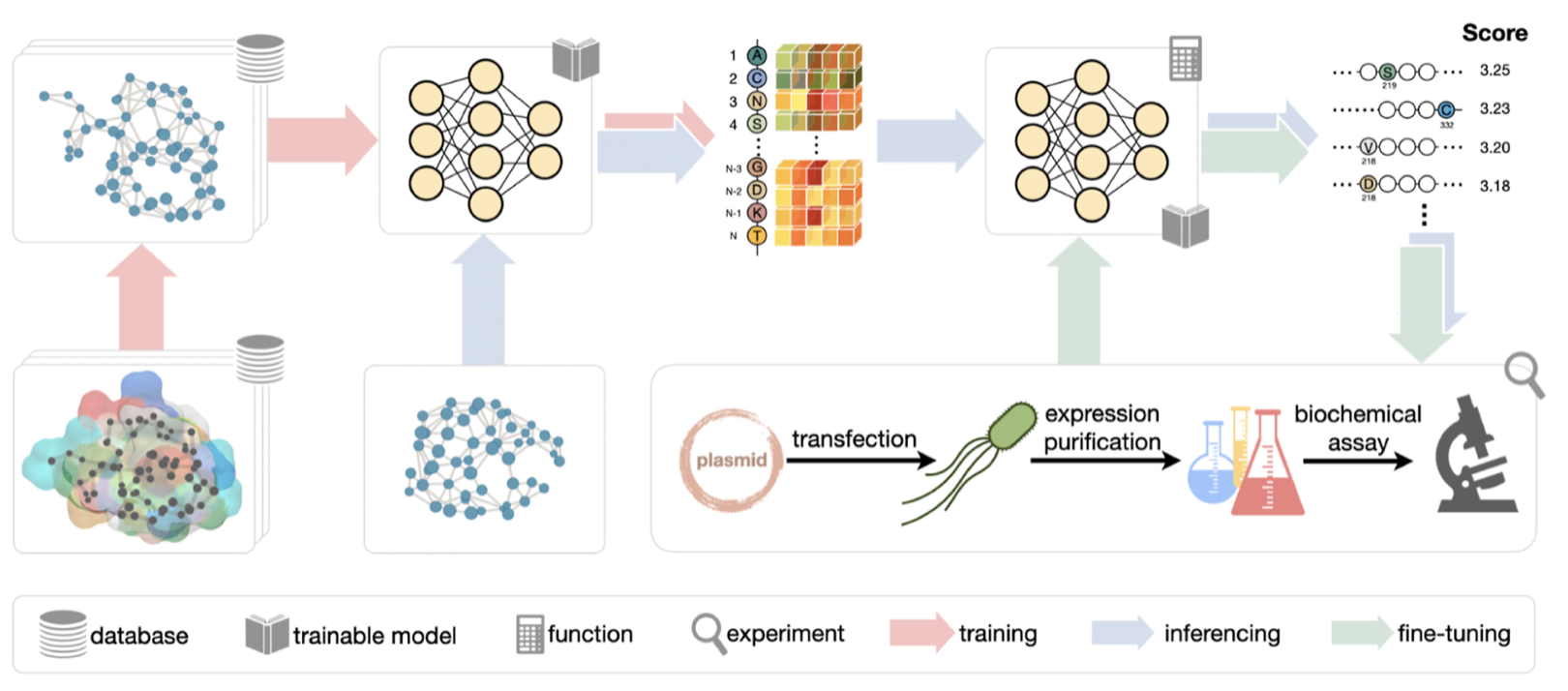
天府錦城實驗室在生物傳感與蛋白質(zhì)測序領(lǐng)域取得重要進展





 DeepMind最新推出新一代蛋白質(zhì)結(jié)構(gòu)預測工具,已用于藥物設(shè)計
DeepMind最新推出新一代蛋白質(zhì)結(jié)構(gòu)預測工具,已用于藥物設(shè)計











評論