急性肝功能衰竭(ALF)是一種嚴重危及生命的疾病,短期內(nèi)會導致大量肝細胞壞死和肝功能快速喪失,具有較高的死亡率。肝細胞移植能迅速支持肝臟生物功能并促進肝臟再生,在ALF治療中展現(xiàn)出巨大的潛力。但目前用于肝細胞移植的細胞來源受限;此外,通過靜脈注射移植的肝細胞在體內(nèi)易被快速清除,限制了其治療效果。針對此,中山大學李明強和陶玉團隊通過體外誘導干細胞分化獲得功能性肝細胞樣細胞,并優(yōu)化其在體內(nèi)的移植和遞送效率。
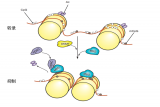
該研究采用Y形DNA納米結(jié)構(gòu)遞送microRNA-122,在體外誘導干細胞的定向分化和成熟。為進一步提高細胞移植效率和治療效果,研究人員運用液滴微流控技術(shù)制備了用于遞送肝細胞樣細胞的保護性微凝膠。研究顯示,當這些肝細胞樣細胞與人臍靜脈內(nèi)皮細胞(HUVECs)在微凝膠中共培養(yǎng)時,其肝功能得到顯著增強。將載細胞微凝膠移植到ALF小鼠體內(nèi),可促進肝功能的恢復和肝臟再生(圖1)。
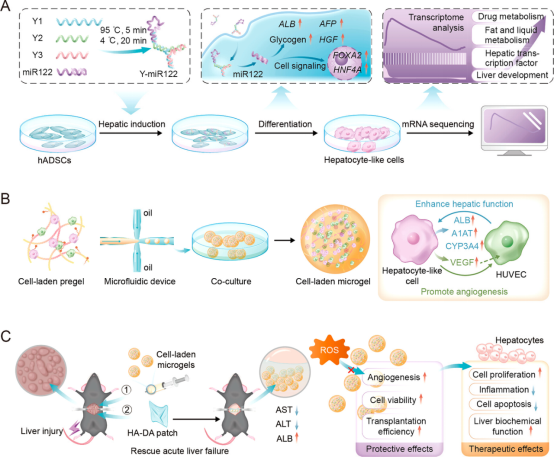
圖1 Y-miR122誘導干細胞分化機制及載細胞微凝膠球體內(nèi)移植用于治療急性肝衰竭的示意圖
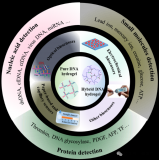
DNA材料具有良好的生物相容性,其序列和結(jié)構(gòu)具有高度可調(diào)控性,通過堿基互補配對作用可高效負載核酸藥物,提高其穩(wěn)定性和細胞攝取效率。本研究使用Y形DNA納米載體增強miR122的細胞內(nèi)遞送效率。如圖2所示,研究團隊首先對Y-miR122的組裝結(jié)構(gòu)和胞內(nèi)遞送效率進行了表征和測試,并驗證了其在體外誘導干細胞肝向分化的生物功能(圖3)。
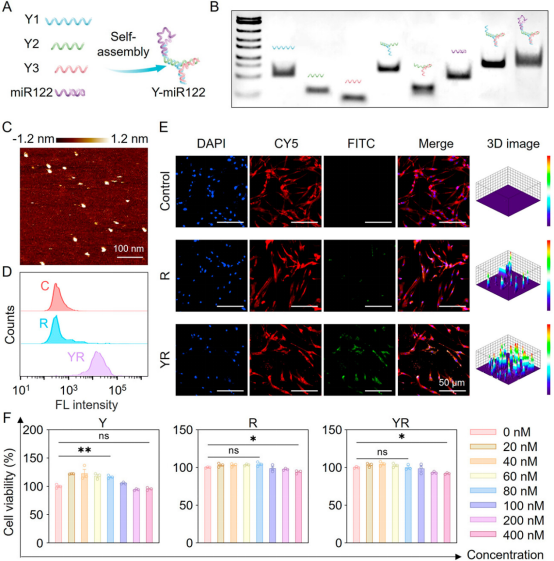
圖2 Y-miR122的制備及表征
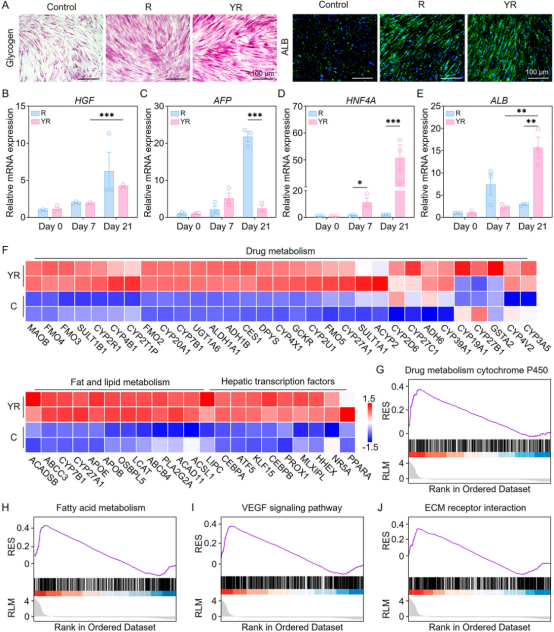
圖3 Y-miR122在體外誘導干細胞的肝向分化
基于微流控技術(shù)開發(fā)的3D微凝膠細胞遞送系統(tǒng)不僅促進了內(nèi)部細胞-細胞和細胞-基質(zhì)的相互作用,還能有效保護封裝細胞免受外界刺激損傷。當Y-miR122誘導的肝細胞樣細胞與HUVECs在微凝膠中共培養(yǎng)時,肝細胞樣細胞的肝功能顯著增強(圖4)。
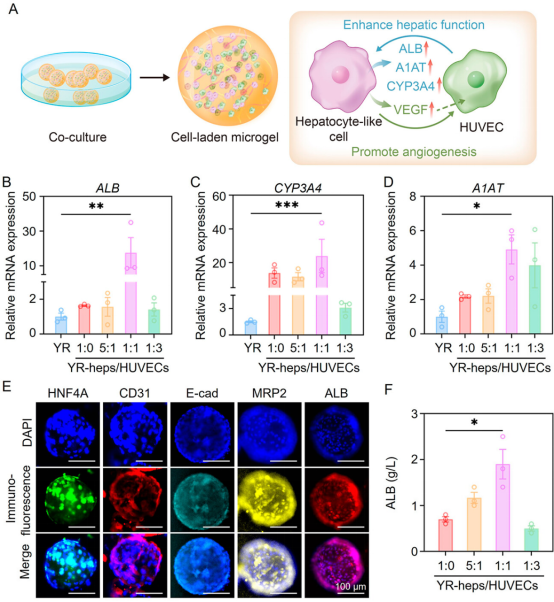
圖4 誘導后的肝細胞樣細胞與HUVECs在基于微流控技術(shù)開發(fā)的微凝膠球內(nèi)共培養(yǎng)
體內(nèi)實驗結(jié)果顯示,載細胞微凝膠顯著降低ALF小鼠的天門冬氨酸氨基轉(zhuǎn)移酶(AST)和丙氨酸氨基轉(zhuǎn)移酶(ALT)水平,緩解小鼠的炎癥,促進小鼠肝功能的恢復和肝臟再生(圖5、6)。進一步對移植物進行表征,發(fā)現(xiàn)載細胞微凝膠治療組具有最高的細胞移植效率和細胞活性(圖7)。上述結(jié)果表明,基于微流控技術(shù)開發(fā)的微凝膠可有效保護移植細胞免受氧化應激微環(huán)境的損害,從而增強移植細胞在ALF治療中的效果。
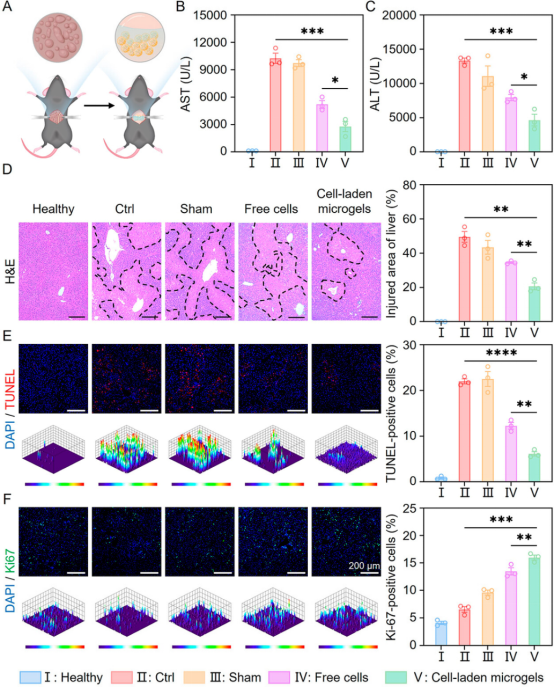
圖5基于微流控技術(shù)開發(fā)的載細胞微凝膠在ALF小鼠模型中的治療效果
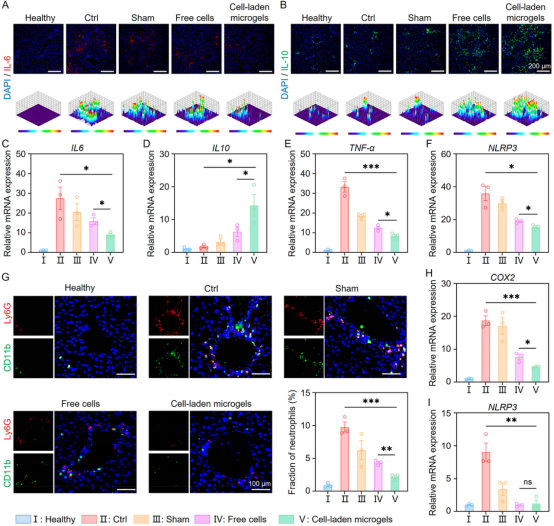
圖6 載細胞微凝膠移植治療可有效減輕ALF小鼠的炎癥
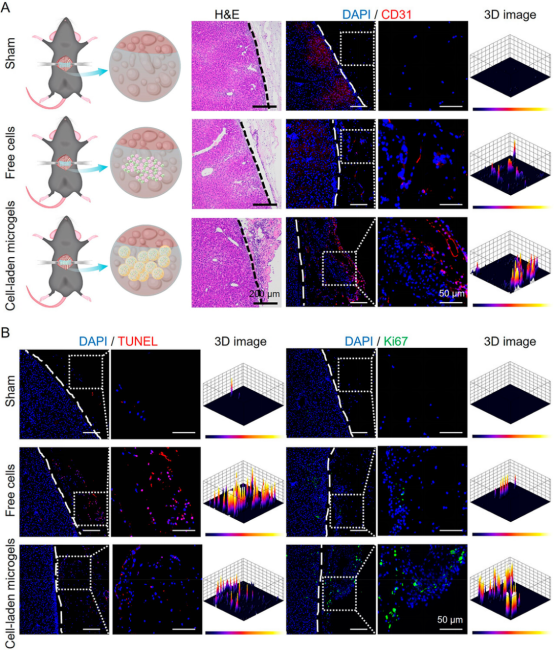
圖7 微凝膠包封策略對體內(nèi)移植的細胞起到保護作用
綜上所述,該研究利用DNA納米材料調(diào)控干細胞分化獲得功能性肝細胞樣細胞,并結(jié)合微流控技術(shù)對其進行包封和遞送,用于肝衰竭治療。該研究為干細胞的定向肝分化提供了新方法,為肝衰竭的細胞治療提供了可靠的細胞來源。
審核編輯:劉清
-
微流控
+關(guān)注
關(guān)注
16文章
526瀏覽量
18891
原文標題:基于微流控技術(shù)和DNA納米材料制備的載細胞微凝膠,用于治療急性肝功能衰竭
文章出處:【微信號:MEMSensor,微信公眾號:MEMS】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
微流控技術(shù)的生物學應用
安泰功率放大器應用領(lǐng)域:微流控技術(shù)和分子結(jié)合的體外診斷研究
微混合器集成技術(shù)的市場前景
ATA-7020高壓放大器在微流控3D細胞微球培養(yǎng)中的應用
微流控芯片3大制作技術(shù)
玻璃微流控芯片前景分析
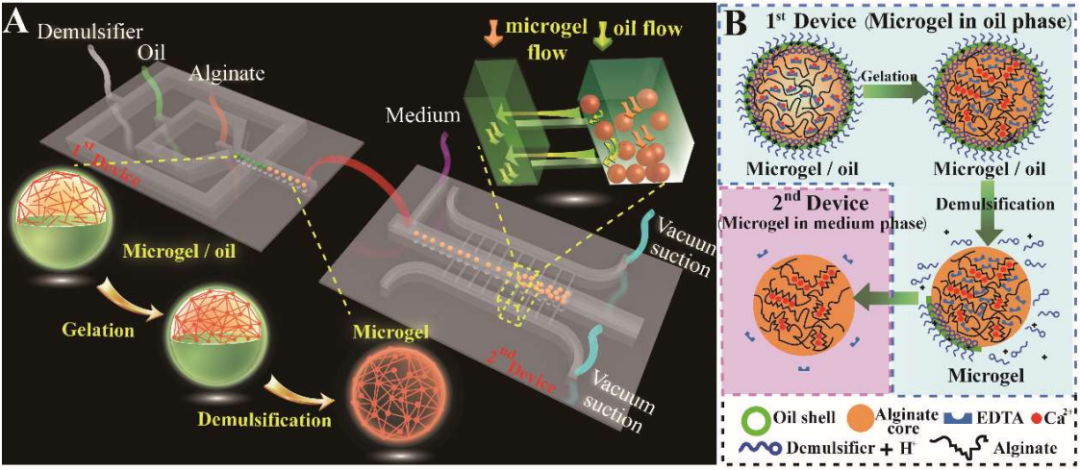
綜述:基于微流控技術(shù)的氧釋放生物材料的制備與應用研究進展
基于顏色變化水凝膠的集成微流控壓力傳感

淺談微流控芯片技術(shù)





 基于微流控技術(shù)和DNA納米材料制備的載細胞微凝膠研究
基于微流控技術(shù)和DNA納米材料制備的載細胞微凝膠研究











評論