石墨烯作為新材料之王,由于其出色的結構、力熱光電和生物學性質,石墨烯能夠應用于生物醫用多個領域,但要實現石墨烯材料的臨床應用,其生物安全性是一個不可忽視的重要問題。
一、石墨烯概述
石墨烯(Graphene)是一種由sp2雜化的碳原子呈蜂窩狀結構緊密排列而成的單原子層二維材料。Andre Geim和Konstantin Novoselov于2004年首次通過微機械力剝離高取向熱解石墨(HOPG)成功制備并觀察石墨烯,二人因此分享2010年諾貝爾物理學獎。
源于其特殊的單原子層二維結構,石墨烯在電子學、光學、力學和熱學等方面擁有出色的性能。2012年,Nature發表了關于石墨烯的前瞻性文章,指出石墨烯在電子學(柔性電子材料、高頻晶體管、邏輯晶體管等)、光子學(光電探測器、光調制器、鎖模激光/太赫茲信號發生器、光學偏振控制器等)、復合材料、涂料、能源、傳感器和生物醫用等領域具有良好的應用前景[1]。碳元素是有機生物體的基本組成元素之一,而且經研究證實,經一定修飾的石墨烯確實具有良好的生物相容性,故石墨烯在生物醫學領域具有天然的優勢。2008年,戴宏杰課題組基于石墨烯材料首次實現藥物傳送,開啟了石墨烯在生物醫用領域研究和應用的新紀元[2]。由于真正意義上的石墨烯難以實現宏量制備,因此實際應用多為石墨烯衍生物,包括少層石墨烯(2~10層)、多層石墨烯(10層以上,但厚度小于100nm)、氧化石墨烯(GO)與經還原的氧化石墨烯(rGO)等。目前,石墨烯和其衍生物經研究證實可應用于藥物基因輸送、復合材料、腫瘤光熱治療、生物成像、電化學生物傳感器、抗菌和組織工程等生物醫用相關領域。
二、石墨烯在生物醫用領域的應用進展
1.石墨烯的結構性質相關應用
石墨烯尤其GO比表面積大,并且在水中有很好的分散性。GO表面含有豐富的含氧官能團,能將各種藥物和生物分子通過化學方式固定在其表面,故在藥物和基因輸送領域具有良好的應用前景。由于呈非水溶性,一些具有良好療效的芳香族藥物難以實現實際應用。戴宏杰課題組通過非共價的π-π相互作用成功將非水溶性抗腫瘤藥物喜樹堿衍生物(SN38)負載到經聚乙二醇修飾的GO表面,可很好分散在水中并保持其出色療效,證明石墨烯是一種出色的藥物載體[2]。陳永勝課題組成功將鹽酸阿霉素(DXR)負載到GO上,并研究了DXR的釋放過程,發現GO對DXR的裝載率可高達2.35 mg/mg,且DXR的裝載率和釋放動力學均可通過調節pH值進行調控[3]。Zhang等人[4]分別對GO進行了磺酸基和葉酸分子修飾以提高其在生理溶液中的穩定分散性和MCF-7細胞靶向性,并將2種抗癌藥物阿霉素與喜樹堿共同負載于其表面,表現出優于單藥物的MCF-7細胞毒性。
除了用于輸送藥物,石墨烯還可作為基因載體用于基因轉染。GO表面含有大量的羧基、羥基等官能團,使其較容易地通過表面修飾得到帶正電荷的石墨烯復合物以用于基因輸送轉染相關研究。目前,聚乙烯亞胺、殼聚糖和1-芘甲基胺等帶正電荷材料已被用于修飾石墨烯并充當基因輸送載體。張智軍課題組[5]研究發現經聚乙烯亞胺(PEI)共價修飾的GO具有更低的細胞毒性,并表現出較PEI更好的基因轉染效果,且能有效地將質粒DNA輸送至細胞核。同時發現經PEI修飾的GO可同時負載siDNA和抗腫瘤藥物DOX,將Bcl-2蛋白特異性的siRNA輸送到腫瘤細胞內可有效下調細胞內Bcl-2蛋白的表達水平,增強細胞對DOX的敏感性,實現基因治療與化療對腫瘤細胞的協同治療。Kim等人的[6]相關研究表明,利用PEG–BPEI–rGO載體在近紅外光的輻照下高效的光熱轉換能力可有效促進負載質粒DNA的石墨烯載體從溶酶體內釋放,實現近紅外光可控的基因輸送。
2.石墨烯的力學性質相關應用
由于其碳原子層二維結構特點,石墨烯具有極好的力學性能,無支撐單層石墨烯的楊氏模量高達1.0 TPa,內稟強度為130GPa。因此,石墨烯可作為二維增強相應用于復合材料領域。
羥基磷灰石(HA)的化學成分、晶體結構與人體骨組織中的磷酸鈣鹽相似,故其具有優異的生物相容性,適宜成骨細胞的粘附、增殖和成骨礦化。但其固有的共價鍵或共價鍵/離子鍵共存的特征,使其斷裂韌性差,降低了HA的可靠性與服役時間。Zhang等[7]選用石墨烯納米片(GNSs)作為HA的二維增強相,研究了HA及GNS/HA復合材料的力學性能(如顯微硬度、彈性模量和斷裂韌性)。結果表明,1.0 GNS/HA(質量分數)的彈性模量、顯微硬度和斷裂韌性分別比HA增加了約40%、30%和80%。GNS的拔出、GNS在晶粒之間的橋接、裂紋橋接、裂紋偏轉等是GNS/HA復合材料中的主要增韌機制。Fan等[8]利用酰胺化反應將酪蛋白磷酸肽接枝到羧基化石墨烯的表面,制備了酪蛋白磷酸肽石墨烯復合物以改善石墨烯的骨整合能力。通過水熱法一步合成了石墨烯/羥基磷灰石納米棒復合新材料,研究發現該復合材料能顯著提高羥基磷灰石的楊氏模量和力學性能。同時,與石墨烯和羥基磷灰石相比,該復合材料中含有40%羥基磷灰石時,表現出更高的骨整合能力、更好的生物相容性及優異的骨細胞繁殖誘導能力。
作為人工關節材料之一,超高分子量聚乙烯(UHMWPE)雖然具有較好的耐磨性能,但在長期使用過程中磨損仍不可避免,產生的磨屑會導致周圍骨溶解,進而引起無菌性松動,影響人工關節服役壽命。通過引入GO制備的GO/UHMWPE復合材料卻表現出更為優異的硬度和在不同潤滑介質下的耐磨性能。聚甲基丙烯酸甲酯(PMMA)義齒基托材料具有出色的仿真美學效果和生物學性能,但其力學性能不能很好地滿足臨床要求,主要表現在耐磨性差等。在其中添加一定量的GO(質量分數約為0.1%),可有效提高其在人工唾液潤滑介質下的耐磨性能。
3.石墨烯的熱學性質相關應用
由于在近紅外光區域具有出色的光熱轉換能力,石墨烯與經修飾的石墨烯被大量研究并用于腫瘤的光熱治療。劉莊課題組于2010年發現與碳納米管不同,經聚乙二醇(PEG)修飾的石墨烯可通過被動靶向富集到腫瘤組織,而且利用其在近紅外區的良好光吸收能力,首次將石墨烯基材料應用于腫瘤的光熱治療[9]。該課題組還較系統地比較研究了具有不同尺寸和表面特性的rGO對體內腫瘤的光熱治療效果,發現水合肼還原的氧化石墨烯經PEG修飾后,在較傳統功率低一個量級的808nm激光輻照下即可實現對腫瘤組織100%的消除。該課題組還制備了一種由四氧化三鐵和金納米粒子共同修飾的具有強順磁性和高近紅外吸收能力的氧化石墨烯納米結構GO-IONP-Au,并經PEG處理獲得了可在生理環境中穩定存在的GO-IONP-Au-PEG,體內和體外實驗結果均證明該復合材料無顯著毒性,且具有增強的腫瘤光熱治療效果。戴宏杰課題組研究發現,經PEG修飾后超小尺寸(約20nm)的rGO較GO具有更高的近紅外區光吸收能力,可實現對腫瘤細胞的光熱殺傷,且在所需劑量下并無明顯生物毒性[10]。除通過光熱治療直接殺死腫瘤細胞,石墨烯的光熱轉換效應還被廣泛應用于腫瘤的協同治療相關研究中。
4.石墨烯的光學性質相關應用
由于具有良好的分散穩定性、生物相容性和較強的熒光成像效果,石墨烯基材料作為一種新興的熒光成像材料在生物活體成像領域具有廣泛的應用前景。石墨烯自身在近紅外光激發下即可發出熒光,且將一些熒光染料通過共價或非共價方式連接到石墨烯上可獲得具有更優熒光性能的復合物。戴宏杰課題組制備了可在生理環境中可穩定存在的聚乙二醇化的氧化石墨烯(GO-PEG),并發現GO-PEG在可見和近紅外光區均存在良好的光致發光性能,且易與細胞的自發熒光區分開,因此可用于進行細胞成像。Yang等[9]將染料Cy7連接到經聚乙二醇修飾的GO上,并通過靜脈注射方式將其注入種植有腫瘤的小鼠體內,1天后經Cy7修飾的石墨烯大量富集在腫瘤內部,并呈現出強烈的熒光,實現了腫瘤的標記檢測。此外,石墨烯量子點(GQDs)具有優異的水中分散性、出色的生物相容性和光致發光性質,是一種新興的生物成像材料,可作為一種出色的細胞標記和成像材料。
5.石墨烯的電學性質相關應用
石墨烯可促進電子傳遞,對一些生物小分子表現出優異的電催化行為,同時電化學檢測方法具有易攜帶、靈敏度高、成本低等優點,故在高性能電化學生物傳感器領域,石墨烯也受到廣泛關注。為研究石墨烯在電化學生物傳感器領域的應用前景,有必要對其基礎電化學行為進行研究。Zhou等人[11]發現經rGO修飾的玻碳電極在0.1 M磷酸緩沖液中的電位窗口高到2.5V,與石墨修飾電極和玻碳電極接近,且對于多種無機和有機電活性化合物的電化學相應,rGO修飾電極表現出更低的電荷轉移電阻。簡便快捷地檢測葡萄糖在預防、診斷和治療糖尿病中具有重要意義。石墨烯作為電極表面和葡萄糖氧化酶氧化還原中心的導電原件,可很好地保持葡萄糖氧化酶的生物活性,并促進電子信號從酶的活性中心向電極表面的傳遞。且由于石墨烯具有較大的比表面積,酶可較好負載于其表面,基于此構建的葡萄糖氧化酶電化學生物傳感器具有較寬的檢測范圍。
在食品、醫藥、臨床、人體健康等領域,過氧化氫(H2O2)、煙酰胺腺嘌呤二核苷酸(NADH)和多巴胺等生物分子的電化學檢測具有重大的意義。經石墨烯修飾的電極具有出色的電催化活性,且其邊緣存在的缺陷可作為活性位點,提高被檢測生物分子的電子轉移速度,降低電子轉移電阻。石墨烯修飾的電極可在同時存在多種生物分子的條件下,對其中一種分子進行檢測,具有分離效果好和檢測限低等優點。
在檢測選定DNA序列和疾病相關變異基因方面,電化學DNA傳感器具有靈敏度高、選擇性高和成本低等優點,有望提供一種簡單、準確和廉價的臨床檢測平臺。石墨烯具有較寬的電勢窗口,可直接檢測氧化還原電位較高的核酸分子。Zhou等[11]報道了基于rGO的DNA電化學傳感器,該傳感器可有效區分DNA的4個自由基(鳥嘌呤、腺嘌呤、胸腺嘧啶和胞嘧啶)在電極上的電化學反應,并可在不需水解的前提下同時測定ssDNA和dsDNA。
6.石墨烯的生物學性質相關應用
(1)石墨烯的抗菌性
Hu等人于2010年首次發現氧化石墨烯(GO)和還原后的氧化石墨烯(rGO)均具有優異的抗菌性[12],通過真空抽濾方法制備的GO和rGO膜同樣表現出優異的抗菌性。深入研究結果表明,GO和rGO片層結構的邊緣堅硬,可能會對大腸桿菌等細菌的細胞膜造成損傷。Akhavan等人[13]通過電泳沉積方法在不銹鋼基底表面制備了GO薄膜,并通過水合肼還原得到了rGO薄膜,兩者均會對細菌細胞膜的完整性產生破壞從而表現出優異的抗菌性。rGO薄膜較GO薄膜表現出對革蘭氏陰性菌(大腸桿菌)與革蘭氏陽性菌(金黃色葡萄球菌)更好的抑制效果,這主要是由于當具有更加鋒利邊緣的rGO與細菌相互作用時具有更好的電荷轉移特性。Akhavan等人進一步發現,團聚的GO和rGO能夠通過捕獲大腸桿菌使其與外界環境相分離,細菌由于不能有效獲得營養成分而停止生長甚至死亡,因此GO和rGO表現出良好的抗菌性。Liu等人[15]通過比較發現石墨烯基材料的結構性質、片層大小均會影響其抗菌性能。在相同條件下,GO表現出最好的抗菌性,其次分別是rGO、石墨和氧化石墨;大尺寸GO具有更加優異的抗菌性能。同時發現石墨烯基材料的抗菌性主要來源于其尖銳的邊緣與細菌的細胞膜相接觸時而產生的膜應力,超氧陰離子氧化應激也是抗菌原因之一。Fan等人[16]合成了不同質量比的銀/石墨烯復合物,然后與聚丙烯酸和聚甲叉雙丙烯酰胺交聯制成石墨烯復合水凝膠。當水凝膠中銀與石墨烯的質量比為5:1時,該水凝膠表現出較好的力學性能以及優異的抗菌性和生物相容性。由于GO的制備簡便、成本低廉,GO的抗菌性有望在環境和臨床領域得到廣泛的應用。不過,Ruiz等人研究發現[17]GO分散液和薄膜不但未能抑制細菌的增殖,反而起到促進細菌生長的作用。他們認為在之前研究中,GO之所以能夠起到抗菌作用,其來源可能是GO制備過程中遺留的污染物或低估了GO濃度,而他們所使用的是經長時間透析的含雜質比較少的GO。這說明GO的制備工藝和質量均會嚴重影響細菌數量。
(2)石墨烯促進細胞生長分化
Ruiz等人[17]發現GO薄膜可以通過促進哺乳動物細胞的粘附和增殖而提高其生長能力。石墨烯具有較低的細胞毒性,可加快骨髓間充質干細胞(hMSCs)向成骨細胞分化,其誘導分化速度與BMP-2相差無幾。石墨烯表面適宜成骨細胞在其表面進行貼附,而且成骨細胞的貼附則直接關系著其增殖、分化等細胞活動,同時也有研究發現石墨烯有利于磷酸鹽和鈣鹽在其表面礦化,即成骨礦化能力優異,這一系列的細胞活動對植入體表面新骨的生成具有促進作用。Chen等人[18]研究發現iPSCs可在GO和rGO表面粘附和增殖,但rGO會抑制iPSCs的分化,而GO卻可以促進其分化,石墨烯的不同表面特性是調節iPSCs生長和分化行為的重要因素。石墨烯材料在骨組織工程領域具有良好的應用前景。
石墨烯具有良好的生物相容性,可促進hNSCs的粘附并誘導其向神經元細胞分化而不是神經膠質細胞,且能夠明顯提升神經突的數量和平均長度,是一種潛在的神經接口材料。程國勝和戴建武等[19]合作開發了一種三維石墨烯泡沫神經干細胞支架材料3D-GFs。神經干細胞可在3D-GFs表面粘附增殖,且可進一步定向分化為星形膠質細胞尤其是神經元細胞。美國西北大學Ramille Shah課題組開發出了可3D打印石墨烯油墨(石墨烯含量高達60%),該油墨除石墨烯之外的材料是主要具有良好生物相容性的可降解聚酯材料,這使得其能夠靈活安全地應用于生物醫用領域(圖1)。體內實驗證實采用該油墨3D打印的石墨烯支架結構具有良好的生物相容性。體外實驗表明,石墨烯支架不會影響干細胞生存,且能促進其繼續分裂、增殖并轉化成類似神經元的細胞。石墨烯有望在神經組織工程及神經干細胞移植治療等領域得到應用。
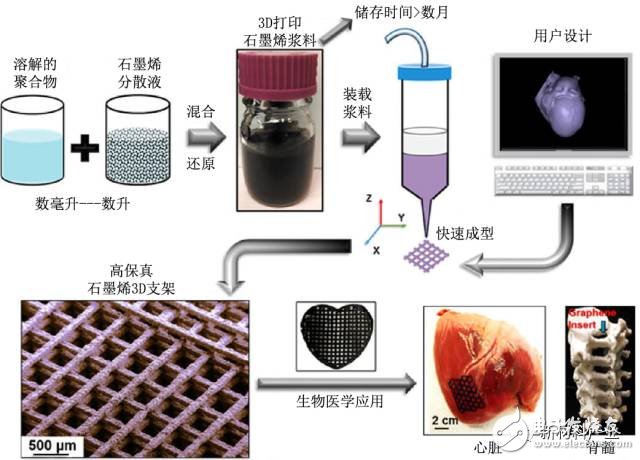
圖1.可根據需要采用3DG漿料通過3D打印制備適于不同用途的石墨烯結構
三、石墨烯的生物安全性
由于其出色的結構、力熱光電和生物學性質,石墨烯能夠應用于生物醫用多個領域,但要實現石墨烯材料的臨床應用,其生物安全性是一個不可忽視的重要問題。石墨烯的主要組成元素是碳,而碳是組成生物有機體內最基本的元素之一,因此石墨烯材料在生物醫用應用中具有天然的優勢。由于制備工藝不同,石墨烯與其衍生物材料的物理化學性質(如尺寸大小、結構形狀、表面化學狀態等)不盡相同,因此其與生物分子、細胞、組織和器官等相互作用方式多種多樣。但目前大量研究表明石墨烯是一種生物相容性良好的碳納米材料。
細胞毒性是評估材料生物安全性的重要指標之一。石墨烯材料一般均表現出較低的細胞毒性。雖個別研究發現GO呈現出較高的溶血率,但經過聚乙二醇、殼聚糖、吐溫、人工過氧化物酶、葡聚糖、蛋白等修飾后,石墨烯材料的細胞毒性能顯著降低。動物毒性是評估材料生物安全性的又一重要指標。雖石墨烯與其衍生物可在肺部富集并存在較長時間,進而導致肺部水腫和肉芽腫瘤的形成,誘發肺部損傷,但經聚乙二醇、葡聚糖、殼聚糖等聚合物修飾可顯著降低石墨烯基材料的體內毒性。且有研究表明,生物體內存在的辣根過氧化物酶、人髓過氧化物酶等酶分子會引發石墨烯材料的降解,這種酶促降解行為可在很大程度上降低石墨烯材料的生物毒性尤其是長期生物毒性,使其更為安全有效地應用于生物醫用領域。
因其出色的結構、力學、熱學、光學、電學和生物學等性質,石墨烯和其衍生物有望廣泛應用于藥物/基因輸運、生物材料、腫瘤的光熱治療、生物熒光成像、組織工程、電化學生物傳感和抗病毒/抗菌等生物醫用領域。石墨烯在生物醫用領域的巨大研究進展是鼓舞人心的,但不能否認所面臨的挑戰也同樣艱巨。由于石墨烯基材料的多樣性和生物系統的復雜性,對石墨烯與生物分子、細胞、組織、器官乃至生物體相互作用的機制缺乏系統詳盡的研究。目前,石墨烯作用于生物分子和細胞后引發的生理生化反應以及機制通過體外實驗取得了一些積極成果,但體內實驗研究甚少。毫無疑問,如何在保持石墨烯材料出色特性的前提下,改善其生物相容性和穩定性是值得研究的重要方向。同時也應注意到,石墨烯雖然具有眾多優異性質,但并非“萬能材料”,需針對各具體應用對其進行修飾改進,開發相應的石墨烯衍生材料,這就需要具有不同學科背景的科研人員共同協作努力攻關。不過,隨著研究的不斷開展和深入,石墨烯材料必將在不遠的將來在生物醫用診斷和治療領域取得實質應用。


 詳解石墨烯生物醫用領域的應用
詳解石墨烯生物醫用領域的應用















評論